赛诺菲今日(1月9日)宣布,旗下抗CD38单抗赛可益®(艾沙妥昔单抗注射液)获得国家药品监督管理局(NMPA)批准,用于与泊马度胺和地塞米松联合用药,治疗既往接受过至少一线治疗(包括来那度胺和蛋白酶体抑制剂)的多发性骨髓瘤成人患者。
此次获批基于全球III期ICARIA-MM研究结果以及中国IsaFiRsT真实世界研究结果。ICARIA-MM研究结果显示艾沙妥昔单抗注射液与Pd联合疗法(Isa-Pd)可显著降低40%疾病进展或死亡风险,延长无进展生存期(PFS)近两倍,并延长总生存期(OS),展现出有临床意义的生存获益。在中国开展的真实世界研究IsaFiRsT结果显示中国复发或难治性多发性骨髓瘤(RRMM)患者的总体缓解率(ORR)达到82.6%。
在今年更新的中国临床肿瘤学会(CSCO)与中国抗癌协会(CACA)指南中先后新增Isa-Pd联合疗法为“I级推荐”*与首次复发MM患者“首选方案”**。更新的美国国立综合癌症网络(NCCN)多发性骨髓瘤诊疗指南中,Isa-Pd联合疗法仍作为RRMM患者“优先推荐”***。
近年来,NMPA在积极探索将真实世界数据(RWE)应用于药械产品的审评审批,促进国际先进药品及医疗器械尽快进入中国市场惠及患者。作为在乐城先行区开展真实世界数据研究的药品,如今赛可益®也成为首个基于乐城真实世界研究数据作为关键证据获得批准的血液肿瘤治疗药物。
乐城先行区管理局党委书记、局长贾宁表示:“赛可益®获批是博鳌乐城临床真实世界数据应用试点的又一重要成果。作为中国唯一的‘医疗特区’,乐城先行区充分发挥特许药械和真实世界研究政策双重优势,为全国药械审评审批制度改革探索新工具、新标准和新方法,其中赛可益®就是‘乐城真研速度’的代表之一。未来,我们将持续与监管部门、临床机构、科研院所、药械企业等携手,以患者需求为中心,加快释放特许政策和优质医疗资源集聚效能,引进更多创新、高质量的产品,不断加速创新可及,为广大患者提供更多治疗选择,助力中国健康事业创新发展。”
赛诺菲大中华区总裁施旺表示:“赛诺菲一直致力于将全球领先的突破性创新药物加速引入中国。赛可益®在华获批标志着赛诺菲在肿瘤领域的全新开端,也展现了产品创新与乐城真研创新加速的‘双创新’叠加效应,为更多中国多发性骨髓瘤患者带来更长生存、更高质量生活的希望。未来,我们将聚焦患者需求,不断推动创新药物研发可及以及多元合作创新模式,共筑健康中国2030。”
ICARIA-MM研究显示:Isa-Pd治疗组和Pd治疗组中位PFS分别为11.5个月和6.5个月(HR=0.596;P=0.001)。相较Pd疗法,Isa-Pd联合疗法可显著降低40%疾病进展或死亡风险,延长PFS近两倍。随访52.4个月的中位OS分别为24.6个月和17.7个月(HR=0.78;P=0.0319),Isa-Pd延长患者中位OS 6.9个月,从而产生有临床意义的生存获益。并且,Isa-Pd相较Pd治疗组的至首次缓解中位时间分别为35天和58天,≥VGPR率高达31.8%,达到Pd治疗组的4倍左右,更短中位时间达成深度缓解1。随着随访时间的延长,Isa-Pd组未发现新的安全性问题。在亚组分析中,无论难治性状态如何(来那度胺难治性患者、蛋白酶体抑制剂难治性和双重难治性患者),Isa-Pd均可改善患者PFS。IsaFiRsT真实世界研究与全球III期ICARIA-MM研究结果一致,并且研究数据显示,Isa-Pd联合疗法对中国复发或难治性多发性骨髓瘤患者的总体缓解率达到82.6%。
现任上海交通大学医学院附属瑞金医院副院长、上海血液学研究所所长、上海市重中之重临床医学中心主任、IsaFiRsT真实世界研究主要研究者赵维莅教授表示:“艾沙妥昔单抗注射液的获批为多发性骨髓瘤首次复发的创新治疗提供了重要支柱,基于IsaFiRsT的研究结果也为我们在中国患者人群中的使用带来了信心。同时,艾沙妥昔单抗注射液是利用真实世界研究为全国药械审评审批制度改革积累经验、探索方法的有力诠释。本次瑞金海南医院用时仅238天快速推进完成了该项目。我们期待未来能够将更多创新、优质的药物通过真研路径落地中国。”
多发性骨髓瘤是第二大最常见的恶性血液肿瘤,高发于老年群体。在中国每10万人中就有约1.6个新发多发性骨髓瘤患者,发病率呈上升趋势。根据国家统计局最新数据显示,截至2023年底,全国60岁及以上老年人口达2.9亿,占全国人口的21.1%。多发性骨髓瘤已逐渐成为庞大老年群体的“健康杀手”。目前多发性骨髓瘤仍是不可治愈的癌症,患者终将面临复发困境。临床上患者复发的次数越多,治疗难度也随之增加,患者无进展生存和复发后的生存时间也就越短。
苏州大学附属第一医院血液科主任、国家血液系统疾病临床医学研究中心常务副主任、中华医学会血液学分会第十一届主任委员吴德沛教授表示:“过去几十年,中国血液肿瘤如多发性骨髓瘤的创新发展不断推进,诊疗能力也不断提升。在当前中国迈向重度人口老龄化的时代背景下,多发性骨髓瘤已不仅是癌症生存问题,更成为健康老龄化的关键议题。多发性骨髓瘤患者面对复发以及复发后耐药难治的‘双重困境’,仍有巨大未尽之需。本次获批的全新抗CD38单抗为多发性骨髓瘤患者抓住首次复发的关键治疗窗口提供了创新武器,推动更早的生存获益。随着更多创新疗法引入,诊疗规范化与学术建设快速推进,多发性骨髓瘤等血液肿瘤将成为重要切入口,助力‘健康中国’2030癌症总体5年生存率目标的达成。”
备注:
*《2024年CSCO恶性血液病诊疗指南》对各类型RRMM患者均新增Isa-Pd方案为I类推荐。
**第二版《中国肿瘤整合诊治指南(CACA)—癌肿篇》新增Isa-Pd方案为首次复发MM来那度胺耐药CD38敏感的首选方案。
***2025年v1版美国国立综合癌症网络(NCCN)《多发性骨髓瘤指南》仍在硼替佐米、来那度胺耐药的RRMM患者中,将Isa-Pd方案作为“优先推荐”。
来源:医谷网
为你推荐
 资讯
资讯 国家医保局:医保领域2025年度第一批重点事项清单
2025年底前,全国80%左右统区基本实现与定点医药机构即时结算。基本实现医保部门与医药企业对集采药品的直接结算,加快推动与医药企业对集采医用耗材、国谈药的直接结算。
2025-02-18 21:14
 资讯
资讯 “悦如初,达新程” 2025特应性皮炎免疫创新学术会议于成都举办
特应性皮炎是一种慢性、复发性、炎症性皮肤病,在非致命性皮肤疾病中疾病负担位列第一,给患者个人及家庭带来沉重的生理、心理负担,造成长期的社会影响。
2025-02-18 10:58
 资讯
资讯 拜耳在欧盟申请EyleaTM 8mg治疗间隔延长至6个月
拜耳已向欧洲药品管理局(EMA)提交申请,将EyleaTM 8mg(阿柏西普8mg,114 3mg ml注射液)用于治疗两种主要视网膜疾病,即新生血管(湿性)年龄相关性黄斑变性(nAMD)和糖...
2025-02-17 19:55
 资讯
资讯 EyleaTM 8mg延长给药间隔治疗湿性年龄相关性黄斑变性的长期疗效和安全性在三年时得到证实
近日,在于美国迈阿密举行的第22届新生血管年会上,拜耳及其合作伙伴Regeneron公布了PULSAR开放标签扩展研究治疗新生血管(湿性)年龄相关性黄斑变性(nAMD)患者第三年的临床试验结果。
2025-02-17 19:44
 资讯
资讯 备思复(维恩妥尤单抗)联合疗法全国首张处方落地,开启泌尿肿瘤精准治疗新篇章
2025年2月17日,北京大学肿瘤医院泌尿肿瘤暨黑色素瘤肉瘤内科主任、中国临床肿瘤学会副理事长兼秘书长郭军教授为一位晚期尿路上皮癌患者开具备思复(维恩妥尤单抗)联合帕博利珠...
2025-02-17 19:38
 资讯
资讯 安诊儿率先融合DeepSeek-R1,升级大模型底座能力
2月16日,由浙江省卫健委和蚂蚁集团联合推出的 "安诊儿 "宣布融合DeepSeek-R1,升级大模型底座能力,成为国内首批支持专业推理模型的AI医疗健康应用之一。
2025-02-16 15:46
 资讯
资讯 驯鹿生物CAR-T细胞产品伊基奥仑赛注射液申请香港上市
2025年2月14日,驯鹿生物宣布,中国香港卫生署已正式受理其CAR-T细胞产品伊基奥仑赛注射液(FUCASO)的新药上市许可申请(NDA),用于治疗既往经过至少3线治疗后进展的复发 难治...
2025-02-15 20:59
 资讯
资讯 辉瑞公布TALAPRO-2研究最新数据:泰泽纳®联合恩扎卢胺可显著改善转移性去势抵抗性前列腺癌患者生存结局
泰泽纳®(甲苯磺酸他拉唑帕利胶囊)联合恩扎卢胺是目前首个在转移性去势抵抗性前列腺癌(mCRPC)的治疗中,无论患者是否携带HRR 基因突变,均显示出统计学显著和临床意义上总...
2025-02-14 19:17
 资讯
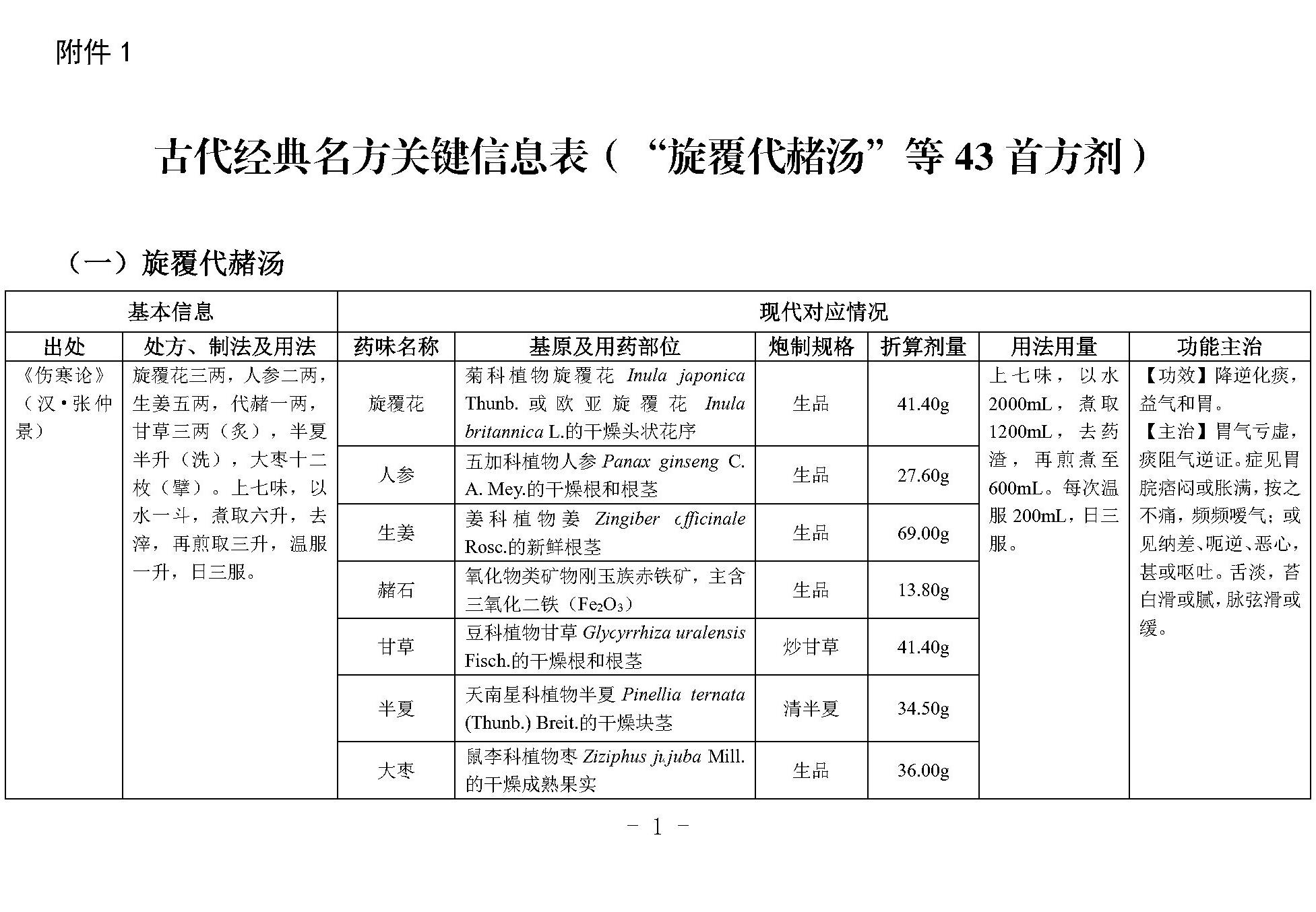
资讯 旋覆代赭汤、吴茱萸汤、猪苓汤、甘草泻心汤黄连汤等43首方剂古代经典名方关键信息表发布
国家中医药局、国家药监局积极组织推进古代经典名方关键信息考证研究工作,现将《古代经典名方关键信息表(“旋覆代赭汤”等43首方剂)》予以公布。
2025-02-14 16:42
 资讯
资讯 艾捷博雅完成数亿人民币C轮融资,加速分离纯化技术研发与市场拓展
艾捷博雅成立于2020年8月28日,总部位于中国江苏省,是一家依托分离材料、流体自动化技术、在线检测技术的高科技企业。
2025-02-14 10:18
 资讯
资讯 诺美新创完成超3亿元融资,专注耳鼻喉及颅脊外科器械研发与创新
此次融资将为诺美新创的市场拓展和产品研发提供强有力的资金支持,进一步巩固其在耳鼻喉及颅脊外科器械领域的领先地位。
2025-02-14 10:08
 资讯
资讯 NMN/NR一项权威研究数据公布
在科技的发展过程中,科学家从未停止对健康长寿的研究。2014年哈佛教授Sinclair发现,对老年小鼠补充NMN NR可提高体内辅酶I水平,延长小鼠的寿命[1]。这项研究使NMN NR成为世...
2025-02-13 19:24
 资讯
资讯 司美格鲁肽注射液新适应症在中国申报上市
近日,据国家药监局药审中心信息显示,诺和诺德申报的司美格鲁肽注射液新适应证上市申请已获得受理,注册分类为进口3 1,虽尚无具体适应症信息披露,但根据以往诺和诺德披露公...
2025-02-13 12:27