2025年1月2日,华东医药(000963.SZ)发布公告,独家经销产品注射用重组A型肉毒毒素YY001用于改善中度至重度眉间纹的上市许可申请获国家药品监督管理局受理。
据悉,YY001是由华东医药参股公司重庆誉颜制药有限公司自主创新研发并拥有全球知识产权的注射用重组A型肉毒毒素,与天然肉毒毒素具有一致生物功能和药理药效作用,具有高纯度、良好的安全性及生产可扩展性等多种优点。
华东医药拥有YY001在中国大陆、香港特别行政区、澳门特别行政区医美适应症领域的独家商业化权益及相关优先受让权、优先谈判权。
YY001借助重组蛋白技术,树立肉毒素领域新里程碑
公告显示,YY001注册上市许可申请的受理,是基于一项在中国进行的多中心、随机、双盲、安慰剂及阳性药平行对照的Ⅲ期临床试验。YY001在大规模人群的III期临床研究结果显示,其有效性、安全性和免疫原性都达到了既定的临床试验终点,与对照药相比表现优异。
A型肉毒毒素产生高活性的作用原理已得到深入的研究并获得普遍的共识, 也是临床应用最广泛的肉毒素。目前,国内外所有A型肉毒素的产品都来自致病性肉毒杆菌,安全生产风险高。此外,绝大多数A型肉毒毒素产品都有活性蛋白纯度低的缺陷。
重组蛋白技术有望成为众多缺陷的解决方案,然而,重组蛋白技术路线是极为复杂的系统工程,门槛极高、难度极大。
值得一提的是,YY001是全球首款且目前唯一已递交上市申请的重组A型肉毒毒素产品。YY001在不改变蛋白活性的基础上,避免了传统技术路线使用肉毒杆菌生产肉毒毒素的生物安全风险;通过全套创新设计的生产工艺,所生产的重组肉毒毒素具有纯度高、比活性高、免疫原性低的特征,被业内视为新一代肉毒毒素。
目前,肉毒素市场尚处于蓝海赛道,发展潜力巨大。根据ISAPS(国际美容整形外科学会)发布的数据,近5年来肉毒素治疗量稳居全球医美非外科手术处理类TOP 1,从2019年的627.1万例增长到2023年的887.8万例,五年内增长约40%,市场规模不断扩大。在国内,肉毒素市场同样表现强劲。根据弗若斯特沙利文的数据,2017-2021年,中国肉毒素产品的市场规模由人民币19亿元增加至人民币46亿元,复合年增长率为25.6%,预计市场规模将于2025年及2030年分别达到人民币126亿元及人民币390亿元。
随着人们对美的追求不断提升,国内肉毒素市场有望保持高增长。不仅市场广阔,肉毒素应用范围同样广阔,可实现医学+美学双应用。肉毒素首先被FDA批准应用于斜视的临床治疗,现已广泛运用于神经、康复及泌尿等临床治疗领域。在我国,随着大量肉毒素的临床应用,其适应症也正在被逐步开发,向其他医疗应用拓展。YY001用于治疗成人上肢肌肉痉挛的临床研究(代号YY001-002)亦于2024年7月在中国进入II期临床试验阶段,预期将在全球范围内首先将重组A型肉毒毒素应用于医疗领域,占据先发优势。
本次重组A型肉毒毒素YY001的药品注册上市许可申请顺利获得受理是该款药品研发进程中的又一重要进展,将进一步提高华东医药在医美面部注射剂领域的市场竞争力。
华东医药深耕高端医美市场,纵深发展注射针剂领域
华东医药持续布局医美领域,丰富注射类产品管线,为求美者提供一站式面部完整美学解决方案。截至目前,在注射剂领域,华东医药旗下已经拥有多款重要产品,包括Ellansé®伊妍仕®、MaiLi系列玻尿酸、Lanluma®V型及X型再生针剂、肉毒素产品YY001等,在注射类产品领域实现再生类、玻尿酸、肉毒素三大品类的全覆盖,每个品类均已形成两个以上差异化产品管线。
Ellansé®伊妍仕®是华东医药医美的核心产品之一,因出色的“即时填充+长效维持+自然代谢”三重效果被冠以“少女针”的称号。Ellansé®伊妍仕®S型已在国内上市,是国内首款获批的三类医疗器械认证的进口PCL高端面部填充剂,且新增 “额部填充改善额部轮廓”适应症于2024年11月完成全部受试者入组;Ellansé®伊妍仕®M型已于2024年10月完成中国临床试验18个月安全性随访。
2024年7月,MaiLi系列玻尿酸在新加坡顺利上市、积极开拓新市场,其于2021年上半年在欧洲市场上市,获得了积极的市场反馈。华东医药正持续推进MaiLi系列产品的国内注册进程,针对MaiLi 系列中MaiLi Precise、MaiLi Extreme两款产品进行了国内的临床试验。作为MaiLi系列中透明质酸钠浓度最低的一款,MaiLi Precise完成了中国临床试验全部受试者的主要终点随访。此外,MaiLi系列中含透明质酸浓度最高、丰盈能力最强的MaiLi Extreme已于2024年4月递交国内注册申请并获得受理,有望于2025年内获批。
此外,华东医药另一款再生医美填充剂聚左旋乳酸胶原蛋白刺激剂Lanluma®的临床试验也在如火如荼地推进中。2024年11月,Lanluma® V用于改善下颌缘轮廓缺陷临床试验皆已完成全部受试者入组。Lanluma®是目前全球唯一一款被批准可用于臀部和大腿填充的再生型产品,该产品于2020年获得欧盟CE认证,截止目前已在全球32个国家和地区获批上市销售。
华东医药在国际上持续推进注射填充管线的临床布局,加速高端医美全球化进程。公司旗下一款全新专利成分的真皮注射填充剂KIO021中国临床试验顺利启动。KIO021与KIO015成分相同,规格不同,KIO015已于2024年7月提交欧盟CE认证申请,预计将于2025年获得欧盟CE-MDR认证。华东医药表示,届时KIO015将有望成为全球首个非动物源性壳聚糖医美填充剂。
从整体产品管线布局来看,华东医药已经在全球范围内实现非手术类医美注射产品和能量源器械中高端市场全覆盖,产品组合覆盖改善眉间纹、面部及身体填充、埋线、皮肤管理、身体塑形、脱毛、私密修复等非手术类主流医美领域。公司已拥有“微创+无创”医美国际化高端产品40款,其中海内外已上市产品达26款,在研全球创新产品14款,华东医药通过医美全球化经营布局,着力打造国际化品牌硬实力。
展望未来,华东医药持续推进管线临床进展,将有更多的医美新品获批,为医美市场带来新的活力。华东医药致力于成为医美领域的技术引领者和市场领导者,以其卓越的产品力和品牌影响力,为全球求美者提供更专业、安全、高效及全面的综合解决方案,开启公司医美发展新篇章。
为你推荐
 资讯
资讯 国务院办公厅关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见
将药品注册检验、生物制品批签发检验和进口药品通关检验每批次用量从全项检验用量的3倍减为2倍。将仿制药质量和疗效一致性评价逐步向滴眼剂、贴剂、喷雾剂等剂型拓展。
2025-01-04 13:23
 资讯
资讯 首个干细胞药物获批,间充质干细胞防治移植物抗宿主病临床试验技术指导原则(试行)
2024年1月12日,国家药监局药品审评中心曾发布了《间充质干细胞防治移植物抗宿主病临床试验技术指导原则》。
2025-01-04 11:25
 资讯
资讯 国内首款干细胞疗法获批上市
昨日(1月2日),国家药品监督管理局通过优先审评审批程序附条件批准铂生卓越生物科技(北京)有限公司申报的艾米迈托赛注射液(商品名:睿铂生)上市,用于治疗14岁以上消化道...
2025-01-03 11:35
 资讯
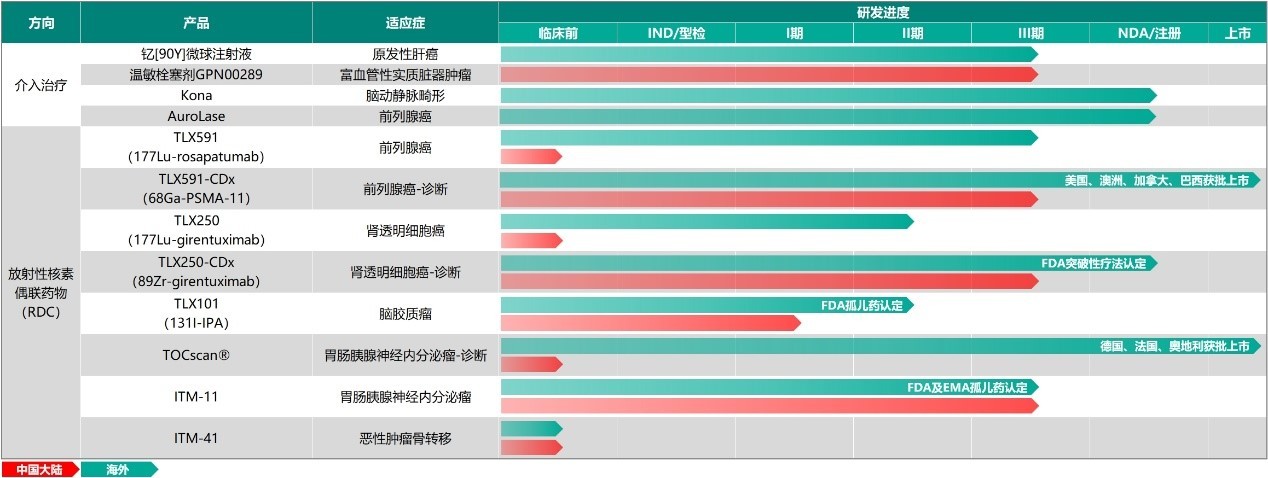
资讯 远大医药创新温敏栓塞剂GPN00289取得临床新进展,已获得药监局创新型医疗器械资质认定
其用于治疗富血管的良性及恶性肿瘤的全球创新温度敏感性栓塞剂产品GPN00289在中国开展的用于原发性肝癌经动脉化疗栓塞的注册性临床研究已于近日完成了首例患者入组。
2025-01-02 17:42
 资讯
资讯 全球首款重组A型肉毒毒素BLA获受理,华东医药医美产品里程碑不断
2025年1月2日,华东医药(000963 SZ)发布公告,独家经销产品注射用重组A型肉毒毒素YY001用于改善中度至重度眉间纹的上市许可申请获国家药品监督管理局受理。
2025-01-02 14:50
 资讯
资讯 首个申报上市的国产司美格鲁肽生物类似药未获批
近日,据国家药监局政务服务门户官网信息显示,九源基因的司美格鲁肽注射液收到 "药品通知件 "。根据国内现行的新药审批流程,如果药物顺利获批,则会收到“药品批准证明文件...
2025-01-02 10:43
 资讯
资讯 个别药企虚开发票制造“两套价格”,悦康药业银杏叶提取物注射液统一下调为11.2元/支
悦康药业主动与事发所在地医疗保障局进行了沟通,申请优化调整银杏叶提取物注射液产品价格,并承诺将该产品全国挂网价格由24 1 元 支、18 14 元 支(部分省份集采中标价格...
2024-12-30 22:22
 资讯
资讯 国家药监局同意广东药检所作为锝标记及正电子类放射性药品检验机构
广东省药品检验所承担广东省行政区域内及中国食品药品检定研究院委派的锝标记及正电子类放射性药品的检验工作,其出具的检验报告可用于企业生产许可及医疗机构备案。
2024-12-28 15:27
 资讯
资讯 安诊儿2.0”发布,支付宝助力浙江打造AI医疗健康服务高地
12月28日,浙江省卫生健康委与支付宝联合打造的数字健康人正式升级为“安诊儿2 0”,让人人拥有陪伴一生的专属“数字医生”。“
2024-12-28 12:01
 资讯
资讯 聚焦肿瘤呼吸病学前沿探索 推动肺癌治疗向“以健康为中心”转变 —— “呼吸与共”专家媒体交流会在广州举行
近日,一场围绕肿瘤呼吸病交叉学科建设、为患者生命加时的媒体工作坊在广州举行。
2024-12-27 19:43
 资讯
资讯 第二款国产伊布替尼片仿制药申报上市
近日,据国家药监局官网信息显示,科伦药业子公司湖南科伦制药的伊布替尼片上市申请获得受理,这也是继齐鲁制药之后,国内第2款申报上市的伊布替尼片剂仿制药。
2024-12-27 15:59
 资讯
资讯 上海微创FireRaptor(火猛禽)冠脉旋磨系统获批上市,填补国产空白
近日,上海微创旋律医疗科技有限公司(以下简称“微创®旋律”)研发生产的FireRaptor®(火猛禽®)旋磨介入治疗仪、一次性使用冠脉旋磨导管和旋磨术用导丝(以下简称“冠脉旋...
2024-12-27 15:34
 资讯
资讯 药明康德卖掉了高端治疗CTDMO海外业务主体
近日,药明康德宣布了一项重大业务调整,公司间接全资子公司WuXi ATU(Ireland)Holding Limited和WuXi ATU(Hong Kong)Limited与Altaris LLC(以下简称“Altaris”)签署了股...
2024-12-26 14:24
 资讯
资讯 国际 SOS 发布《2025 年度全球风险展望》报告
近日,世界领先的健康和安全风险服务企业国际SOS发布《2025年度全球风险展望》报告,自2016年开始,国际SOS就开始发布全球风险展望报告,今年已是第九年,以此助力企业更全面、...
2024-12-26 13:10
 资讯
资讯 阿斯利康王磊被深圳警方逮捕羁押
日前,据澎湃新闻报道,王磊10月30日因涉嫌走私普通货物、物品罪被深圳警方批准逮捕,目前被羁押在当地看守所。同期被带走的还有王磊的几名下属,所涉同样是走私普通货物、物品...
2024-12-25 12:33