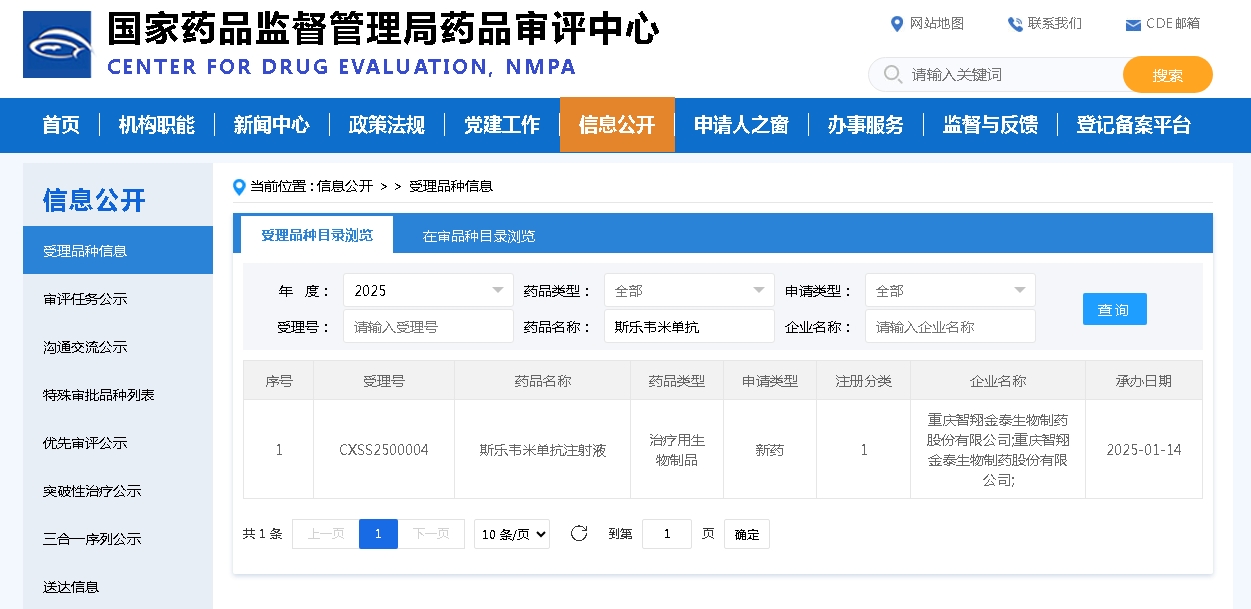
还有不足半个月,新版国家医保目录将开始正式实施,近日,康方生物的PD-1/CTLA-4双抗卡度尼利和PD-1/VEGF双抗依沃西医保支付价格已被披露。
据了解,PD-1/CTLA-4双抗卡度尼利以及PD-1/VEGF双抗依沃西的本次入围医保谈判价格依分别为1860元/支和736元/支。其中,卡度尼利的医保支付价相较于进入医保前6166元/125mg/支的价格,降幅约为69.83%,而依沃西相比于进入目录前2299元/支的挂网价,降幅约为67.98%。
卡度尼利和依沃西作为康方生物的拳头产品,医保目录的进入或将为其带来新的业绩增量。
卡度尼利单抗于2022年6月获得国家药监局附条件批准上市,用于接受含铂化疗治疗失败的复发或转移性宫颈癌患者的治疗,成为获批上市的首款国产双特异性抗体药物,也是全球获批的第一款PD-1/CTLA-4双抗。凭借着先发优势,即使没进医保,卡度尼利单也成功打开了市场,其2023年为康方生物贡献了13.58亿元的收入,相较于2022年增幅达149%。今年上半年,卡度尼利单抗的销售业绩约为7.057亿元,相比去年同期的6.058亿元增长了16.5%。
值得一提的是,今年6月,卡度尼利单抗曾进行过一次主动降价,从13220元瓶降至6166元,降幅为53.4%,该举动彼时也被外界解读为医保谈判做准备,通过降价的方式以减轻医保基金的压力,进入医保就会容易一些,往年度,已有部分药企的产品甚至明星品种进行了类似操作,并最终得偿所愿。
在6月份的降价前,卡度尼利单抗的用药方式为每次用药3瓶,每两周给药。根据康方生物方面的披露,降价前,卡度尼利单抗采用的是“3+2”患者救助方案,即患者自费购买3瓶后,康方生物赠药2瓶,以此为一循环,共循环5次(部分符合特别援助条件的患者,一共循环4次);满足循环购药次数后的一年内,患者继续用药将获得援助,直至疾病出现进展(PD),第二年重新开始计算。按照该定价方案和患者救助方案,卡度尼利单抗年治疗费用不高于19.8万元人民币,但进入医保目录后,按照企业的惯例,会取消赠药援助方案。
目前,在适应症方面,除了已获批的宫颈癌,康方生物还提交了基于卡度尼利单抗联合化疗一线治疗不可手术切除的局部晚期、复发或转移性胃或胃食管结合部(G/GEJ)腺癌的上市申请,并已获得国家药监局受理。
依沃西于今年5月才新近获批,是全球首款获批的融合“肿瘤免疫+抗血管”双重机制的双特异性抗体药物,主要用于非小细胞肺癌的治疗。
在今年获批之后,依沃西凭借头对头击败K药再次“出圈”,5月31日,康方生物发布公告称,依沃西对比帕博利珠单药(俗称K药)一线治疗PD-L1表达阳性(PD-L1TPS≥1%)的局部晚期或转移性非小细胞肺癌(NSCLC)的注册性III期临床试验AK112–303(HARMONi-2),由独立数据监察委员会(IDMC)进行的预先设定的期中分析显示达到无进展生存期(PFS)的主要研究终点。
今年9月康方生物在2024世界肺癌大会上披露的详细数据显示,在ITT人群中,依沃西组和帕博利珠单抗组的mPFS(中位无进展生存期)分别为11.14个月和5.82个月;PFS HR=0.51(P<0.0001),依沃西治疗组疾病进展/死亡风险降低达49%。同时,依沃西相比帕博利珠单抗,显着提高了PD-L1阳性NSCLC患者一线治疗的客观缓解率(50.0%vs 38.5%)和疾病控制率(89.9%vs 70.5%)。由此,依沃西也成为了全球首个在单药头对头III期临床研究中证明疗效显着优于K药的产品。
基于以上积极数据,康方生物的合作伙伴Summit Therapeutics宣布计划开展HARMONi-7研究,用于评估依沃西单药对照帕博利珠单药在一线治疗PD-L1高表达(PD-L1 TPS>50%)转移性NSCLC的全球多中心III期临床试验。
在销售业绩方面,依沃西也同样亮眼,根据康方生物2024年中期业绩报,依沃西上市一个月就为康方生物贡献了1.03亿元的销售业绩。随着本次进入医保目录,依沃西或将迎来更快的市场放量。
来源:医谷网
为你推荐
 资讯
资讯 2024年底,60岁及以上人口3.1亿,占全国人口的22.0%
年末全国人口(包括31个省、自治区、直辖市和现役军人的人口,不包括居住在31个省、自治区、直辖市的港澳台居民和外籍人员)140828万人,比上年末减少139万人。全年出生人口954...
2025-01-17 14:56
 资讯
资讯 赛诺菲荣膺“杰出雇主2025”桂冠,连续五年傲立榜首
作为10多年来首个且唯一连续五年荣获此殊荣的企业,赛诺菲再次彰显了其在企业文化、人才战略、多元发展及员工培养等方面的卓越成就。
2025-01-17 11:02
 资讯
资讯 又一款国产三代EGFR-TKI抑制剂获批上市
昨日(1月16日),据国家药监局官网显示,奥赛康药业的1类创新药利厄替尼片(limertinib ASK120067,商品名:奥壹新)获批上市,用于治疗既往接受表皮生长因子受体酪氨酸激酶抑制...
2025-01-17 10:31
 资讯
资讯 增辉生命,默沙东中国再度荣膺“中国杰出雇主”
1月16日,由全球权威的杰出雇主调研机构(Top Employers Institute)颁布的“杰出雇主2025”榜单正式揭晓
2025-01-16 22:48
 资讯
资讯 国家市场监督管理总局发布《医药企业防范商业贿赂风险合规指引》
本指引所称的商业贿赂, 是指采用财物或者其他手段贿赂交易相对方的工作人员、 受交易相对方委托办理相关事务的单位或者个人、 利用职权或者影响力影响交易的单位或者个人,...
2025-01-14 23:38
 资讯
资讯 阿斯利康与宜联生物达成临床研究合作,共同探索联合治疗创新方案
双方将共同启动一项多中心、开放性、I Ib期研究,旨在评估两款药物联合治疗在实体肿瘤患者中的安全性、有效性和药代动力学。
2025-01-14 18:36
 资讯
资讯 NVIDIA与多家行业顶尖机构达成深度合作,共促医疗健康产业蓬勃发展
在日前举办的摩根大通医疗健康大会上,NVIDIA 宣布与多家行业领先机构达成合作,这类新的合作旨在通过加速药物发现、提升基因组研究,以及利用代理式和生成式 AI 开创先进医...
2025-01-14 13:26
 资讯
资讯 老牌上市药企终止PD-1项目,计提资产减值准备1.75亿元
近日,丽珠医药集团发布公告称,对公司及下属子公司截至2024年12月31日合并报表范围内存在减值迹象的资产进行了减值测试,并对其中存在减值迹象的资产相应计提了减值准备。
2025-01-14 10:13
 资讯
资讯 尊享e生2025升级:首次全场景放开外购药械,医院药品覆盖数量再增
1月13日,众安保险举办“与10光,共生长”尊享e生十周年产品升级发布会,正式发布尊享e生2025版,并推出众安健康险未来将主打的两大产品系列——面向健康人群的“尊享系列”,以...
2025-01-13 20:17
 资讯
资讯 PLA材料的医美应用:安全与效果的双重考验
聚乳酸PLA,作为医美行业面部填充剂历经了3个时代大约20多年的发展,大体可分为1 0、2 0、3 0三个不同的时代;即1 0-结晶片状;2 0-普遍表面粗糙的多孔微球或实心微球;3 ...
2025-01-13 19:53
 资讯
资讯 国家医保局:开展2025年定点医药机构违法违规使用医保基金自查自纠工作,肿瘤类、重症医学类、麻醉类、零售药店典型问题清单
2025年3月底前,各级医保部门根据本地化问题清单,对辖区内所有定点医疗机构和定点零售药店2023-2024年医保基金使用情况开展自查自纠。2025年4月起,国家医保局将对全国定点医药...
2025-01-13 17:32
 资讯
资讯 好大夫正式牵手蚂蚁集团,共同推进“AI+医疗”创新
蚂蚁集团收购好大夫在线尘埃落定。1月11日,在2025年好大夫峰会上,双方在收购完成后首度携手亮相。好大夫在线创始人王航现场表示,共同的使命和愿景让双方走到了一起,后续好大...
2025-01-11 18:05
 资讯
资讯 创新给药机制,全球首个口服GLP-1RA诺和忻(司美格鲁肽片)在中国全面上市
今日(1月11日),全球领先的生物制药公司诺和诺德宣布,全球首个口服胰高糖素样肽-1受体激动剂(GLP-1RA)——诺和忻®(司美格鲁肽片)在中国全面上市。诺和忻®以便利的口服...
2025-01-11 17:56
 资讯
资讯 拜耳诺倍戈(达罗他胺片)第三项适应症注册申请获NMPA受理,实现新适应症全球同步递交
日前,拜耳公司宣布,诺倍戈®(达罗他胺)联合雄激素剥夺疗法(ADT)治疗转移性激素敏感性前列腺癌(mHSPC)成年患者的新适应症申请已获国家药品监督管理局(NMPA)药品审评中...
2025-01-09 16:10