此前,市场上曾一度传出传奇生物被金斯瑞生物科技股出售的消息,但一直并未落定,10月22日早间,金斯瑞生物科技发布公告称,因存托协议变更,决定解除对传奇生物科技的合并,调整为联营公司投资。
具体来讲,根据先前存托协议,倘任何美国存托凭证持有人未及时就特定议程事项提供投票指示,则该持有人被视为已指示存管人将全权委托权交由传奇生物指定的人士,以在相关股东大会上根据该持有人的美国存托凭证所代表的相关普通股份,就该持有人未发出实际指示的该等议程事项进行投票。若(其中包括)传奇生物已指示存管人,其不希望就该议程事项获授全权委托权,则将不会就议程事项授予全权委托权。
根据上述日期生效的协议书,传奇生物以不可撤销方式通知存管人其已决定不再行使全权委托权,尽管存在先前凭证,存管人授予任何全权委托权的能力已被终止。
截止2024年9月30日,金斯瑞生物科技实益拥有1.74亿股传奇生物股份,约占传奇生物已发行股本的47.56%。由于全权委托权的终止,金斯瑞生物失去了在传奇生物股东大会上投票的多数权力,因此决定将传奇生物重新归类为联营公司。
另根据新协议,自2024年10月18日起,传奇生物的资产和负债将不再合并入金斯瑞生物的财务报表。预计解除合并将对金斯瑞生物截至2024年12月31日的合并财务报表会产生重大影响。
传奇生物曾于2020年登陆纳斯达克,其自主研发的BCMA CAR-T疗法Carvykti(西达基奥仑赛)相继在美国、欧盟和日本获批,在中国市场,Carvykti已于今年8月获得国家药监局批准上市,商品名为卡卫荻,用于治疗复发/难治性多发性骨髓瘤,成为第6款在国内获批的CAR-T疗法。
Carvykti自获批后销量持续上涨,2022年销售额为1.34亿美元,2023年迅速飙升至5亿美元,同比增长273%。今年前三季度,Carvykti业绩继续攀升,累计销售收入为6.29亿美元。
在Carvykti商业化快速推进的同时,传奇生物也在不断扩大其适应证范围。今年4月,FDA已批准Carvykti用于治疗既往接受过至少一种治疗(包括一种PI和一种IMiD)且对来那度胺耐药的复发或难治性多发性骨髓瘤成人患者,Carvykti成为首个且唯一获批用于多发性骨髓瘤患者二线治疗的BCMA靶向疗法;当月晚些时候,欧盟委员会批准Carvykti用于治疗复发和难治性多发性骨髓瘤成人患者。
此外,今年4月1日,金斯瑞生物科技股份有限公司发布公告称,传奇生物及杨森制药与诺华达成协议,诺华将承担Carvykti的临床和商业化供应的合同生产服务。
除了Carvykti,传奇生物也在持续布局其他细胞产品,传奇生物官网显示其针对实体瘤(胃癌、胰腺癌、肝癌、小细胞肺癌卵巢癌)、传染病、同种异体CAR-T、CAR-NK产品正在积极研发中。
截至10月21日,传奇生物在纳斯达克的总市值是80.07亿美元,远高于金斯瑞在港股市场不到300亿港元的总市值。业内分析认为,此次变更将有助于传奇生物优化公司治理结构,实现真正的同股同权。
来源:医谷网
为你推荐
 资讯
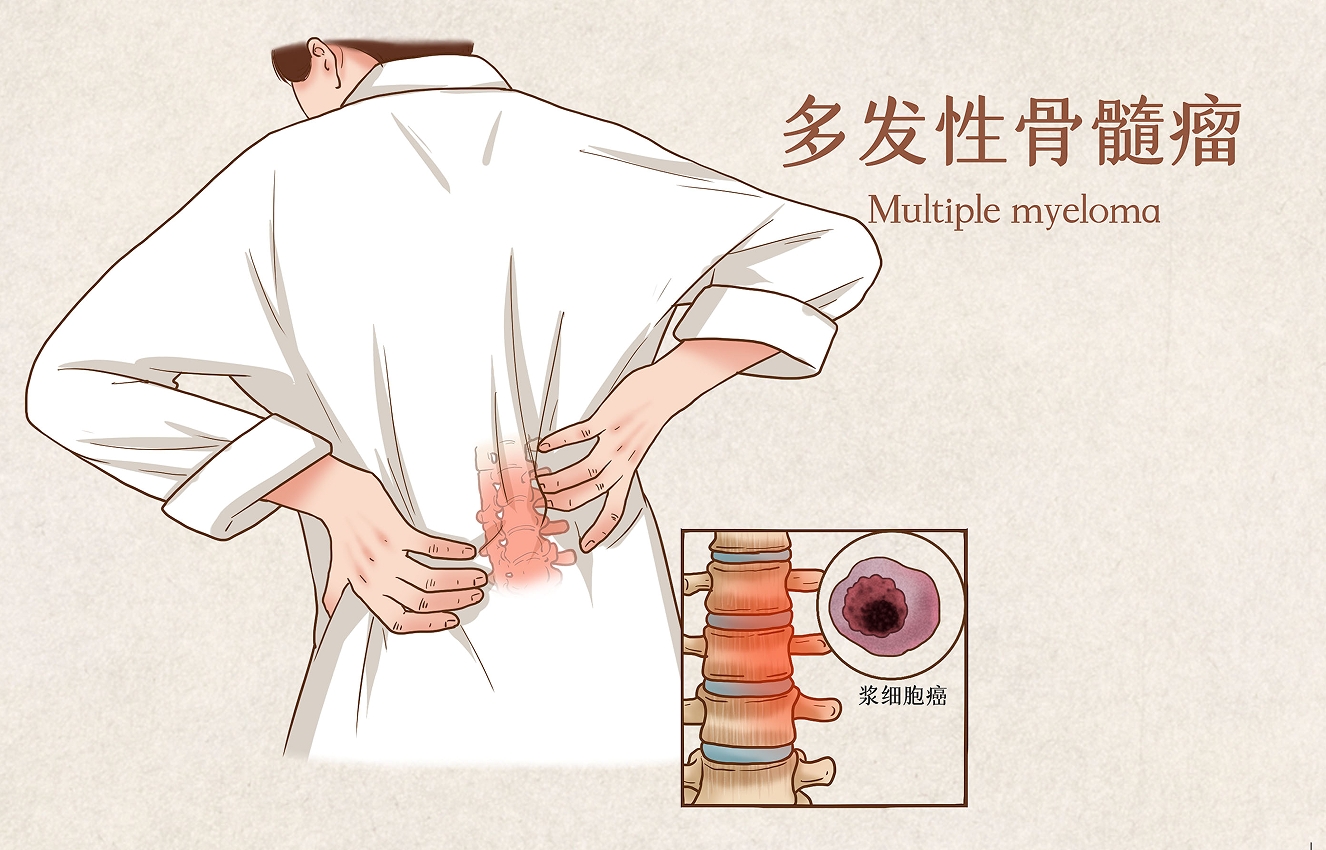
资讯 赛可益获批成为中国首个且目前唯一与标准治疗VRd联合的抗CD38单抗,治疗不适合自体干细胞移植的新诊断的多发性骨髓瘤成人患者
1月24日,赛诺菲抗CD38单抗赛可益®(艾沙妥昔单抗注射液)今日获得国家药品监督管理局(NMPA)批准,用于与硼替佐米、来那度胺和地塞米松(VRd)联合,治疗不适合自体干细胞移...
2025-01-24 22:43
 资讯
资讯 国务院反垄断反不正当竞争委员会:药品领域的反垄断指南
本指南所称中药包括中药材、中药饮片、中药提取物、中药配方颗粒和中成药等;化学药包括化学原料药和化学药制剂;生物制品包括预防用生物制品、治疗用生物制品和按生物制品管理...
2025-01-24 17:30
 资讯
资讯 Ellansé 伊妍仕 M型注册申请获受理,华东医药持续发力高端医美
旗下三类医疗器械注射用聚己内酯微球面部填充剂Ellansé®伊妍仕®M型注册申请获得国家药品监督管理局(NMPA)受理。
2025-01-24 16:26
 资讯
资讯 9岁男孩在红房子医院完成HPV疫苗接种,9-26岁男性都可以打
1月23日,以“和合共生,健康共护”为主题的“HPV男女共防计划”区域媒体圆桌会在复旦大学附属妇产科医院杨浦院区举办
2025-01-24 15:27
 资讯
资讯 复宏汉霖私有化计划失败,将保留H股上市地位
宣布其关于吸收合并及私有化复宏汉霖(02696 HK)的特别决议案未获通过,因此吸收合并计划将不予实施,复宏汉霖将继续保留H股上市地位。
2025-01-23 10:57
 资讯
资讯 国家药监局:关于简化港澳已上市传统口服中成药内地上市注册审批的公告
本公告适用于由香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)...
2025-01-22 17:48
 资讯
资讯 国家医保局21日上海调研交流提纲
国家医保局决定1月21日由国家医保局负责同志带队,联合卫生健康、工业信息化、药品监管部门,赴上海当面听取相关委员、专家关于药品集采政策及中选产品质量保障的意见建议,并重...
2025-01-20 21:41
 资讯
资讯 一款国产肺癌药物2024年大卖超30亿元
日前,艾力斯发布了2024年业绩预告,数据显示,该公司预计2024年度实现营业收入35 5亿元,比上年同期增加15 32亿元,同比增加75 90%;预计实现归属于母公司所有者的净利润为1...
2025-01-20 20:47
 资讯
资讯 华东医药MaiLi Extreme国内获批上市,深耕高端医美领域版图再扩张
据悉,MaiLi系列共有4款产品,包括MaiLi Precise、MaiLi Define、MaiLi Volume 和 MaiLi Extreme,均已在欧洲上市,通过多种配方可适用于面部不同部位,为求美者提供面部美容填充的整体解决方案。
2025-01-20 19:49
 资讯
资讯 华东医药高端玻尿酸、PARP抑制剂于中国上市,创新医疗器械美国获批
2025年1月20日晚,华东医药同时发布三个产品获批上市公告,其在创新及医美领域连续获得多个里程碑进展。
2025-01-20 19:38
 资讯
资讯 早筛与创新疗法并进,共筑前列腺癌防治堡垒
前列腺癌偏爱“高龄+遗传”的双重风险人群,特别是55岁以上的男性、有家族史者及携带特定遗传变异(如BRCA1 2基因突变)的个体。因此,提高公众对前列腺癌的认知,加强早期筛查...
2025-01-20 14:49
 资讯
资讯 国家医保局将赴上海当面听取医生关于集采药效反馈
近日,上海两会期间,来自上海多家三甲医院的 20 名政协委员联名提案《关于在药品集采背景下如何能够用到疗效好的药物的提案》,其中提到集采药药效不稳定的情况。其中,该提...
2025-01-20 13:50
 资讯
资讯 中粮集团领航央地合作,2025年大兴区CGT项目路演专场活动成功举办
历时17个月的精心筹备与建设,国内首个细胞与基因治疗特色产业园——中关村(大兴)细胞基因治疗产业园,于北京中关村科技园区大兴生物医药产业基地落成,并于1月17日举办2025年...
2025-01-20 12:25
 资讯
资讯 “和合共生,健康共护”四价HPV疫苗男性适应证上市暨“HPV男女共防计划”启动新闻发布会成功举办,共筑HPV预防新生态
今日(1月18日),默沙东(默沙东是美国新泽西州罗威市默克公司的公司商号)举办的“和合共生,健康共护”四价HPV(人乳头瘤病毒)疫苗男性适应证上市暨“HPV男女共防计划”启动...
2025-01-18 18:31
 资讯
资讯 四同药品价格治理已基本实现,正建设全国挂网药品价格一览表
目前,我们正在建设全国挂网药品价格一览表,全量汇总展示各地挂网价格信息并对首涨、高涨幅等异常价格行为予以标识,敦促各地持续纠正不合理的挂网高价。
2025-01-18 12:15
 资讯
资讯 2025年全国80%左右医保统筹地区基本实现即时结算,2026年底全部实现即时结算
1月16日,国家医疗保障局办公室正式对外发布《关于推进基本医保基金即时结算改革的通知》。根据通知,以全国统一的医保信息平台为支撑,2025年全国80%左右统筹地区基本实现即时...
2025-01-18 11:20
 资讯
资讯 2024年底,60岁及以上人口3.1亿,占全国人口的22.0%
年末全国人口(包括31个省、自治区、直辖市和现役军人的人口,不包括居住在31个省、自治区、直辖市的港澳台居民和外籍人员)140828万人,比上年末减少139万人。全年出生人口954...
2025-01-17 14:56





