近日,君合盟生物制药(杭州)有限公司宣布,已成功突破重组人胶原蛋白的规模化发酵与纯化技术,实现二十吨发酵体系下的稳定表达,顺利完成相关产品工业化生产工艺的开发。该技术突破,不仅标志着行业由动物源胶原向重组人胶原替代转型的过程中迈出了重要一步,更预示着产业正加速迈入使用重组人胶原蛋白材料的新时代。
攻克关键技术壁垒,实现重组人胶原蛋白规模化生产
重组胶原蛋白采用合成生物学技术开发,分为重组人胶原蛋白、重组人源化胶原蛋白和重组类胶原蛋白三种类型。重组人胶原蛋白是由DNA重组技术制备的人胶原蛋白特定型别基因编码的全长氨基酸序列,且有三螺旋结构。受技术水平限制,目前已上市的产品多为重组人源化胶原蛋白,重组人源化胶原蛋白是由DNA重组技术制备的人胶原蛋白特定型别基因编码的全长或部分氨基酸序列片段,或是含人胶原蛋白功能片段的组合。国内外目前均无与天然人胶原蛋白结构组成、序列长度及生物学功能相一致的重组人胶原蛋白产品获批上市。
“重组人胶原蛋白在结构和功能上更接近天然人胶原蛋白,因此技术难度更高,但其生物学作用也更优。”君合盟CMC研发总监沈玉保博士表示,重组人胶原蛋白因其特有的三螺旋结构,而具备完整的生物学功能,不仅确保了胶原蛋白的稳定性,还具有显著的支撑作用,对于改善皮肤质地、促进组织修复等方面具有重要意义。此外,重组人胶原蛋白作为细胞支架,具有诱导自身胶原蛋白产生的能力。这意味着,在植入人体后,它不仅能够直接补充缺失的胶原蛋白,还能诱导机体自身合成新的胶原蛋白,从而形成一个良性循环,持续改善皮肤生态和组织功能。
据悉,君合盟采用细胞工厂制备,模拟天然人I/III型人胶原蛋白的体内产生过程,利用酵母成功表达,实现产品制备,解决了动物源胶原蛋白的免疫原性问题,及重组人源化胶原蛋白的功能性片段不能行使三螺旋的全部生物学功能的问题,同时也突破了制备技术及制备规模的产业化瓶颈,是国内少数拥有从发酵生产、分离纯化到产品制备全流程的核心技术及自主知识产权,并具备重组人胶原蛋白规模化放大能力的企业,其产品开发进度与产业化实力均位居行业前列。
目前,君合盟在研两种类型的胶原蛋白,分别为重组I型人胶原蛋白及重组III型人胶原蛋白。多项结构表征数据显示,这两种胶原蛋白与天然I/III型人胶原蛋白结构高度一致,同时实现了全长氨基酸序列与三螺旋结构,生物学活性完整,稳定性强。其中,重组III型人胶原蛋白,已申报II类医疗器械,III类医疗器械的临床前研究正在进行中。
“重组人胶原蛋白的半衰期一般为3-6个月,如需延长,需进行交联或化学修饰。III型胶原蛋白丝细且相对柔软,而I型胶原蛋白相较粗大和坚韧,有较强的支撑作用。这两类胶原蛋白各具特性,复合使用可实现作用互补,不仅适用于消费医疗领域,如皮肤填充、祛皱护肤等细分场景,还将在严肃医疗领域如再生医学的人工血管、支架材料等方面发挥重要作用。此外,我们正积极开发具有天然人体组织结构与功能的新型仿生材料和自适应性新型组织材料,全力拓宽相关产品的应用领域与市场潜力。”君合盟特邀顾问、高级工程师顾其胜教授介绍说。
夯实产品开发和产业化能力,全面布局消费医疗和严肃医疗领域
除重组人胶原蛋白外,君合盟正同步推进重组A型肉毒毒素与重组人生长激素的临床研究,全面覆盖消费医疗及严肃医疗领域。其中,重组A型肉毒毒素已于今年四月完成成人中重度眉间纹I期临床试验,目前已完成临床II期试验入组,是全球第二家进入临床阶段的重组 A 型肉毒毒素。
“重组A型肉毒毒素按照药品审批流程管理,临床试验流程无特别要求,但需与药监局沟通临床试验设计、疗效指标、安全性指标及样本量等。”君合盟临床医学总监林丹花强调,公司会及时将I、II、III期产生的临床数据提交给药监局进行审评。
中国肉毒毒素行业市场准入门槛较高,目前的正规供应有限且市场渗透率较低。而A型肉毒毒素的高级结构极为复杂,其研发面临诸多挑战,包括重组表达的高难度和对纯化技术的严苛要求。君合盟重组A型肉毒毒素产品不仅克服了上述难点,而且产品活性符合国际最高质量标准(欧洲)要求,是国际公认的新一代肉毒毒素。
“通过深入研究肉毒毒素A的空间结构与理化特性,我们成功开发出一套高效且简洁的生产工艺,大幅缩短了纯化流程及纯化时间。传统的生物制品开发过程,通常从3-5升的发酵规模开始小试,并逐步放大至中试及商业化制备水平,而我们5升的发酵规模已足以满足重组A型肉毒毒素的商业化生产需求。”沈玉保博士说道。
君合盟生物制药董事长徐葵进一步补充说明,凭借这一先进工艺,君合盟的重组A型肉毒毒素能够在5升的发酵规模下,单批次原液可产出高达3000万到4000万支的制剂,这一产能规模可以满足当前的全球市场需求,展示了公司在技术上的领先地位和规模化生产的强大能力。
君合盟的重组人生长激素注射液已于近期完成临床III期入组。同时,一类创新药重组长效生长激素正在开展临床前药理毒理研究,临床前动物试验结果显示,具有每两周给药一次的治疗潜力。
“目前,生长激素的适应症范围还在不断扩大,海外市场生长激素产品已获批多种适应症,显示了该领域巨大的市场潜力和发展空间。中国儿童生长激素缺乏症(PGHD)患者群体对生长激素治疗的需求显著,但当前患者仍面临两大核心挑战。一是用药频率高,通常需要每天注射一次,给患者及家庭带来不便;二是患者费用负担重,限制了治疗药物的渗透率和治疗率。我们的目标是研发出更高品质、更低费用的生长激素,以降低患者的用药负担,提高治疗依从性。”董事长徐葵说道。
自2020年11月成立以来,君合盟一直专注于合成生物学领域技术及产品的开发。徐葵认为,合成生物学作为当代生物科技的前沿阵地,无疑具备极高的技术门槛与市场潜力。然而,国内合成生物学企业虽数量众多,且不乏佼佼者,但整个行业仍面临两大核心挑战:一是起步时间相对较晚,与国际领先企业存在技术积累上的差距;二是产业化进程滞后,即便前期研发成果斐然,但成功推向市场的产品仍显不足,这严重制约了行业的整体发展步伐。“合成生物企业要想取得成功,需具备三要素,即研发能力、产品选择与产业化能力。”
通过构建国内外领先的重组蛋白表达和分离纯化平台,君合盟不仅致力于研发管线的稳步推进,更在同步开启产业化与商业化的全面进程。从产品设计、工厂建设的源头抓起,直至产品研发、产业化实现及市场布局的全链条覆盖,君合盟构建了一个闭环式的发展模式,确保了技术创新与市场需求的紧密对接。尤为值得一提的是,君合盟团队拥有超过二十年的开发经验,这不仅为公司的持续创新提供了坚实支撑,更在产业化实践中发挥了关键作用。
“君合盟在研管线推进顺利,产品开发进度明确,目标于未来三年内完成多项产品的临床研究和上市申报。伴随医美行业的蓬勃发展和有序扩张,以及严肃医疗领域的深入研究和广泛应用,公司正不断加强自主创新能力,力争在合成生物学领域取得更多突破,实现长足发展。”徐葵表示。
为你推荐
 资讯
资讯 圣因生物完成超 1.1 亿美元 B 轮融资,加速 RNAi 疗法全球布局
本轮融资由知名产业机构领投,国际主权基金、中国生物制药、君联资本等十余家机构跟投,全球制药巨头礼来公司战略入局,高瓴创投、启明创投等现有股东持续加码支持,融资规模创...
2025-12-12 16:59
 资讯
资讯 投后估值达21.37亿元,实体瘤细胞治疗领军企业君赛生物递表港交所
君赛生物共有5款在研产品,其中核心产品也是进展最快的是GC101,正开展上市前的关键II期临床试验,有望成为国内首个获批上市的TIL细胞创新药
2025-12-12 09:24
 资讯
资讯 ESMO-IO | ORR达41.7%!君赛生物GC101 TIL治疗晚期后线非小细胞肺癌I期数据首次公布
这不仅是全球首个无需高强度清淋化疗、无需IL-2给药的TIL疗法治疗肺癌的临床研究,也是国内首个公开披露该领域数据的注册性临床研究。
2025-12-12 09:17
 资讯
资讯 君合盟生物启动重组 A 型肉毒毒素治疗成人上肢痉挛状态临床 III 期试验,并完成首例患者入组
该临床试验由复旦大学附属华山医院李放教授和上海市养志康复医院(即上海市阳光康复中心)靳令经教授联合牵头
2025-12-11 21:06
 资讯
资讯 Medidata发布全新调研报告:临床试验AI应用价值凸显,超七成用户反馈“达到或超预期”
基于对来自全球制药公司、生物科技公司及合同研究组织(CRO)中超200位核心决策者的深度调研,报告显示,目前AI在改善患者招募、优化数据管理、控制运营成本和提升试验效率等方...
2025-12-11 20:57
 资讯
资讯 近20年首个全新类别抗菌药物醋酸来法莫林纳入医保,开启中国成人社区获得性肺炎治疗普惠新篇章
该产品继2025年6月30日获得国家药品监督管理局批准用于治疗成人社区获得性肺炎(CAP)后又纳入国家医保目录
2025-12-11 20:50
 资讯
资讯 专注 “生物学 + AI” ,普瑞基准完成超亿元 D 轮融资,加速 AI 驱动新药研发
本轮融资由信立泰、广投资本、申宏中恒基金联合领投,老股东金谷汇枫、聚翊投资持续跟投
2025-12-10 15:55
 资讯
资讯 别把“嗜睡”当懒癌!新型促觉醒药翼朗清®获批,专注维持日间清醒
促觉醒药物翼朗清®(盐酸索安非托片)正式获得中国国家药品监督管理局(NMPA)批准,用于改善阻塞性睡眠呼吸暂停(OSA)伴有日间过度嗜睡(EDS)的成人患者的觉醒程度。
2025-12-10 11:04
 资讯
资讯 复星医药将其GLP-1产品全球化权益授权辉瑞,总里程碑付款近150亿人民币
12月9日晚间,复星医药发布公告称,公司控股子公司药友制药、复星医药产业与辉瑞共同签订《许可协议》,(其中主要包括)由药友制药就口服小分子胰高血糖素样肽-1受体(GLP-1R)...
2025-12-10 09:12
 资讯
资讯 Capricor Therapeutics公司宣布外泌体疗法Deramiocel在DMD三期中取得积极成果
近日,专注与外泌体疗法的Capricor Therapeutics(纳斯达克代码:CAPR)公司宣布其核心管线Deramiocel在杜氏肌营养不良症关键三期 HOPE-3 研究中取得积极成果。
2025-12-09 16:38
 资讯
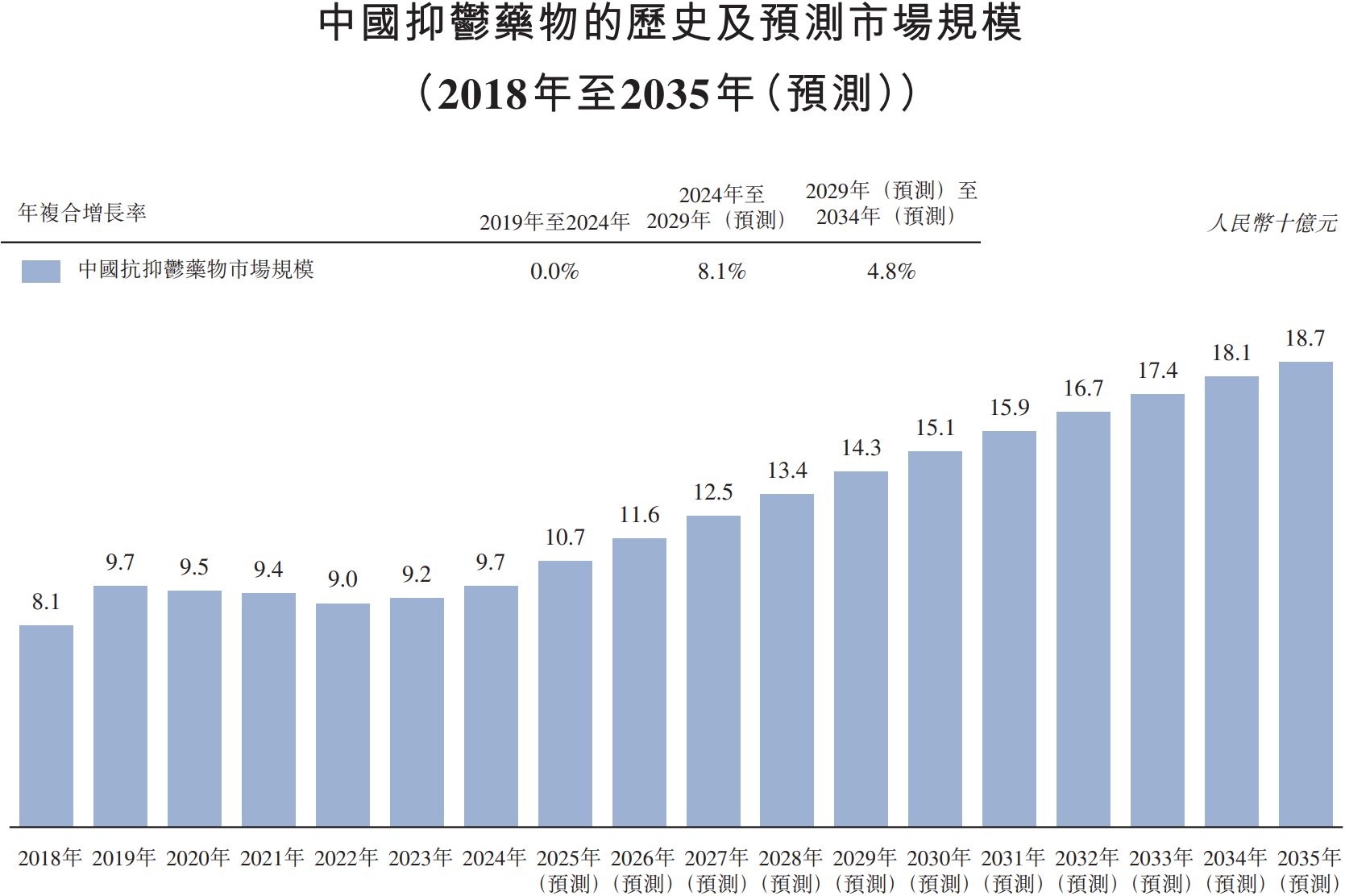
资讯 中药1类创新药剑指抑郁症治疗蓝海,远大医药GPN01360成功达到国内II期临床终点
国产抗抑郁症药物研发取得重大进展。近日,远大医药(0512 HK)的1 1类中药创新药GPN01360国内II期临床研究成功达到临床终点,产品表现出显
2025-12-08 18:27