近日,海森生物和LIB Therapeutics Inc.联合宣布就海森生物在大中华区(包括中国大陆和港澳台地区)开发及商业化第三代长效PCSK9抑制剂Lerodalcibep达成许可协议。
22亿引进长效PCSK9抑制剂
资料显示,血脂异常,尤其是低密度脂蛋白胆固醇(LDL-C)水平升高是动脉粥样硬化性心血管疾病(ASCVD)的致病性危险因素。虽然现有的以他汀类药物为基础的降脂治疗可显著降低LDL-C水平及ASCVD风险,但ASCVD高风险人群的LDL-C降脂达标率现状仍然堪忧。PCSK9被公认为是继他汀类药物之后最具安全有效潜力的降脂靶点,PCSK9抑制剂可选择性的与PCSK9结合,阻止血液中的PCSK与肝细胞表面LDLR结合,从而阻止PCSK9介导的LDLR降解,可显着降低心血管疾病患者LDL-C水平。
Lerodalcibep是由LIB开发的长效PCSK9抑制剂,与传统PCSK9抑制剂单克隆抗体相比,Lerodalcibep每月仅需注射一针,且注射体积更少(1.2ml),可帮助减少注射部位不良反应和免疫原性。在2023年欧洲心脏病学会(ESC)年会上,LIB公布了Lerodalcibep的LIBerate-HeFH全球3期试验的积极结果。该试验共纳入478例杂合子家族性高胆固醇血症患者,校正安慰剂效应后,每月一针皮下注射Lerodalcibep的治疗组患者在第24周时LDL-C平均下降58.6%,在第22周/24周平均下降65.0%。同时,68%Lerodalcibep组患者LDL-C相比基线至少降低50%且达到2019年欧洲心脏病学会推荐的ASCVD或ASCVD高危人群LDL-C目标,而安慰剂组仅有1.9%达标。此外,研究显示Lerodalcibep具有良好的耐受性和安全性,治疗中出现的不良事件与安慰剂组相似。
LIB计划于2024年第一季度向美国食品药品监督管理局(FDA)提交上市申请,于2024年第二季度向欧洲药物管理局(EMA)提交上市申请。
此次海森生物与LIB Therapeutics达成合作,根据协议条款,海森生物获得Lerodalcibep在大中华区开发和商业化的独家专有权。LIB将获得2000万美元的预付款,并有可能额外获得最高达3.05亿美元(约合人民币22亿元)的临床、注册和销售里程碑付款。LIB也将根据Lerodalcibep在大中华区的年净销售额获得特许权使用费。海森生物计划在今年年底向国家药品监督管理局递交Lerodalcibep临床试验申请。
PCSK9靶点药物竞争激烈
目前全球共有4款PCSK9靶点药物获批上市,包括三款单抗药物——安进/安斯泰来的Repatha(依洛尤单抗,商品名:瑞百安)、赛诺菲/再生元的Praluent(阿利西尤单抗,商品名:波立达)、信达的托莱西单抗(商品名:信必乐),以及一款小分子干扰核糖核酸(siRNA)药物——诺华的Leqviq(英克司兰钠,商品名:乐可为)。目前4款药物已全部在国内获批上市,其中托莱西单抗为今年8月获批上市,也是国内首个获批的本土自主研发PCSK9抑制剂。
2022年,3款进口药物的全球销售额分别为12.96亿美元、4.04亿美元、1.12亿美元。价格方面,据悉,Leqviq价格较高,每针大约需要2万元左右,全年大约花费4万元;依洛尤单抗和阿利西尤单抗已纳入医保,价格每针300元左右,每月两针,全年大约花费7200元。此外,国产PCSK9抗体中,今年4月,君实生物的重组人源化抗PCSK9单克隆抗体注射液JS002和康方生物的伊努西单抗均在申报上市阶段。此外,信立泰、和铂医药、前沿生物、天士力、甘宝利等的PCSK9项目也正处于研究中。
来源:医谷网
为你推荐
 资讯
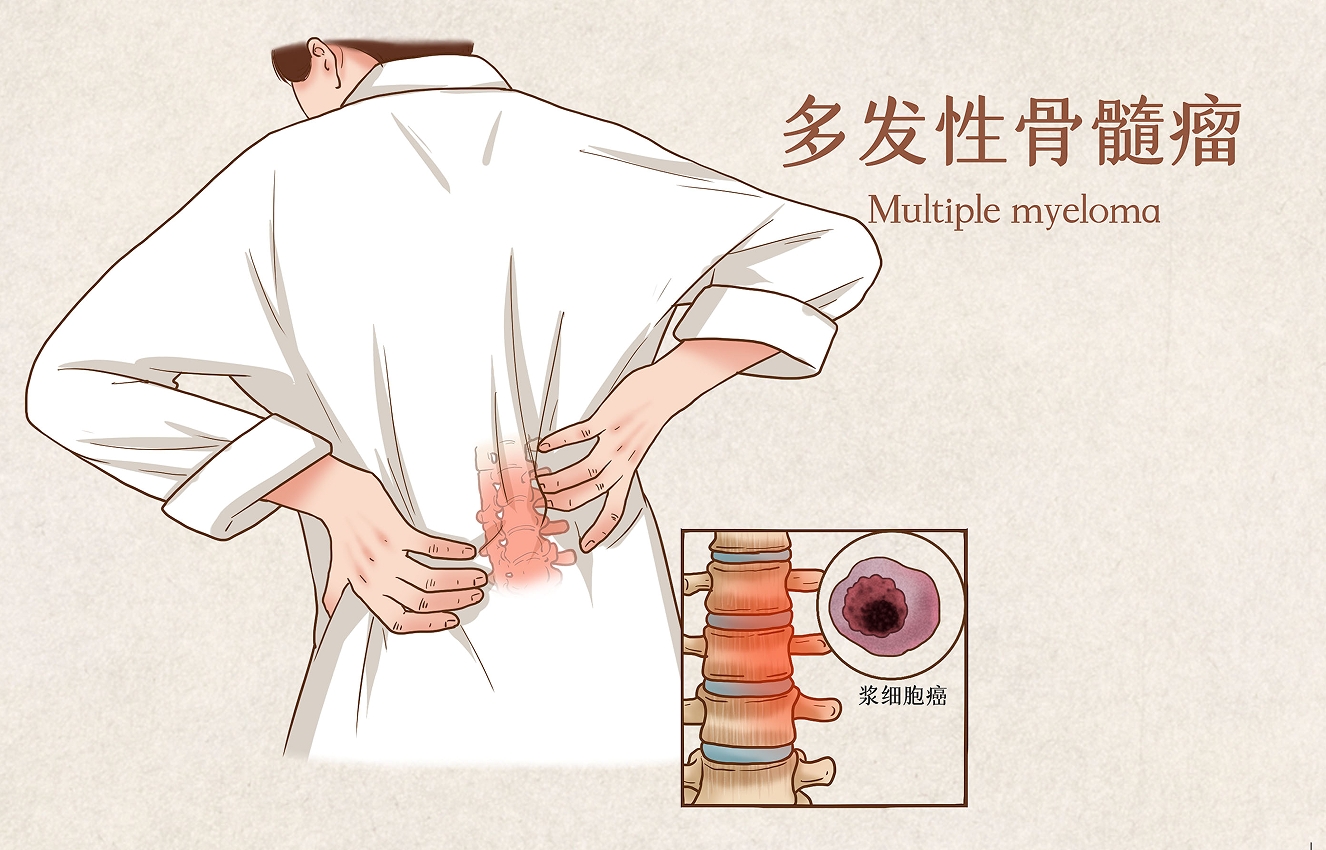
资讯 赛可益获批成为中国首个且目前唯一与标准治疗VRd联合的抗CD38单抗,治疗不适合自体干细胞移植的新诊断的多发性骨髓瘤成人患者
1月24日,赛诺菲抗CD38单抗赛可益®(艾沙妥昔单抗注射液)今日获得国家药品监督管理局(NMPA)批准,用于与硼替佐米、来那度胺和地塞米松(VRd)联合,治疗不适合自体干细胞移...
2025-01-24 22:43
 资讯
资讯 国务院反垄断反不正当竞争委员会:药品领域的反垄断指南
本指南所称中药包括中药材、中药饮片、中药提取物、中药配方颗粒和中成药等;化学药包括化学原料药和化学药制剂;生物制品包括预防用生物制品、治疗用生物制品和按生物制品管理...
2025-01-24 17:30
 资讯
资讯 Ellansé 伊妍仕 M型注册申请获受理,华东医药持续发力高端医美
旗下三类医疗器械注射用聚己内酯微球面部填充剂Ellansé®伊妍仕®M型注册申请获得国家药品监督管理局(NMPA)受理。
2025-01-24 16:26
 资讯
资讯 9岁男孩在红房子医院完成HPV疫苗接种,9-26岁男性都可以打
1月23日,以“和合共生,健康共护”为主题的“HPV男女共防计划”区域媒体圆桌会在复旦大学附属妇产科医院杨浦院区举办
2025-01-24 15:27
 资讯
资讯 复宏汉霖私有化计划失败,将保留H股上市地位
宣布其关于吸收合并及私有化复宏汉霖(02696 HK)的特别决议案未获通过,因此吸收合并计划将不予实施,复宏汉霖将继续保留H股上市地位。
2025-01-23 10:57
 资讯
资讯 国家药监局:关于简化港澳已上市传统口服中成药内地上市注册审批的公告
本公告适用于由香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)...
2025-01-22 17:48
 资讯
资讯 国家医保局21日上海调研交流提纲
国家医保局决定1月21日由国家医保局负责同志带队,联合卫生健康、工业信息化、药品监管部门,赴上海当面听取相关委员、专家关于药品集采政策及中选产品质量保障的意见建议,并重...
2025-01-20 21:41
 资讯
资讯 一款国产肺癌药物2024年大卖超30亿元
日前,艾力斯发布了2024年业绩预告,数据显示,该公司预计2024年度实现营业收入35 5亿元,比上年同期增加15 32亿元,同比增加75 90%;预计实现归属于母公司所有者的净利润为1...
2025-01-20 20:47
 资讯
资讯 华东医药MaiLi Extreme国内获批上市,深耕高端医美领域版图再扩张
据悉,MaiLi系列共有4款产品,包括MaiLi Precise、MaiLi Define、MaiLi Volume 和 MaiLi Extreme,均已在欧洲上市,通过多种配方可适用于面部不同部位,为求美者提供面部美容填充的整体解决方案。
2025-01-20 19:49
 资讯
资讯 华东医药高端玻尿酸、PARP抑制剂于中国上市,创新医疗器械美国获批
2025年1月20日晚,华东医药同时发布三个产品获批上市公告,其在创新及医美领域连续获得多个里程碑进展。
2025-01-20 19:38
 资讯
资讯 早筛与创新疗法并进,共筑前列腺癌防治堡垒
前列腺癌偏爱“高龄+遗传”的双重风险人群,特别是55岁以上的男性、有家族史者及携带特定遗传变异(如BRCA1 2基因突变)的个体。因此,提高公众对前列腺癌的认知,加强早期筛查...
2025-01-20 14:49
 资讯
资讯 国家医保局将赴上海当面听取医生关于集采药效反馈
近日,上海两会期间,来自上海多家三甲医院的 20 名政协委员联名提案《关于在药品集采背景下如何能够用到疗效好的药物的提案》,其中提到集采药药效不稳定的情况。其中,该提...
2025-01-20 13:50
 资讯
资讯 中粮集团领航央地合作,2025年大兴区CGT项目路演专场活动成功举办
历时17个月的精心筹备与建设,国内首个细胞与基因治疗特色产业园——中关村(大兴)细胞基因治疗产业园,于北京中关村科技园区大兴生物医药产业基地落成,并于1月17日举办2025年...
2025-01-20 12:25
 资讯
资讯 “和合共生,健康共护”四价HPV疫苗男性适应证上市暨“HPV男女共防计划”启动新闻发布会成功举办,共筑HPV预防新生态
今日(1月18日),默沙东(默沙东是美国新泽西州罗威市默克公司的公司商号)举办的“和合共生,健康共护”四价HPV(人乳头瘤病毒)疫苗男性适应证上市暨“HPV男女共防计划”启动...
2025-01-18 18:31
 资讯
资讯 四同药品价格治理已基本实现,正建设全国挂网药品价格一览表
目前,我们正在建设全国挂网药品价格一览表,全量汇总展示各地挂网价格信息并对首涨、高涨幅等异常价格行为予以标识,敦促各地持续纠正不合理的挂网高价。
2025-01-18 12:15
 资讯
资讯 2025年全国80%左右医保统筹地区基本实现即时结算,2026年底全部实现即时结算
1月16日,国家医疗保障局办公室正式对外发布《关于推进基本医保基金即时结算改革的通知》。根据通知,以全国统一的医保信息平台为支撑,2025年全国80%左右统筹地区基本实现即时...
2025-01-18 11:20
 资讯
资讯 2024年底,60岁及以上人口3.1亿,占全国人口的22.0%
年末全国人口(包括31个省、自治区、直辖市和现役军人的人口,不包括居住在31个省、自治区、直辖市的港澳台居民和外籍人员)140828万人,比上年末减少139万人。全年出生人口954...
2025-01-17 14:56




