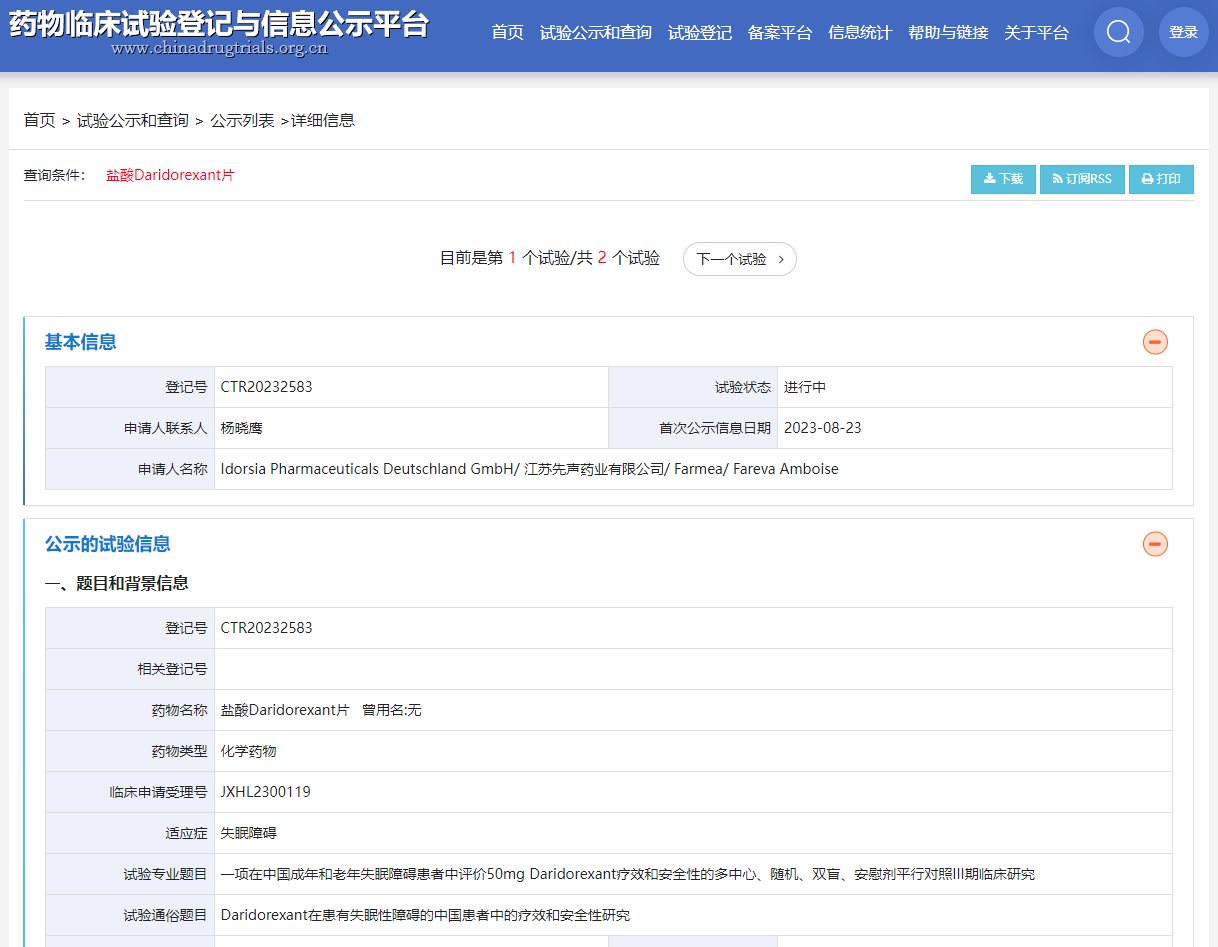
日前,据药物临床试验登记与信息公示平台显示,先声药业与Idorsia公司与等在中国共同启动一项针对抗失眠药物盐酸Daridorexant片的临床研究,临床试验信息显示,这是一项在中国成年和老年失眠障碍患者中评价50mg Daridorexant疗效和安全性的多中心、随机、双盲、安慰剂平行对照III期临床研究,以评估Daridorexant在患有失眠性障碍的中国患者中的疗效和安全性。
该试验计划入组200人,临床试验的主要终点指标为第1个月末(访视7时2晚)经多导睡眠监测(PSG)测定的客观入睡后清醒时间(WASO,2晚的平均值)较基线(访视4时2晚的平均值)的变化,次要终点指标为第1个月最后7天(访视7前7天)经睡眠日记评估的主观总睡眠时间(sTST,7天的平均值)较基线(访视4前7天的平均值)的变化,以及第1个月末(访视7时2晚)经PSG测定的客观睡眠潜伏期(LPS,2晚的平均值)较基线(访视4时2晚的平均值)的变化,临床试验将在首都医科大学宣武医院、河北医科大学第一医院等33家医院开展。
据了解,失眠是目前带来广泛困扰的一项疾病,临床症状主要表现为入睡困难(入睡潜伏期超过30分钟)、睡眠维持障碍(整夜觉醒次数≥2次)、早睡、睡眠质量下降和总睡眠时间减少(通常小于6.5小时),同时伴有日间功能障碍。一项对于中国普通人群失眠患病率的荟萃分析显示,中国失眠患病率约为15%,这也意味着有上亿人饱受失眠困扰。
根据先声药业此前的官方新闻稿介绍,Daridorexant为一种双食欲素受体拮抗剂,与传统失眠药物(如苯二氮䓬类药物)通过镇静大脑来促进睡眠的疗法不同,Daridorexant通过阻断食欲素受体的激活,从而降低觉醒驱动,促使睡眠发生,并且不改变患者的睡眠结构,未观察到次日残余效应。
此前,Daridorexant已发表于《柳叶刀神经病学》的海外III期临床数据显示,在接受1个月、3个月治疗后,Daridorexant较安慰剂显著改善了患者入睡、睡眠维持及自我报告的总睡眠时间。具体而言,接受Daridorexant 50mg治疗的受试者,治疗的第三个月,持续睡眠潜伏期(LPS)显著下降34.8分钟,入睡后清醒时间(WASO)显著下降29.4分钟,自我报告的总睡眠时间(sTST)显著增加57.7分钟。此外,研究表明Daridorexant除可改善慢性失眠障碍成年人群的夜间睡眠外,还可改善患者的日间功能。
2022年1月,Daridorexant已获得美国FDA批准上市,商品名为Quviviq,用于治疗失眠症成人患者。同年11月,先声药业与Idorsia订立独家授权协议,获授Daridorexant在大中华地区的开发及商业化的独家权利。目前,Daridorexant已在美国、英国、意大利、德国、瑞士、加拿大获批上市。国内尚无此类双重食欲素受体拮抗剂(DORA)类失眠药上市。
来源:医谷网
为你推荐
 资讯
资讯 CDE:可复制型慢病毒检测共性问题与技术要求
药审中心对细胞和基因治疗产品中可复制型慢病毒检测共性问题进行整理,组织制定了《可复制型慢病毒检测共性问题与技术要求》,内容旨在针对这类慢病毒载体系统的 RCL 检测问题...
2024-10-29 22:32
 资讯
资讯 药品耗材挂网“一省核验、全国通享”启动,2025年1月1日起全国各省全部正式上线
10月29日,山东省医保局发布《关于开展医药产品挂网全国联审通办试运行工作的通知》,药品耗材信息一次提交,一省核验、全国通享正式进入试点执行阶段。
2024-10-29 21:58
 资讯
资讯 罗氏七赴进博,深耕中国三十周年,聚力共筑健康未来
罗氏将以“华彩三十,聚氏未来”为主题,于1000平方米的进博展台上全面展示超过30款已上市和即将在华上市的全产品矩阵及创新解决方案,重磅推出3款即将在华获批的全球创新产品。
2024-10-29 14:50
 资讯
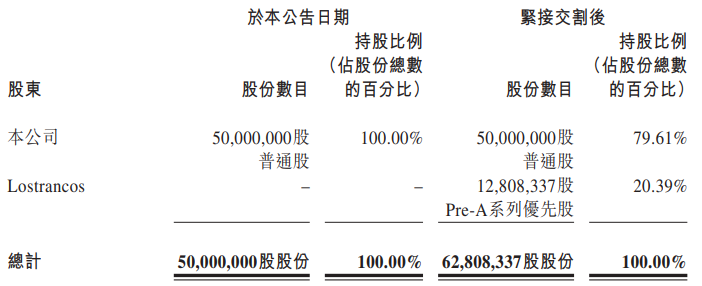
资讯 信达生物转让子公司约20%股权
近日,信达生物发布通告称,全资子公司Fortvita与Lostrancos签订了认购协议,Lostrancos有条件同意按认购价认购及购买,而Fortvita有条件同
2024-10-29 14:37
 资讯
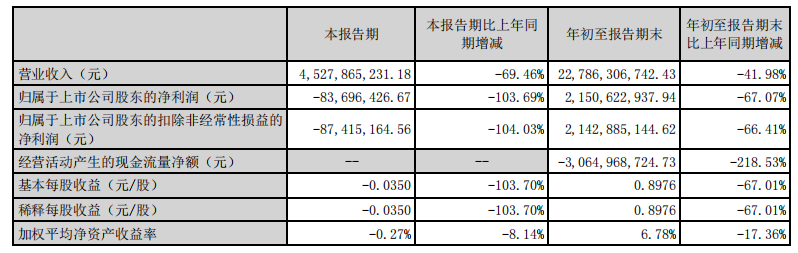
资讯 HPV疫苗卖不动了?智飞生物三季报净利润腰斩
近日,智飞生物发布2024年三季度报告。财报显示,今年前三季度,公司实现营业收入为227 86亿元,同比减少41 98%;归属于上市公司股东的净利
2024-10-29 14:02
 资讯
资讯 2024爱尔眼科眼底病论坛(湖南站)盛大召开
由爱尔眼科长沙医学中心、爱尔眼科湖南省区眼底病学组、湖南爱眼公益基金会主办,长沙爱尔眼科医院、长沙湘江爱尔眼科医院承办的“2024爱尔眼科眼底病论坛(湖南站)暨疑难眼底...
2024-10-27 11:37
 资讯
资讯 特应性皮炎患者人手必备的“百科全书”,《特应性皮炎365问》正式启动
近日,2024樱花皮肤健康学术周在线上顺利召开,会议期间,作为由中华医学会皮肤性病学分会发起的皮肤健康三年行动(2024-2026)的重要组成部分,365科普书系列《特应性皮炎365...
2024-10-27 11:29
 资讯
资讯 2024青岛呼吸产业大会暨第二十三届呼吸周圆满举办,多领域、多维度共同守护亿万国民呼吸健康
本届大会由青岛市人民政府主办,青岛市科学技术局、青岛市工业和信息化局、青岛国家高新技术产业开发区管理委员会、医师报与阿斯利康联合承办。
2024-10-26 10:03
 资讯
资讯 肾癌质控首批试点中心建设启动,持续推动肿瘤治疗公平性
2024年10月25日,由国家癌症中心国家肿瘤质控中心肾癌质控专家委员会指导、北京中康联公益基金会主办、北京大学第一医院承办的“国家癌症中心肾癌质控专家委员会第一批试点中心...
2024-10-25 20:50
 资讯
资讯 2024 Veeva中国商务峰会成功举办,推动生命科学领域数字化营销新变革
10月24日,在全球数字化转型浪潮与医药行业深刻变革的交汇点,全球生命科学行业云软件领导者Veeva Systems成功举办“2024 Veeva中国商务峰会”。本次峰会以“一起领新V来”为...
2024-10-25 17:19
 资讯
资讯 安斯泰来VYLOY获美国FDA批准用于治疗晚期胃和胃食管交界处腺癌
近日,安斯泰来宣布,美国食品和药品监督管理局(FDA)已批准VYLOY®(zolbetuximab-clzb)与含氟尿嘧啶和铂类化疗药物联合用于一线治疗患有局部晚期不可切除或转移性胃或胃食管交...
2024-10-25 14:49
 资讯
资讯 华东医药2024年三季报亮点:创新引领医药工业板块高增长,多款新药蓄势待发
报告显示,2024年1-9月公司合计实现营业收入314 78亿元,同比增长3 56%;实现归母净利润25 62亿元,同比增长17 05%,实现扣非归母净利润24 82亿元,同比增长14 90%。
2024-10-24 18:47