因为一份网传的会议纪要,港股18A药企康诺亚近两日过得有点起伏。
股价“闪崩”
5月29日,一份网传的会议纪要显示:5月中旬康诺亚和监管机构沟通,获得对CM310疗效和安全性的正面反馈,但监管同时主要要求康诺亚补充长期、大样本人群数据。如若按照该纪要表达的意思,即现有的临床数据还不完全足以支持CM310的上市申请,该产品的临床试验时间或将被延长,相应地也将延后其上市时间。
上述消息一出,康诺亚二级市场表现随即出现异动,其股价一路下探,盘中一度跌至39港元每股,创2022年10月以来新低,当日收盘跌幅则高达24.46%,来了个“闪崩”。
康诺亚坐不住了,5月30日,其发布公告称,CM310治疗中重度特应性皮炎(AD)的III期确证性临床研究已完成揭盲及初步统计分析,主要研究终点均成功达到。按临床方案规定,公司正在持续推进并收集本次三期临床的长期疗效及安全性数据,且无需就有关数据收集招募更多额外患者,公司将持续与国家药监局药品审评中心进行沟通,积极推动CM310用于成年人中重度特应性皮炎治疗的上市申请。该公告一定程度上提振了康诺亚的股价,5月30日其收盘涨幅达9.33%。
但业内指出,这份公告并未说明其需要补充的具体临床疗效时间数据,这对于上市进程来说仍然具有不确定性。
疗效评估时间或将延长
市场对CM310的上市动态如此敏锐,是因为其是一款被寄予了厚望的创新产品。
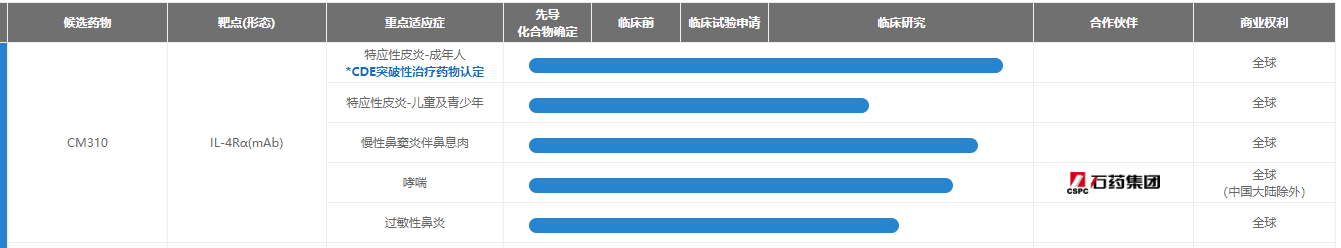
据了解,CM310是康诺亚自主研发的1类新药,是一款针对白介素4受体α亚基(IL-4Rα)的高效、人源化抗体,通过靶向IL-4Rα,CM310可双重阻断白介素4(IL-4)及白介素13(IL-13)的信号传导,IL-4及IL-13为引发II型炎症的两种关键细胞因子,在过往多项临床试验中,CM310已显示了良好的安全性及疗效,其也是首个国产且获得国家药监局临床试验申请批准的IL-4Rα抗体。
根据康诺亚官网信息显示,CM310临床研究开展的针对适应症包括特应性皮炎(成人、青少年和儿童)、慢性鼻窦炎伴鼻息肉、哮喘、以及过敏性鼻炎,其中,特应性皮炎研究最为靠前,也是CM310即将提交上市申请的主打适应症。
值得注意的是,CDE去年11月曾出台意见稿《特应性皮炎治疗药物临床试验技术指导原则》明确指出:因特应性皮炎病程通常具有长时间持续和反复发作的特点。通常,不论患病期间疾病活动度是否存在波动,成人患病周期至少一年,青少年(12-18岁)至少半年,2岁及以上患者至少3个月。针对药物的试验疗效评估,全身治疗药物给药周期最短3个月,外用治疗药物给药周期最短1个月。通常,对长期疗效维持数据至少需52周。按照该《指导原则》,则意味着外用治疗药物CM310需要52周的长期疗效时间观察,但目根据康诺亚方面的信息,目前CM310的疗效时间数据仅为16周。
CM310 16周的疗效数据来源于一项名为CM310AD005的多中心、随机、双盲、安慰剂对照的III期确证性临床研究,该研究主要用于评价CM310用于中重度特应性皮炎受试者的疗效、安全性、PK特征、PD效应和免疫源性。符合入组标准的受试者以1:1的随机比例,分别接受CM310(600mg–300mg Q2W)和安慰剂治疗。以治疗16周时达到湿疹面积及严重指数(EASI)-75(EASI评分较基线降低≥75%)的达标率及研究者整体评分法(IGA)评分达到0或1分且较基线下降≥2分的达标率为共同主要终点。
在文章开头曝出的会议纪要中,康诺亚也表示临床试验的观察时间可能要延长到52周,预计要到本年年底前完成52周的临床试验观察,而这带来的多米诺骨牌效应是明显的,根据瞪羚社的报道,康诺亚或至少在今年第三季度后才能递交CM310的上市申请,即使CM310此前已被CDE授予突破性疗法,意味着审查时间会快于一般药物,但也很难在2024年6月之前获批,这就会导致错过2024年的医保谈判,最终错失2025年进入医保执行的机会,而越到后期,随着医保谈判价格降幅的不确定性,如何定价也将是一件非常难的决定。市场此前对于CM310的信心也就此打了折扣。
强劲的对手
值得一提的是,CM310实则对标的是赛诺菲与再生元合作研发的“重磅炸弹”产品度普利尤单抗(商品名:Dupixent),这也是一款靶向IL-4Rα的药物。2014年,度普利尤单抗曾凭着优异的临床试验数据获得美国FDA突破性疗法认证,并于2017年批准上市,成为全球首个用于成人中重度特应性皮炎的靶向生物制剂。
除了特应性皮炎,度普利尤单抗还斩获了包括慢性鼻窦炎伴鼻息肉、哮喘等多种免疫性疾病适应症。去年5月,度普利尤单抗就获得了美国FDA批准,用于治疗12岁及以上的嗜酸性粒细胞性食管炎(EoE)患者,与此同时,度普利尤单抗还有多项临床研究在进行中,涉及2型炎症性慢阻肺、大疱性类天疱疮、慢性自发性荨麻疹、慢性诱导性寒冷性荨麻疹、慢性鼻窦炎不伴鼻息肉等。
2020年6月,度普利尤单抗在中国获批上市用于治疗成人中重度特应性皮,比原计划提前了两年,商品名为达必妥,并于同年进入国家医保目录,此后,又相继获批可用于治疗12岁-17岁青少年特应性皮炎患者、6岁及以上特应性皮炎患者,昨日(5月30日),度普利尤单抗新获批用于6个月至5岁患有中重度特应性皮炎(AD)的婴幼儿,成为国内目前首个也是唯一一个被批准用于治疗从婴儿期到成年期覆盖全年龄人群的中重度特应性皮炎靶向生物制剂,也是同类首个可用于6个月及以上婴幼儿的治疗用生物制剂。
业绩方面,自获批上市以来,度普利尤单抗销售一路上扬,2017年-2021年,其分别取得销售额业绩2.19亿欧元、7.88亿欧元、20.74亿欧元、35.34亿欧元、52.49亿欧元、82.93亿欧元,累计销售已超200亿欧元。另有消息称,在国内治疗中重度特应性皮炎的靶向IL-4Rα生物制剂领域,度普利尤单抗有着强劲的先发优势,其去年在中国的销售额已接近20亿元人民币。
另一边,特应性皮炎患者还在不断增加,有统计数据显示,发达国家儿童特应性皮炎患病率约10%-25%,成人患病率约2%-8%,而我国特应性皮炎患病率近年来也增长迅速,患群的不断扩大也是CM310此前被寄予厚望的原因之一,其一旦获批上市,就能获得与度普利尤单抗瓜分庞大市场的资格,有分析人士乐观地表示,在三期临床已经成功的背景下,CM310延迟递交对最终成功上市的结果并不会有影响。
来源:医谷网
为你推荐
 资讯
资讯 CDE:可复制型慢病毒检测共性问题与技术要求
药审中心对细胞和基因治疗产品中可复制型慢病毒检测共性问题进行整理,组织制定了《可复制型慢病毒检测共性问题与技术要求》,内容旨在针对这类慢病毒载体系统的 RCL 检测问题...
2024-10-29 22:32
 资讯
资讯 药品耗材挂网“一省核验、全国通享”启动,2025年1月1日起全国各省全部正式上线
10月29日,山东省医保局发布《关于开展医药产品挂网全国联审通办试运行工作的通知》,药品耗材信息一次提交,一省核验、全国通享正式进入试点执行阶段。
2024-10-29 21:58
 资讯
资讯 罗氏七赴进博,深耕中国三十周年,聚力共筑健康未来
罗氏将以“华彩三十,聚氏未来”为主题,于1000平方米的进博展台上全面展示超过30款已上市和即将在华上市的全产品矩阵及创新解决方案,重磅推出3款即将在华获批的全球创新产品。
2024-10-29 14:50
 资讯
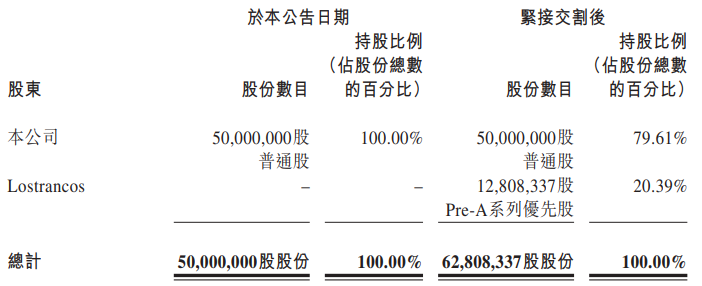
资讯 信达生物转让子公司约20%股权
近日,信达生物发布通告称,全资子公司Fortvita与Lostrancos签订了认购协议,Lostrancos有条件同意按认购价认购及购买,而Fortvita有条件同
2024-10-29 14:37
 资讯
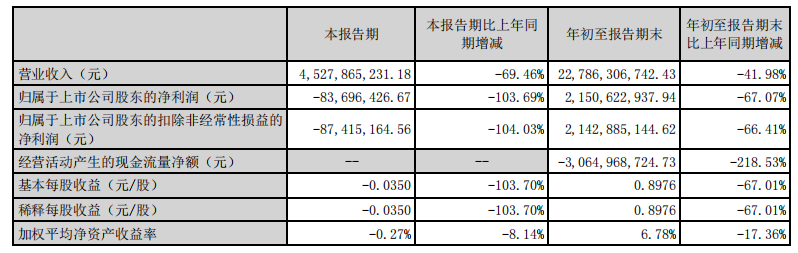
资讯 HPV疫苗卖不动了?智飞生物三季报净利润腰斩
近日,智飞生物发布2024年三季度报告。财报显示,今年前三季度,公司实现营业收入为227 86亿元,同比减少41 98%;归属于上市公司股东的净利
2024-10-29 14:02
 资讯
资讯 2024爱尔眼科眼底病论坛(湖南站)盛大召开
由爱尔眼科长沙医学中心、爱尔眼科湖南省区眼底病学组、湖南爱眼公益基金会主办,长沙爱尔眼科医院、长沙湘江爱尔眼科医院承办的“2024爱尔眼科眼底病论坛(湖南站)暨疑难眼底...
2024-10-27 11:37
 资讯
资讯 特应性皮炎患者人手必备的“百科全书”,《特应性皮炎365问》正式启动
近日,2024樱花皮肤健康学术周在线上顺利召开,会议期间,作为由中华医学会皮肤性病学分会发起的皮肤健康三年行动(2024-2026)的重要组成部分,365科普书系列《特应性皮炎365...
2024-10-27 11:29
 资讯
资讯 2024青岛呼吸产业大会暨第二十三届呼吸周圆满举办,多领域、多维度共同守护亿万国民呼吸健康
本届大会由青岛市人民政府主办,青岛市科学技术局、青岛市工业和信息化局、青岛国家高新技术产业开发区管理委员会、医师报与阿斯利康联合承办。
2024-10-26 10:03
 资讯
资讯 肾癌质控首批试点中心建设启动,持续推动肿瘤治疗公平性
2024年10月25日,由国家癌症中心国家肿瘤质控中心肾癌质控专家委员会指导、北京中康联公益基金会主办、北京大学第一医院承办的“国家癌症中心肾癌质控专家委员会第一批试点中心...
2024-10-25 20:50
 资讯
资讯 2024 Veeva中国商务峰会成功举办,推动生命科学领域数字化营销新变革
10月24日,在全球数字化转型浪潮与医药行业深刻变革的交汇点,全球生命科学行业云软件领导者Veeva Systems成功举办“2024 Veeva中国商务峰会”。本次峰会以“一起领新V来”为...
2024-10-25 17:19
 资讯
资讯 安斯泰来VYLOY获美国FDA批准用于治疗晚期胃和胃食管交界处腺癌
近日,安斯泰来宣布,美国食品和药品监督管理局(FDA)已批准VYLOY®(zolbetuximab-clzb)与含氟尿嘧啶和铂类化疗药物联合用于一线治疗患有局部晚期不可切除或转移性胃或胃食管交...
2024-10-25 14:49
 资讯
资讯 华东医药2024年三季报亮点:创新引领医药工业板块高增长,多款新药蓄势待发
报告显示,2024年1-9月公司合计实现营业收入314 78亿元,同比增长3 56%;实现归母净利润25 62亿元,同比增长17 05%,实现扣非归母净利润24 82亿元,同比增长14 90%。
2024-10-24 18:47