近日,据中国药物临床试验登记与信息公示平台显示,赛诺菲针对其肌萎缩侧索硬化症(又名“渐冻人症”)疗法SAR443820在中国启动一项二期临床试验。
据公示的试验信息显示,赛诺菲本次登记的是一项随机、双盲、安慰剂对照的国际多中心2期临床研究,主要目的是评估SAR443820与安慰剂相比在减缓ALS进展方面的作用(通过修订版肌萎缩侧索硬化功能评分量表[ALSFRS-R]测定),次要目的是评估SAR443820与安慰剂相比对功能和生存期的综合评估、唿吸功能、肌肉力量和生活质量(QoL)的影响。该研究计划在国际入组261人,中国境内入组44人,主要在北京大学第三医院、浙江大学医学院附属第二医院、四川大学华西医院、华中科技大学同济医学院附属同济医院等医疗机构开展。
公开资料显示,SAR443820是一种新型的CNS渗透性小分子RIPK1抑制剂,具有穿越血脑屏障的潜力。2018年10月,赛诺菲和Denali公司就RIPK1抑制剂的全球开发和商业化展开广泛合作,赛诺菲将领导SAR443820治疗ALS和MS的1期临床和2期临床开发,并与Denali公司一起进行该药治疗ALS、MS和阿尔茨海默病的3期临床试验。
在健康志愿者中进行的1期临床试验中,SAR443820在耐受性良好的剂量下,表现出与靶点的强力相互作用。基于这些结果,赛诺菲决定在ALS患者中启动2期临床试验,此前,美国FDA已经授予SAR443820治疗ALS的快速通道资格。
来源:医谷网
为你推荐
 资讯
资讯 超10亿美元,映恩生物创新临床前ADC药物授权GSK
12月4日,映恩生物宣布与GSK已就一项抗体偶联药物(ADC)DB-1324达成独家授权协议。根据协议,GSK将获得全球(不包括中国大陆、香港地区和澳门地区)的独家授权,以推进该ADC药...
2024-12-04 09:56
 资讯
资讯 拜耳在2024年北美放射学会年会上展示其放射学组合创新
拜耳继续推进其全面的放射学产品组合,在开发管线和人工智能(AI)领域的创新都取得了进展。公司将在2024年12月1日至5日在美国芝加哥举行的北美放射学会年会上展示Gadoquatrane...
2024-12-03 15:44
 资讯
资讯 优时比与博锐生物达成战略合作,加速倍捷乐®中国上市进程
在中国,比奇珠单抗已于2024年7月获得中国国家药品监督管理局(NMPA)批准,用于治疗常规疗法效果不佳或不耐受的活动性强直性脊柱炎(AS)成人患者,并于9月获批用于治疗放射学...
2024-12-03 10:35
 资讯
资讯 CPL-01有望开启镇痛新时代,远大生命科学集团与加立生科达成战略合作
根据协议约定,远大生命科学将向加立生科支付首付款,以及里程碑款;同时加立生科授权远大生命科学为其CPL-01项目在中国的独家商业化合作伙伴,并根据协议约定向远大生命科学支...
2024-12-02 09:25
 资讯
资讯 全国中药饮片采购文件正式发布,涉45个品种
本次联合采购中药饮片45个品种,分别为黄芪、党参片、金银花、当归、红花、麦冬、太子参、白芍、川芎、丹参、山药、蒲公英、牡丹皮、桔梗、炙黄芩、白术、炒白芍、炙甘草、茯苓...
2024-11-30 11:20
 资讯
资讯 国家药监局发布医药代表管理办法(征求意见稿)
医药代表应当具有医学、药学或相关专业本科及以上学历(或者中级及以上专业技术职称);具有药品临床理论知识及实践经验,或者具有药品研发、生产、检验、质量管理等岗位工作经...
2024-11-29 18:50
 资讯
资讯 三高共管,三慢共防:2024中国医药城大健康产业论坛“慢病协同共管”专题圆满举办
大会以“三高共管,三慢共防”为主题,聚焦共病共管、心肾保护、跨界融合、慢病管理创新模式、创新产业技术等前沿内容
2024-11-29 15:03
 资讯
资讯 湖南省视觉功能及儿童眼病学术研讨会暨世界近视眼大会成果宣讲会在长沙举办
11月28日,由爱尔眼科湖南省区视光学组、爱尔眼科湖南省区小儿眼科学组主办、长沙爱尔眼科医院承办的“湖南省视觉功能及儿童眼病学术研讨会暨世界近视眼大会成果宣讲会”,在长...
2024-11-29 09:09
 资讯
资讯 一个手功能康复训练仪器的设计
系统由3个模块组成:指示锻炼情况和治疗持续时间,并为气动螺纹管提供动力的驱动泵;穿戴在健康一侧手臂的镜像手环,及穿戴在患肢的康复机器手套。
2024-11-29 09:02
 资讯
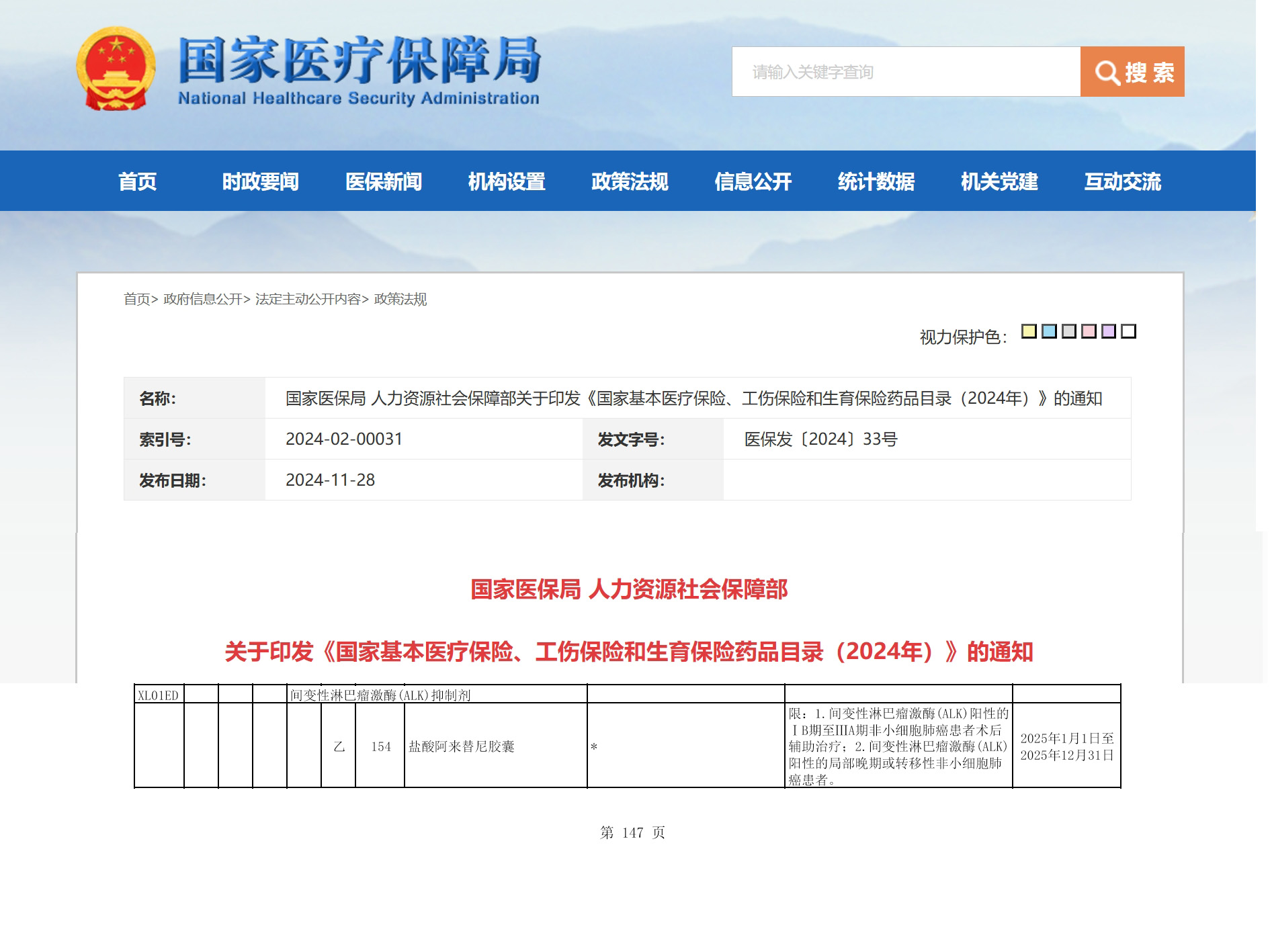
资讯 阿来替尼ALK阳性早期NSCLC术后辅助治疗适应症成功纳入医保
2024年11月28日,国家医保局公布了《国家基本医疗保险、工伤保险和生育保险药品目录(2025年)》(以下简称:国家医保目录),安圣莎®(通用名:阿来替尼)ALK阳性早期非小细胞...
2024-11-28 18:58
 资讯
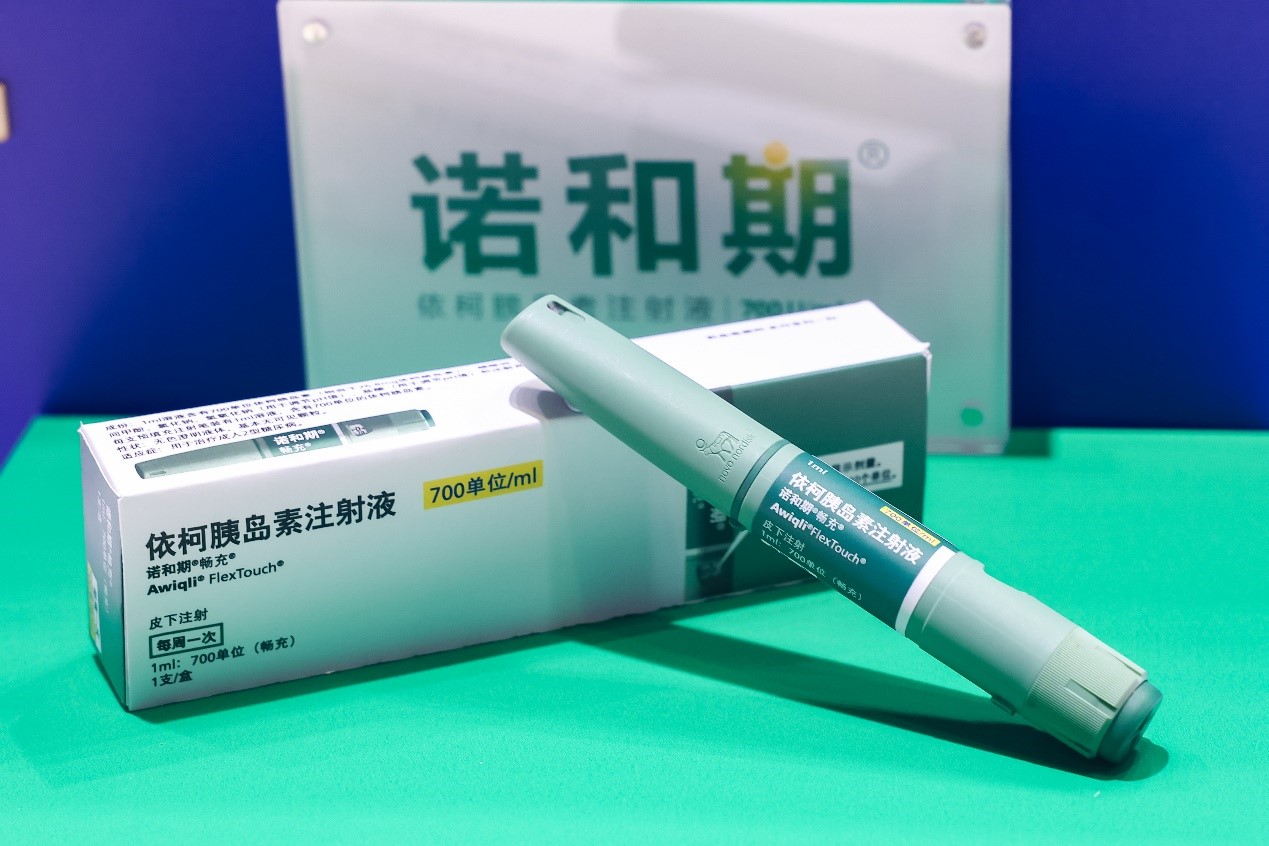
资讯 全球首个胰岛素周制剂诺和期(依柯胰岛素注射液)成功纳入国家医保目录
11月28日,根据国家医疗保障局最新公布,依柯胰岛素注射液(商品名诺和期®)被纳入《国家基本医疗保险、工伤保险和生育保险药品目录(2024年)》。目录将于2025年1月1日起正式执行。
2024-11-28 15:52
 资讯
资讯 一款国产PD-1被首次被纳入,多款“全球新”在列,2024国家医保谈判结果发布(附完整版目录下载链接)
今日(11月28日),2024年版国家医保药品目录调整名单正式公布。
2024-11-28 14:49
 资讯
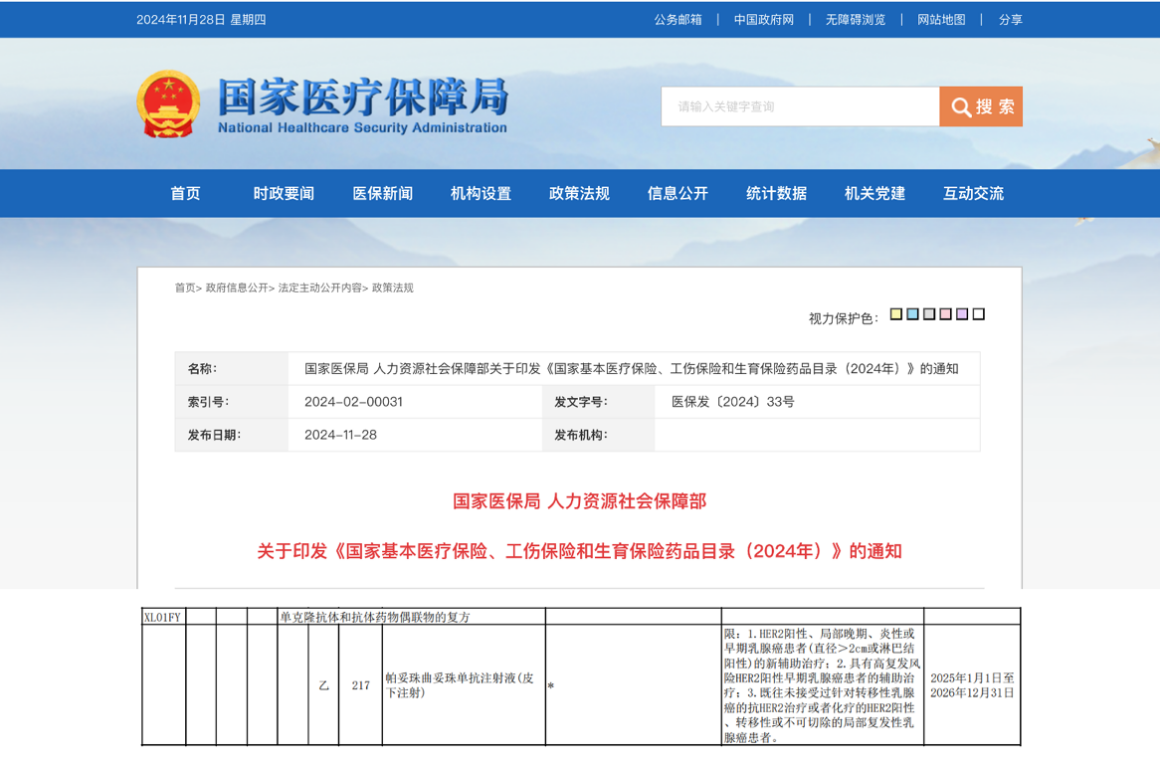
资讯 首个抗HER2复方皮下制剂赫双妥纳入国家医保目录,5-8分钟靶向治疗助力乳腺癌患者拥抱自由新生
2024年11月28日,国家医疗保障局发布最新公告,罗氏抗HER2乳腺癌皮下生物制剂赫双妥®(通用名:帕妥珠曲妥珠单抗注射液(皮下注射))正式进入《国家基本医疗保险、工伤保险和...
2024-11-28 13:53









