这是Insight数据库利用自身数据制作的「上市新药报告」,带你一起追踪CFDA(国家食药监总局)、EMA(欧洲药物管理局)、FDA(美国食品药品监督局)最新上市药品动态。
本次报告采集时间:2018.1.26 - 2018.3.15
EMA药品动态
批准上市3个新药
EMA通过的3个药品中,基本都已在FDA上市。
其中,日本药企协和麒麟和Ultragenyx合作的Crysvita(Burosumab)是治疗 X 连锁低磷血症(XLH)第一个获得批准的新药。
据悉,美国食品和药物管理局(FDA)也正在评审Crysvita的生物制剂许可证申请,用于治疗XLH的儿童和成人患者。预计评审结果将在4月下旬公布。
FDA药品动态
批准了5个新子实体上市
值得一提的是,Trogarzo是由中裕新药创制、药明生物协助生产的创新药物,也是美国FDA在 2018 年批准的首款创新生物药,Trogarzo作为一种全新的抗逆转录病毒疗法,治疗现有多种疗法均无法起效的成人HIV感染者。
批准了9个首仿药物上市
CFDA药品动态
有12个品种即将上市
即将上市药物筛选规则:
使用Insight数据库(https://db.dxy.cn)
离开CDE时间:本报告采集时间内
申请类型:进口、新药
申请内容:上市申请
删除有不批准、批准公示的药物
来源:Insight数据库 作者:音sir
为你推荐
 资讯
资讯 国家药监局发布医药代表管理办法(征求意见稿)
医药代表应当具有医学、药学或相关专业本科及以上学历(或者中级及以上专业技术职称);具有药品临床理论知识及实践经验,或者具有药品研发、生产、检验、质量管理等岗位工作经...
2024-11-29 18:50
 资讯
资讯 三高共管,三慢共防:2024中国医药城大健康产业论坛“慢病协同共管”专题圆满举办
大会以“三高共管,三慢共防”为主题,聚焦共病共管、心肾保护、跨界融合、慢病管理创新模式、创新产业技术等前沿内容
2024-11-29 15:03
 资讯
资讯 湖南省视觉功能及儿童眼病学术研讨会暨世界近视眼大会成果宣讲会在长沙举办
11月28日,由爱尔眼科湖南省区视光学组、爱尔眼科湖南省区小儿眼科学组主办、长沙爱尔眼科医院承办的“湖南省视觉功能及儿童眼病学术研讨会暨世界近视眼大会成果宣讲会”,在长...
2024-11-29 09:09
 资讯
资讯 一个手功能康复训练仪器的设计
系统由3个模块组成:指示锻炼情况和治疗持续时间,并为气动螺纹管提供动力的驱动泵;穿戴在健康一侧手臂的镜像手环,及穿戴在患肢的康复机器手套。
2024-11-29 09:02
 资讯
资讯 阿来替尼ALK阳性早期NSCLC术后辅助治疗适应症成功纳入医保
2024年11月28日,国家医保局公布了《国家基本医疗保险、工伤保险和生育保险药品目录(2025年)》(以下简称:国家医保目录),安圣莎®(通用名:阿来替尼)ALK阳性早期非小细胞...
2024-11-28 18:58
 资讯
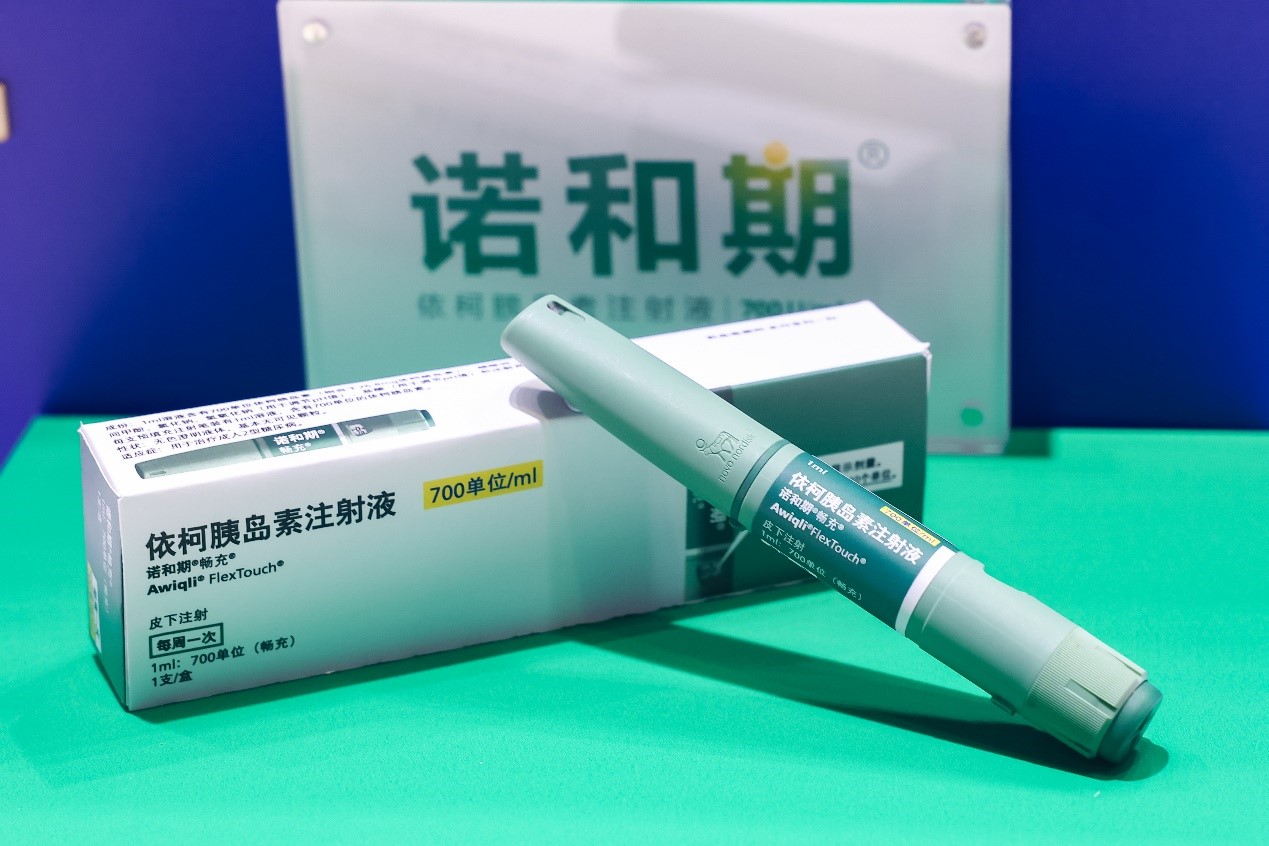
资讯 全球首个胰岛素周制剂诺和期(依柯胰岛素注射液)成功纳入国家医保目录
11月28日,根据国家医疗保障局最新公布,依柯胰岛素注射液(商品名诺和期®)被纳入《国家基本医疗保险、工伤保险和生育保险药品目录(2024年)》。目录将于2025年1月1日起正式执行。
2024-11-28 15:52
 资讯
资讯 一款国产PD-1被首次被纳入,多款“全球新”在列,2024国家医保谈判结果发布(附完整版目录下载链接)
今日(11月28日),2024年版国家医保药品目录调整名单正式公布。
2024-11-28 14:49
 资讯
资讯 首个抗HER2复方皮下制剂赫双妥纳入国家医保目录,5-8分钟靶向治疗助力乳腺癌患者拥抱自由新生
2024年11月28日,国家医疗保障局发布最新公告,罗氏抗HER2乳腺癌皮下生物制剂赫双妥®(通用名:帕妥珠曲妥珠单抗注射液(皮下注射))正式进入《国家基本医疗保险、工伤保险和...
2024-11-28 13:53
 资讯
资讯 罕见病创新药盐酸伊普可泮胶囊纳入2024年国家医保药品目录
作为全球首个且唯一获批的特异性补体旁路B因子抑制剂和成人阵发性睡眠性血红蛋白尿症(PNH)口服单药疗法,纳入医保会大大提升患者用药可及性及便利性,为PNH患者带来新的治疗选择。
2024-11-28 13:09
 资讯
资讯 强生2款创新药物纳入新版国家医保目录,惠及更多中国患者
今日(11月28日),在国家医疗保障局公布的《国家基本医疗保险、工伤保险和生育保险药品目录(2024版)》(以下简称:国家医保目录)中,强生的2款创新药物收获了好消息,包括兆...
2024-11-28 12:25
 资讯
资讯 深化创新产品布局 远大生命科学集团获得幽门螺杆菌创新治疗药物独家商业化权益
根据协议条款,远大生命科学将独家负责TNP-2198在中国大陆、香港、澳门的市场推广和商业化销售。丹诺医药将继续负责TNP-2198针对幽门螺杆菌的后续全部临床、非临床和药学研究、...
2024-11-28 09:28
 资讯
资讯 2024青年防艾公益行动在京启动,防艾主题艺术作品在全国11座城市亮相
在第37个“世界艾滋病日”到来之际,由中国性病艾滋病防治协会与中国青年报社共同主办、吉利德科学公益支持的“2024青年防艾公益行动”正式启动。
2024-11-27 18:51
 资讯
资讯 推动智能实验室进化,安捷伦在Analytica China 2024展示技术与服务创新
近日,第12届慕尼黑上海分析生化展隆重举行,安捷伦科技公司如期亮相。本届展会,安捷伦以“创新不止,深谙所需”为主题,重点展示一系列创新的技术与服务,借以诠释公司对科学...
文/史士云 2024-11-27 17:21












