每年,全球超过32万人被诊断为肾细胞癌(Renal Cell Carcinoma, RCC, 也简称肾癌),超过14万人死亡。在美国,肾癌为第9大癌症,2017年预计发生63,990 例,死亡14,400例。早期的肾癌多可以通过手术切除治愈,三期进展的肾癌五年存活率为53%,晚期转移性的肾癌(mRCC)则仅为8%。肾癌总体五年平均生存率为75%。
国内肾癌发病率在过去20年间,以平均每年6.5%的速度增长,已经超过膀胱癌成为泌尿系统疾病首位。肾癌高发的诱因与不良生活方式关系很大,吸烟、喝酒、肥胖,还包括中药肾脏毒副作用等。
75-80%的肾癌为透明肾细胞癌(clear cell renalcell carcinoma (ccRCC)),其余为非透明肾细胞癌(non-clear cellcarcinoma (nccRCC)),也叫乳头状肾细胞癌。又被分为二类,I型(5%)、II型 (10%)。I型多具有遗传性,原癌酪氨酸激酶基因MET的变异会增加患病风险 [1]。
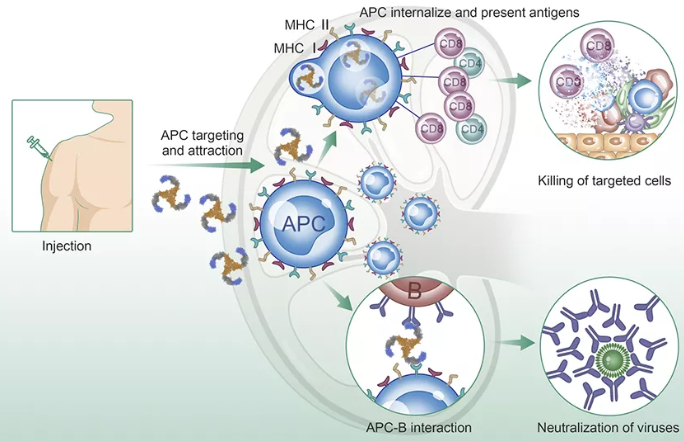
靶向疗法之前,化疗在转移性肾细胞癌上疗效甚微,几乎没有获益。后来免疫细胞因子,IL-2及IFN-α,原始态的免疫疗法,基于较好的应答率于1992年获得FDA的批准,用于治疗肾细胞癌。IL-2 的获批是第一次通过增加个体的免疫反应对抗肿瘤的尝试,意义重大。但总体而言,原始的免疫疗法不是非常给力,总体的特点:疗效低,毒性极大,且不可预测,极少情况下会出现治愈奇迹。
肾癌靶向疗法的理论基础
一个是Kaelin et al.发现von Hippel-Lindau (VHL) 基因突变,在透明细胞肾癌中高达四分之三,VHL突变导致不能降解缺氧诱导因子(hypoxia-inducible factor-1α(HIF-1α))。HIF-1 α的积累是参与血管生成下行信号的有力激活剂[2],从而导致VEGF的过量表达和肿瘤血管增生。
另外一个重要的变异途径即是常染色体显性遗传性疾病,结节性硬化症(tuberous sclerosis),主要发生在非透明肾细胞癌。结节性硬化症的基因突变经常会导致下游的Rheb蛋白失活,从而持续激活了PI3K/mTOR信号通路,进而促进了VEGF、PDGF等介导的肿瘤血管增生 [3]。
肾细胞癌血管增生信号通路
靶向VEGF/VEGFR血管增生通路
转移性肾细胞癌第一个一线获得FDA批准的VEGFR靶向疗法是辉瑞的sunitinib(Sutent,2006年3月), 主要作用于VEGFR、PDGFR 等血管生成途径靶点。Sunitinib不直接抑制肾癌细胞的生长,而是主要作用于肿瘤相关的新生血管。它的PFS比之前的标准疗法IFN-α有了较大的提高(11个月:5个月),大大减轻了肾细胞癌的恶劣性。主要副作用为高血压(12%)、疲劳(11%)、腹泻(9%),和手足综合征(9%)等 [4, 5]。
随后,另一个VEGFR抑制剂pazopanib也于2009年获得FDA批准。其PFS 远远好于安慰剂(11.1 vs. 2.8 个月)。主要副作用为腹泻(52%)、高血压(40%)、头发颜色的变化(38%)和恶心(26%)等 [6]。
为了比较sunitinib与pazopanib谁作为一线使用更有效,二者做了一个头对头的三期临床比较试验。结果表明二者差别不大,PFS pazopanib为10.5 个月,sunitinib为10.2 个月。从患者的问卷调查来看,更多的人选择pazopanib。有趣地是,二者虽然主要靶点都是VEGFR,但脱靶靶点不尽相同,结果造成二者的毒副作用差别很大。Pazopanib的手足综合症、疲劳、骨髓抑制均低于sunitinib,但肝损伤要比sunitinib严重。Pazopanib引起头发颜色的变化可能与其靶向CSF-1R有关,即最近介绍的巨噬细胞的靶点 [7],因为这个也是巨噬细胞选择性小分子抑制剂和抗体的主要靶向相关副作用之一。这些不同的毒副作用在临床上也用于指导个性化的用药选择,比如有肝脏功能缺陷的患者应该选择肝损伤较小的sunitinib [8]。
高血压为靶向VEGFR的靶向直接相关毒副作用。而它也是一个有效的良好预后生物标志物(biomarker of efficacy)。出现高血压的患者比不出现高血压的比例疗效显著:ORR ,54.8%:8.7%;PFS,12.5:2.5;OS,30.9:7.2 [9]。
Bevacizumab是VEGF-A配体的单抗,即Roche/Genentech的重磅抗癌药物Avastin。Bevacizumab与IFN-α 合用跟安慰剂与IFN-α.合用相比,PFS和ORR均大幅提高(10.2 vs 5.4 个月), ORR(30.6 vs 12.4%)。Bevacizumab于2009年获FDA批准,用于mRCC 一线。总体疗效与VEGFR的两个一线VEGFRTKI相当。
Sorafenib 治疗IL-2或IFN-a耐受的患者比安慰剂效果好(PFS 5.5 : 2.8 个月),但作为一线与IL-2比较时,效果不显著。所以Sorafenib虽然获批更早,但应用标签是用于IL-2或IFN-a耐药患者。
Axitinib 作为二线使用效果显著。但一线与sorafenib相比,效果不显著。它也只能在二线使用。
Cabozantinib 是一个多靶点的酪氨酸激酶抑制剂,靶点包括RET、VEGFR、MET、KIT,、AXL等。最初基于靶向RET获得FDA批准用于转移性甲状腺髓样癌。在与everolimus的二线应用比较中,cabozantinib表现出色,于2016年获批用于mRCC二线。
靶向mTOR信号通路
PI3K家族蛋白丝氨酸/苏氨酸激酶mTOR在2000初曾经是非常火热的抗肿瘤靶点之一。但总体结果来看雷声大雨点小、毒性大、有效适应症少。2007年,mTOR抑制剂temsirolimus获得FDA批准,用于靶向肾细胞癌的一线治疗。从数据上看,PFS和ORR比对照组有所提高(3.8个月:1.9个月;9%:7%),但总体效果没有VEGFR靶点抑制剂有效。但由于temsirolimus能够相对有效的靶向非透明肾细胞癌,扩大了靶向疗法的覆盖范围。
另一个mTOR抑制剂everolimus与temsirolimus的效果类似。但在与sunitinib相比时,没有表现出非劣性。所以,everolimus的使用标签是用于VEGFRTKI耐药后二线使用 [8]。
免疫疗法
与黑色素瘤、肺癌等一样,肾细胞癌也有较多的突变负荷和免疫原性,对PD-1/PD-L1免疫疗法也有较好的应答。施贵宝的PD-1 单抗nivolumab二线与everolimus相比,ORR显著提高(25%:5%);OS 提高显著(25:19.6个月);但PFS数据不明显(4.6:4.4)。2015年11月,FDA批准了施贵宝的nivolumab二线用于肾细胞癌的治疗 [10, 11]。最近一项5年的随访调查显示,nivolumab作为VEGFR TKI一线耐药后的维持疗法,生存率达到34% [12]。而mRCC五年的传统生存率只有8%,靶向疗法与免疫疗法惯序使用取得的获益还是非常明显的。
FDA批准的靶向转移性肾细胞癌的药物汇总
组合疗法进展及前景
Lenvatinib 与cabozantinib一样,也是多靶点的酪氨酸激酶抑制剂,最初首先获批于转移性甲状腺髓样癌,主要靶点包括 VEGFR1-3、FGFR1-4、PDGFRα、RET、KIT等。作为后来的VEGFR TKI,它没有去mRCC一线,或二线开展单用的临床试验,而是直接展开了组合疗法的试验,结果也获得成功。Lenvatinib与everolimus联用效果好于单用everolimus或lenvatinib, PFS (14.6:5.5:7.4)。Lenvatinib+Everolimus组合疗法于2016年5月获得FDA批准用于VEGFR TKI耐药后的二线患者 [13]。
这个三臂试验非常有意义,确认了在mRCC中同时靶向VEGFR与mTOR能够互相增益,而毒副作用虽有所增加,却还能够耐受。而之前的Bevacizumab与VEGFR的TKI的几个组合试验都因为毒性过大而夭折。
最值得期待还是以免疫疗法为支柱的组合疗法,包括免疫疗法与靶向疗法在mRCC上的表现。经典的靶向药靶点如EGFR 或ALK等靶向驱动突变与PD-1/PD-L1免疫疗法的作用人群属于井水不犯河水,二者没有交集。与非小细胞肺癌的情况不同,在mRCC上,PD-1抗体能够有效地跟在VEGFRTKI耐药后起作用。同时,PD-1与VEGFRTKI的组合联用也许才是最具潜力的。背后的科学依据在于VEGFR血管生成通路能够直接影响肿瘤微环境,如促进髓系基质细胞(myeloid-derived stromal cells)活性,直接抑制积极的抗肿瘤免疫反应。
Axitinib 当初作为一线使用的临床试验没有成功。现在,找了个免疫疗法的帮手,成功的机会大增。初步的临床试验结果显示axitinib+avelumab(PD-L1检查点抑制剂)ORR 高达58.2%,非常积极(2017, ASCO)。
PD-1与IDO 小分子抑制剂也展现出良好的潜力。今年ASCO的初步数据显示,PD-1与IDO抑制剂联用(pembrolizumab 和IDO 抑制剂epacadostat),在肾细胞癌上数据非常积极,ORR 达到47% (2017,ASCO #4515)。
8月16日,施贵宝更新了免疫组合疗法nivolumab与 ipilimumab的三期数据,ORR 为41.6 对sunitinib的26.5%,统计数据显著。但PFS 11.6对8.4个月,对比不够显著。最重要的生存数据(OS)还没有完成。总体来看数据还算积极。PFS不显著对免疫疗法来说时有发生,应该不是关键的数据。一个比较重要的担心倒是二者联用可能引起较为严重的免疫相关毒副作用。
8月17日,Exelixis向FDA递交了MET/VEGF双抑制剂cabozantinib的一线肾癌用药申请。在一个157人的二期临床试验中,cabozantinib与sunitinib相比,PFS 8.2:5.6个月,统计数据显著,ORR 为46:18%,数据显著。OS 30.3:21.8个月,不显著。有不少人对这个试验有些看法: 人数较少,sunitinib的数据与传统数据相比偏低。当然,市场已经认可cabozantinib会获得批准用于一线,(exelixis市值翻了近10倍),甚至有人建议辉瑞应该收购Exelixis,用以填补sunitinib专利到期后的空白以及降低对sunitinib的冲击。
Cabozantinib是一个典型的多靶点激酶抑制剂,在肾细胞癌上,它的优势据说主要是双抑制VEGF和MET。这个就是一个典型的“自带组合”踩到点上的例子。如果这个假说成立,那么辉瑞倒不如开发一下自家的组合疗法,sunitinib加crizotinib。一般来说,靶向疗法的组合瓶颈主要是毒副作用太大,患者无法忍受。而crizotinib的MET活性比已经获批的ALK+适应症活性高3-5倍。这样,crizotinib也许可以仅用三分之一的剂量来与sunitinib联用,从而能够大大降低毒性。如果毒性偏大,也许可以进一步开发间歇给药的方案 [14],来降低联用的毒性,同时也许能够提高疗效。下面还会简单重复介绍一下sunitinib间歇给药的积极进展。
靶向转移性肾细胞癌的在研临床试验组合药物
用药顺序及间歇给药
来自美国国家癌症综合网(NCCN)和欧洲协会泌尿科的一级建议是首先使用酪氨酸激酶抑制剂(TKI),特别是Sunitinib和pazopanib。所以临床实践中,sunitinib 和pazopanib 现在还是一线主力。这个是比较明确的。
至于一线耐药后的二线使用次序则存在较多争议,特别是当没有头对头的比较时,非常难以判断不同药物疗效的优劣。ZarrabiK 等人最近的综述中总结了临床数据和众多实践指南,推荐首先选择cabozantinib 或PD-1免疫检查点抑制剂nivolumab。若有进展,再依次选择组合疗法lenvatinib 加everolimus、axitinib、sorafenib,最后可以用Bevacizumab打底 [8]。
肾细胞癌推荐用药顺序
肾细胞癌有着非常大的异质性,同时也表现在可治愈程度上,即部分患者会有特别好的应答,甚至治愈。这个特点也许是间歇给药临床试验能够成功的原因之一。前文专门介绍了间歇给药的进展。这里再贴一遍间歇给药的临床试验疗效图结。患者22、25、34即是间歇给药的最大获益者。经过一轮密集给药,停药后可以获得持续缓解,且缓解时间超过2年。初步结果看来,肾细胞癌靶向微环境的药物间歇给药的获益潜力非常大。PFS与传统数据比较几乎可以翻倍(22.4 个月) [14]。
Sunitinib间歇给药疗效图解
小结
以前对肾细胞癌的靶点不是很了解,总觉得VEGFR、mTOR不算严格的靶向药靶点,毒性也偏大。但了解到肾细胞癌的治疗历史后,特别是在靶向药应用之前,化疗几乎没有作用,才逐渐对VEGFR TKI和mTOR靶点在肾癌上的积极作用有了崭新的认识。
肾细胞癌上有获得FDA批准较早的靶向药,且获批数量也最多。VEGFR及mTOR靶点抑制剂在肾细胞癌上的应答率明显好于其它肿瘤类型,极大的改善了肾细胞癌的劣质性。肾细胞癌上的靶向用药顺序、间歇给药、组合疗法等都在引领肿瘤疗法的未来。
参考文献
1. New strategies in renal cell carcinoma: targeting the genetic and metabolic basis of disease. Srinivasan R, et al. Clin Cancer Res. 2015;21(1):10–7.
2. Identification of the von Hippel-Lindau disease tumor suppressor gene. Latif F, et al. Science. 1993;260 (5112):1317–20.
3. The von Hippel-Lindau tumor suppressor protein and clear cell renal carcinoma. Kaelin WG, Jr. Clin Cancer Res.2007;13:680s-84s.
4. Sunitinib in patients with metastatic renal cellcarcinoma. Motzer RJ, et al. JAMA. 2006;295 (21):2516–24.
5. Sunitinib versus interferon alfa in metastatic renal-cell carcinoma. Motzer RJ, Hutson TE, Tomczak P, et al. N Engl J Med.2007;356:115-24.
6. Pazopanib in locally advanced or metastatic renal cell carcinoma: results of a randomized phase III trial. Sternberg CN, etal. J Clin Oncol. 2010;28(6):1061–8.
7. 靶向巨噬细胞的肿瘤药物研发进展,药时代,2017-07-19。
8. New treatment options for metastatic renal cell carcinoma with prior anti-angiogenesis therapy. Zarrabi K, Fang C, Wu S. J Hematol Oncol. 2017 Feb 2;10(1):38.
9. Hypertension as a biomarker of efficacy in patients with metastatic renal cell carcinoma treated with sunitinib. Rini BI,Cohen DP, Lu DR, et al. J Natl Cancer Inst. 2011, 103(9):763-73.
10. Nivolumab for metastatic renal cell carcinoma: results of a randomized phase II trial. Motzer RJ, et al. J Clin Oncol.2015;33(13):1430–7.
11. Nivolumab versus everolimus in advanced renal-cell carcinoma. Motzer RJ, et al. N Engl J Med. 2015;373(19):1803–13.
12. Long-term overall survival (OS) with nivolumab in previously treated patients with advanced renal cell carcinoma (aRCC) from phase I and II studies. McDermott DF. In 2016 ASCO Annual Meeting. 2016.
13. A phase 1b clinical trial of the multi-targeted tyrosine kinase inhibitor lenvatinib (E7080) in combination with everolimus for treatment of metastatic renal cell carcinoma (RCC). Molina AM, et al. Cancer Chemother Pharmacol.2014;73(1):181–9.
14. A Phase II Study of Intermittent Sunitinib in Previously Untreated Patients With Metastatic Renal Cell Carcinoma. Ornstein MC, Wood LS, Elson P, et.al. J Clin Oncol. 2017 Jun 1;35(16):1764-1769.
来源:药时代(微信号 DrugTimes) 作者:紫薯
为你推荐
 资讯
资讯 Cytiva推出全新一次性超滤系统 ÄKTA readyflux TFF 500,赋能先进疗法研发与小规模生产
以更灵活、多元的ÄKTA 产品组合,满足行业在先进治疗药物开发领域
2025-07-29 16:39
 资讯
资讯 爱尔眼科联合行业多方发起“三正规”倡议 对假货“零容忍”
儿童青少年近视防控已成为关乎国家未来的重要民生课题。然而,当前市场上假冒伪劣近视防控产品屡见不鲜,不仅无法起到防控效果,更可能加剧视力恶化。
文/陈炜 2025-07-29 16:20
 资讯
资讯 外用制剂领域再突破 MC2-01乳膏治疗中国斑块状银屑病的Ⅲ期临床试验获批
杭州中美华东制药有限公司开发的MC2-01乳膏,用于治疗中国斑块状银屑病的Ⅲ期临床试验申请已正式获得国家药品监督管理局批准
2025-07-28 18:18
 资讯
资讯 欧盟批准含Blenrep(注射用玛贝兰妥单抗)的联合治疗方案用于治疗复发或难治多发性骨髓瘤
葛兰素史克(LSE NYSE:GSK)7月24日宣布,Blenrep已获得欧盟(EU)批准,用于以下适应症:联合硼替佐米和地塞米松(BVd),用于既往接受过至少一线治疗的复发或难治多发性骨髓...
2025-07-28 16:08
 资讯
资讯 欧狄沃联合逸沃获批成为中国首个非小细胞肺癌一线双免疫疗法
今日(7月28日),百时美施贵宝宣布,欧狄沃®(纳武利尤单抗注射液)联合逸沃®(伊匹木单抗注射液)方案获得中国国家药品监督管理局(NMPA)批准。
2025-07-28 15:58
 资讯
资讯 橙帆医药完成超6000万美元Pre-A+轮融资,加速全球首创新药管线临床开发
2025年7月28日,专注多抗与ADC药物研发的创新企业橙帆医药宣布完成超6000万美元Pre-A+轮融资。本轮融资由顺为资本领投,北极光创投、汉康资
2025-07-28 09:21
 资讯
资讯 Lenacapavir“零时差”落地乐城,我国HIV防控迈入长效预防新时代
2025年7月25日,全球同类首创、一年仅需给药两次的HIV暴露前预防药物Lenacapavir(来那帕韦)正式落地海南博鳌乐城国际医疗旅游先行区
2025-07-27 10:35
 资讯
资讯 国家卫健委:医养结合示范项目工作方案(2025年版)
全国医养结合示范机构。具备医疗卫生机构资质,依法进行养老机构备案的医疗卫生机构或养老机构。示范机构每2年评估一次,每次命名100个左右(含中医药特色的示范机构),2030年...
2025-07-26 17:05
 资讯
资讯 CDE :化学药品口溶膜剂药学研究技术指导原则(试行)
膜剂是指原料药物与适宜成膜材料等经加工制成的膜状制剂,根据给药部位不同,可分为口用膜、眼用膜、阴道膜等。口用膜可分为口溶膜、口颊膜、舌下膜和口腔贴膜。口溶膜是指在口...
2025-07-26 10:52
 资讯
资讯 CDE:12项生物类似药药学相似性研究的问题与解答
生物类似药进行临床试验申请时,对于生产工艺和规模的要求是什么?候选药的剂型、规格、 制剂处方是否必须与参照药一致?对参照药的来源如何要求?多规格制剂中是否可以选择一...
2025-07-26 10:40
 资讯
资讯 皮尔法伯集团毕太维®联合疗法在华获批,精准靶向BRAFV600E突变型转移性结直肠癌
用于既往接受过系统治疗的BRAFV600E突变型转移性结直肠癌(mCRC)成人患者。
2025-07-25 18:24
 资讯
资讯 《特殊医学用途流质配方食品注册指南》和《特殊医学用途增稠组件配方食品注册指南》
流质配方为非全营养配方食品,一般在短时间内使用,满足需要流质饮食和限制脂肪摄入人群的基本营养需求。
2025-07-25 17:15
 资讯
资讯 扬子江药业在固阳成功举办第二届717龙凤堂有机黄芪节
“健康中国”战略指引下,扬子江药业集团(以下简称扬子江)旗下中药品牌龙凤堂始终致力于全链条把控产品质量,从源头助力中药材产业发展水平提升。
2025-07-25 10:42
 资讯
资讯 国家市场监督管理总局禁止武汉用通收购山东华泰制药股权,要求解除
本案是2008年《中华人民共和国反垄断法》施行以来第四起禁止的经营者集中案件,是第一起对未达申报标准的经营者集中予以禁止的案件,也是首次要求相关方对已实施的集中采取措施...
2025-07-24 17:43
 资讯
资讯 1500万美元里程碑付款,一款国产双靶向CAR-T疗法出海
近日,科弈药业宣布,与美国生物医药企业ERIGEN LLC就其自研的全球首个并联增强型双靶向CAR-T细胞治疗产品KQ-2003(靶向BCMA CD19)的独家海外授权许可达成战略合作。
2025-07-24 14:28
 资讯
资讯 AQ健康数据警示:暑期割包皮咨询量翻5倍 非必要不手术
随着暑期到来,全国多家医院小儿泌尿外科门诊迎来就诊高峰。部分医院暑期预期手术量甚至高达4000多台,不少家长选择利用假期为孩子安排包皮手术咨询和预约。
2025-07-24 12:00