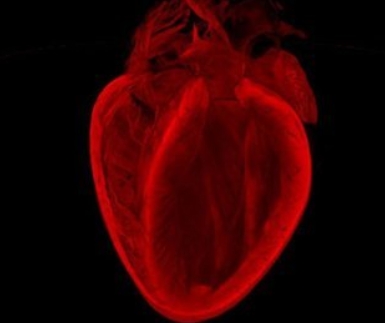
研究药物
Nivolumab注射液,是百时美施贵宝公司(Bristol-Myers Squibb)开发的抗癌免疫药,它是一种抗PD-1单克隆抗体,属于免疫检查点抑制剂。研究适应症:胃癌(GC)或胃食管交界处癌(GEJ)。
研究标题
Nivolumab+Ipilimumab(伊匹木单抗)或nivolumab+化疗对比化疗治疗既往未接受过治疗的晚期或转移性胃癌或胃食管交界处癌受试者的随机化、开放性、III期研究。
研究目的
1.比较nivolumab联合伊匹木单抗或nivolumab联合奥沙利铂+氟嘧啶与奥沙利铂+氟嘧啶给药治疗肿瘤表达PD-L1的晚期或转移性GC或GEJ癌受试者的OS, PFS和症状恶化的时间(TTSD)。 2.比较nivolumab联合伊匹木单抗或nivolumab联合奥沙利铂+氟嘧啶与奥沙利铂+氟嘧啶给药治疗所有随机的晚期或转移性GC或GEJ癌受试者的OS, PFS和症状恶化的时间(TTSD)。
研究范围
本研究为国际多中心研究,本次招募计划,面向全球患者,国内有多家医疗机构(医院)参与,目标入组人数:总体1266人,中国203人。临床参加机构(医院),参见文末列表。
主要入选标准:
1.年龄≥18岁确诊为无法手术治疗的晚期或转移性胃癌或胃食管交界处癌患者;
2.既往没有接受过针对晚期或转移性癌症的全身治疗;
3.既往如有围手术期化疗、放疗或化放疗的,必须在随机入组前至少6个月已完成;
4.既往如有姑息性放疗的,必须在随机入组前2周已完成;
5.体力状况较好,ECOG PS评分为0-1;
(详细说明见下文,最终入选标准由医生评估)
本次临床招募和实施方案,已经在中国国家食品药品监督管理总局登记注册(注册号:CTR20170371)。按照方案规定,入选患者将随机分配接受:
nivolumab联合伊匹木单抗(研究组),或
nivolumab联合奥沙利铂+氟嘧啶(研究组),或
奥沙利铂+氟嘧啶(对照组)
考虑参与或有兴趣了解有关研究信息,请访问文末网址链接,获得更多详情。符合所有合格性条件(包括入选和排除标准)的患者,在参与临床研究过程中,将可获得免费的研究相关检查和治疗。咨询方式,参见文末的研究人员和医疗机构(医院)信息。
本次招募的入选标准包括:
主要研究者信息:
负责人:沈琳 主任医师
单位名称:北京肿瘤医院
(其他主要研究者,参见下表)
临床参加机构(医院)信息:
来源:e药环球
为你推荐
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34
 资讯
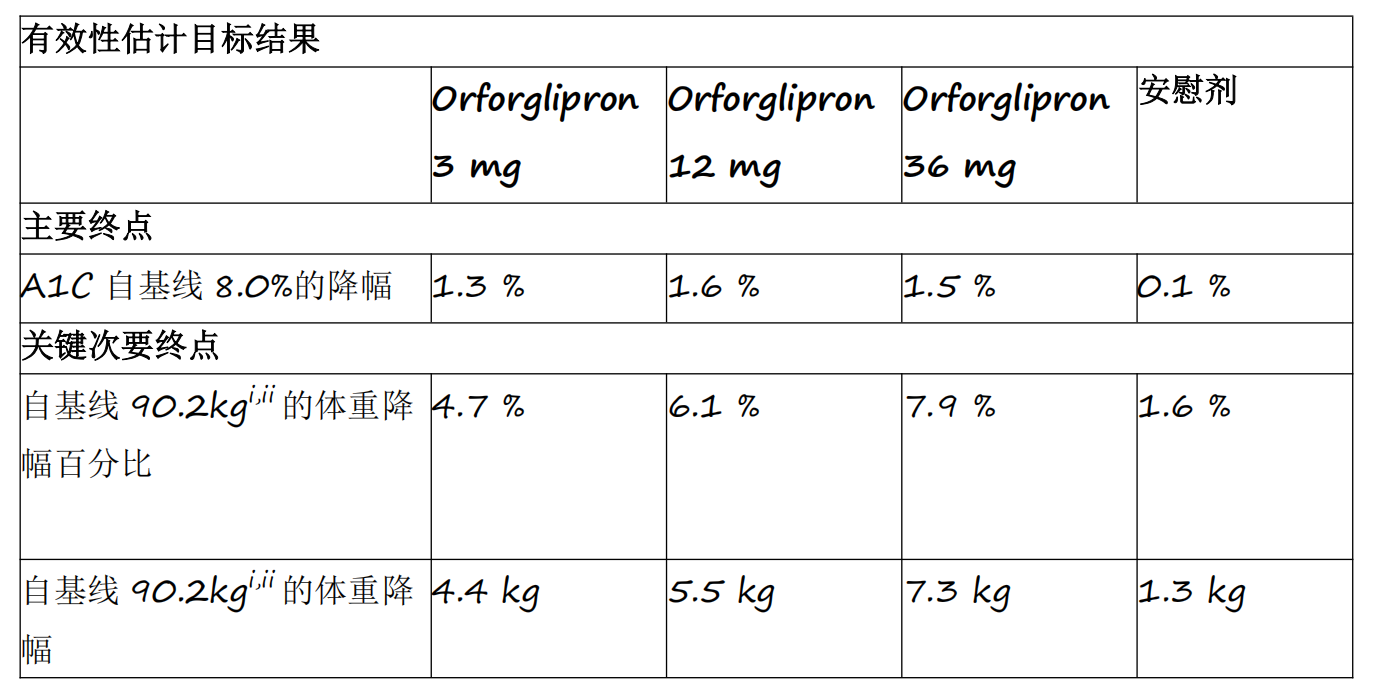
资讯 礼来首个小分子口服GLP-1RA药物orforglipron 3期临床研究成功
Orforglipron是首个成功完成3期临床研究的小分子GLP-1类药物,各剂量组平均A1C降幅为1 3%至1 6%
2025-04-18 14:12
 资讯
资讯 WSOPRAS 2025落幕:中国眼整形闪耀国际舞台,李冬梅教授代表爱尔眼科获2027年大会主办权
4月10日至12日,世界眼整形重建外科学会(WSOPRAS)2025年国际峰会在土耳其伊斯坦布尔盛大举行。
文/李林 2025-04-18 09:27
 资讯
资讯 华东医药2024年报出炉,营收超400亿,创新产品密集上市
报告显示,2024年公司合计实现营业收入419 06亿元,同比增长3 16%;实现归母净利润35 12亿元,同比增长23 72%,实现扣非归母净利润33 52亿元,同比增长22 48%。
2025-04-17 21:18
 资讯
资讯 讯飞医疗与爱奥乐医疗联合首发AI血压计,开启高血压管理新时代
4月11日,在备受瞩目的乌镇健康大会上,讯飞医疗与爱奥乐医疗联合首发AI血压计,作为行业首款搭载医疗大模型的AI血压计,引领家用医疗器械从单一检测工具进化为全周期健康管理解...
2025-04-17 20:34
 资讯
资讯 又一款常用药物被暂停采购资格
近日,上海阳光采购网发布通知,因未按要求调整药价,自2025年4月15日24时起暂停仁和堂药业有限公司盐酸地芬尼多片(25mg*12片 板 盒,铝塑)采购资格。
2025-04-17 15:29
 资讯
资讯 超16亿元,达仁堂“清仓”中美史克
日前,达仁堂发布公告称,公司拟分别向赫力昂(中国)、Haleon CH SARL(简称“赫力昂(英国))转让所持有的中美天津史克制药有限公司(简称“中美史克”)4 6%股权份额、7...
2025-04-17 15:08
 资讯
资讯 上海发布10款重点监控品种
根据上海此前发布的相关规则,医疗机构根据市场供需情况在阳光采购平台采购药品是,“红黄绿线”议价将实时提醒采购产品的价格是否存在问题,从而保证临床需求,并避免不合理调价。
2025-04-16 22:15
 资讯
资讯 马斯克称今年将首次在人体植入“盲视”设备,让失明者重见光明
4月初,马斯克在多个场合宣布,公司计划于今年底首次在人体内植入名为“Blindsight(盲视)”的脑机接口设备,目标是让完全失明者重见光明。
2025-04-16 14:28
 资讯
资讯 诺令生物完成数亿元人民币C轮融资,加速出海步伐和多元化产品布局
本轮融资将主要用于核心产品“便携式一氧化氮(NO)吸入治疗仪”的产能扩充、全球化推广,以及围绕NO缓释与发生技术的创新管线研发
2025-04-15 17:12
 资讯
资讯 扬帆出海正当时:Cytiva 为中国生物药企绘制全球合规航海图
峰会聚焦法规解读、国际监管环境、中国生物药企业出海案例等关键议题,通过专家分享和深入解读,为中国生物药企提供全球化战略指导和合规支持;
2025-04-15 17:00
 资讯
资讯 全国肿瘤防治宣传周:礼来携手信达生物、和黄医药加速赋能本土医药创新
礼来携手本土合作伙伴信达生物、和黄医药齐聚上海,共话本土医药创新发展,探索加速惠及中国肿瘤患者的新模式
2025-04-15 16:27
 资讯
资讯 ADC明星企业映恩生物港交所上市,开盘高开91.33%
上市首日,其股价开盘高开91 33%,随后涨幅迅速扩大至127 06%,午间收报214 80港元,市值突破178 66亿港元,成为近年来港股18A生物科技公司中最亮眼的IPO案例之一。
2025-04-15 13:19