背景
肺癌是全球癌症死亡的主要原因。肺癌主要分为小细胞肺癌和非小细胞肺癌(non-small cell lung cancer,NSCLC),其中NSCLC约占80%,多数诊断为晚期(局部晚期或转移性疾病)。NSCLC患者5年的存活率低于5%,在英国,每100例肺癌中就有87例(87%)为非小细胞肺癌(NSCLC)。NSCLC有三种常见的类型,腺癌,鳞状细胞癌和大细胞癌。将他们分在一组,是因为它们具有相似的表现形式,可以采用相同的治疗方式(cancer research uk)。至于采用何种方式治疗NSCLC,需要看疾病发展到哪个阶段,对于早期NSCLC的治疗主要手段为手术。对于Ⅱ期和Ⅲ期NSCLC,之前采用全身性化疗的方式,患者的生存期和生活质量均得到了明显改善。
在过去几年中,人们发现,肿瘤的生长与表皮生长因子受体(EGFR)在肿瘤细胞中的过度表达相关,基于此,第一代EGFR酪氨酸激酶抑制剂(EGFR-TKIs)吉非替尼诞生了,对突变基因的检测也表明了个性化医疗时代的到来,晚期NSCLC的治疗方式从此发生了重大变化。
NSCLC患者中,北美和欧洲患者EGFR突变的发生率占10-17%,亚洲国家占30%-50%。而一般发生的EGFR突变多为经典突变,即在外显子19有缺失突变(del19)或外显子21中的Leu858Arg (L858R)点突变,或二者兼有(即共同的突变)。这两种突变占据了所有EGFR突变NSCLC患者的85%-90%,部分患者(10%)的EGFR突变肿瘤隐藏有罕见的突变[1]。这种经典EGFR突变的概率和种族有一定关系。事实上,一些大型(EGFR基因分型)的前瞻性研究表明,在欧洲患者中,与L858R突变相比,del19突变的频率更高,而与欧洲患者相比,del19突变的发生率在亚洲患者中略高一些。更有趣的是,一项临床研究发现,与携带L858R突变的患者相比,携带del19突变的患者对可逆性EGFR-TKI更加敏感[2]。与化疗药物相比,靶向药物的毒副作用更低,不会产生骨髓抑制,这也使靶向药物在临床得到了广泛应用。
三代EGFR-TKI的特点及应用
对于无驱动基因的局部晚期或转移性NSCLC患者,推荐的标准化疗方案为铂类联合三代化疗药物,包括长春瑞滨,吉西他滨,紫杉醇,多西他赛或培美曲塞。对于EGFR驱动突变的局部晚期或转移性NSCLC患者,使用靶向药物EGFR-TKI作为一线的治疗药物。
第一代的EGFR-TKI靶向药
特罗凯(厄洛替尼)、易瑞沙(吉非替尼,ZD1839)、凯美纳等属于第一代的EGFR-TKI靶向药,即表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)。这些药物专门针对外显子19、21发生突变进行治疗。吉非替尼,是全球首个EGFR-TKI抑制剂,2002年在日本获批。在携带EGFR突变的晚期NSCLC患者中,使用EGFR-TKI在反应率,无进展生存期和生活质量方面均明显优于基于铂剂的化学疗法,(对于晚期的NSCLC患者一线化疗药物一般为铂系,只有30-40%的患者达到PR,平均总生存期为8-11个月),为晚期NSCLC患者提供了一种新的选择方式。
最初的临床试验研究了ZD1839用于实体瘤患者的药代动力学、耐受性和疗效。研究结果表明,ZD1839的副作用很小。最常见的1、2级不良事件为痤疮形式皮疹、恶心和腹泻,剂量限制性毒性为腹泻,当日剂量达到700mg时观察到DLT,明显高于有效剂量,而且在临床表现中并不常见。
药动学试验表明,ZD1839每日给药一次的方案是合适的[3]。在随后的一项随机、双盲、平行的二期临床试验中,再次研究了ZD1839的耐受性和安全性,入组病例为先前接受过至少一个或者两个化疗药物治疗的晚期非小细胞肺癌患者(至少一个为铂剂),研究者以2:1的比例将上述受试者随机分为两组,一组接受口服吉非替尼治疗,500mg PO QD;另一组接受口服吉非替尼治疗,250mg PO QD。实验结果表明,两组疗效相似,客观缓解率分别为18.4% (95%Cl,11.5-27.3)和19.0 (95%Cl,12.1-27.9),中位PFS分别为2.7和2.8个月,中位OS分别为7.8和8个月,两组剂量水平相关的不良事件均为轻度,主要为皮肤反应和腹泻。所以,吉非替尼可以作为治疗NSCLC患者的二线药物或者三线药物[4]。
早期III期研究比较了吉非替尼、厄洛替尼与安慰剂对化疗失败的NSCLC的治疗,接受EGFR-TKI的个体生存均得到了改善,吉非替尼对亚洲患者和无吸烟史的患者效果更佳。而欧洲和美国也基于BR.21试验给予了厄洛替尼化疗失败的晚期NSCLC的二线或三线药物的资格。IPASS (NCT00322452)临床研究结果显示,对于既往无吸烟史或有轻度吸烟史的亚洲肺腺癌患者一线治疗中,吉非替尼与卡铂/紫杉醇方案相比,可显著延长患者的无进展生存[5] (PFS,研究主要终点)。其中对意向治疗总体人群及EFGR突变呈阳性患者亚组的无进展生存都有延长。不幸的是,大约三分之一的EGFR突变患者显示出对吉非替尼或厄洛替尼的初次耐药,而几乎所有最初受益于治疗的患者最终都会发展成获得性耐药。绝大部分患者经EGFR-TKI一线治疗9-13个月后即出现疾病进展。
研究发现,吉非替尼原发性耐药与外显子20的插入突变相关。与这些数据一致,大多数携带外显子20插入突变的肿瘤患者已被证明对吉非替尼具有耐药性[6]。至于获得性耐药,在约50%的患者中,归因于位于“关键”的EGFR基因的20外显子第790位点上的密码子的错义突变(T790M),致使蛋氨酸(M)取代了原本处于相应位置的苏氨酸(T),也就是T790M突变。这种突变诱导产生吉非替尼或厄洛替尼耐药的方式被认为是由于EGFR和ATP之间的结合亲和力增加而不是EGFR和EGFR-TKI之间的亲和力降低[7]。另一种耐药模式认为:TKI治疗前的NSCLC患者存在T790M突变的微小克隆,经TKI治疗后,敏感克隆被杀死,而含有T790M突变的耐药克隆得以保留下来,产生耐药。后期发现,接受第一代EGFR-TKIs患者的获得性耐药还与另外三个较不常见的二次突变相关,即D761Y(外显子19),L747S(外显子19)和T854A(外显子21)突变。
第二代EGFR-TKI靶向药
第二代EGFR-TKI靶向药有两种阿法替尼与达克替尼,具有代表性的为阿法替尼。该药物的获批来自关键性LUX-Lung 3试验的数据,这是一个涉及EGFR突变阳性肺癌患者的最大规模的全球性III期临床试验,旨在比较阿法替尼与培美曲塞/顺铂联合化疗的效果。
来自LUX-Lung 3研究的数据显示,接受阿法替尼作为一线治疗的患者在肿瘤重新开始生长之前的生存时间达到了一年[中位无进展生存期(PFS)为11.1个月],而接受培美曲塞/顺铂的患者则稍超过半年(PFS为6.9个月)。
值得注意的是,携带两种最常见EGFR突变类型(Del19或L858R,占所有EGFR突变类型的90%)的NSCLC患者在接受阿法替尼后的无进展生存期远远超过了一年(PFS为13.6个月),而对照组患者则稍超过半年(PFS为6.9个月)。该药物于2013年7月12日获美国食品及药物管理局(FDA)核准上市,作为新型一线治疗药物,应用于通过经FDA批准的检测方法检出存在表皮生长因子受体(EGFR)外显子19缺失突变或外显子21 (L858R)替代突变的转移性非小细胞肺癌(NSCLC)患者。中华民国行政院卫生署食品药物管理局(TFDA)亦早于2013年5月17日抢先核准阿法替尼药物上市。
第二代靶向药针对的主要EGFR基因位点与第一代相比没有区别,在临床实际运用过程中,其疗效并没有优于第一代的靶向药,LUX-Lung 8是一项多中心随机开放对照三期临床试验,研究在分布于23个国家的183个癌症中心进行,入组的病例为经过铂剂化疗四个周期病情出现进展的鳞状细胞癌(非小细胞肺癌的一种组织学亚型)的成年人,其疾病分期为IIIB期或IV期。按1:1的比例将参与者随机分为两组,一组接受阿法替尼,40mg PO QD;另一组接受厄洛替尼,150mg PO QD。主要终点是(意向治疗人群)的无进展生存期,次要终点是总生存期。研究表明,与厄洛替尼相比,阿法替尼无进展生存期和总体生存期显着改善,两者三级以上的不良事件发生率相似。
LUX-Lung 7试验是全球首个头对头比较阿法替尼和吉非替尼作为一线药物用于EGFR突变(Del19或L858R)阳性的NSCLC患者的二期临床试验,该试验的主要复合终点为独立审查无进展生存期(PFS)、以及至治疗失败时间(TTF)和总生存期(OS),次要终点包括客观有效率、疾病控制率、肿瘤体积缩小、患者报告的结局与安全性。该研究共入组319例(13个国家,64个中心)携带常见EGFR突变(Del19或L858R)的晚期NSCLC患者。入组的患者中一半以上是亚洲患者,95%以上都是IV期患者,两组发生Del19突变患者占58%,L858R突变患者占42%,入组患者以1:1的比例接受每日口服阿法替尼40mg或每日口服吉非替尼250mg。研究结果显示与吉非替尼相比,阿法替尼显著降低肺癌进展风险27%和治疗失败风险(HR,0.73,TTF,13.7个月vs 11.5个月),关于OS,据最新的统计结果,与吉非替尼相比,阿法替尼治疗有改善OS的趋势,但未达到统计学意义[8]。最常见的治疗相关的3级或4的不良反应为腹泻(阿法替尼:13% VS 吉非替尼:1%)和皮疹或痤疮(阿法替尼:9% vs吉非替尼:3%)和肝酶升高(阿法替尼:无VS吉非替尼:9%)。与治疗相关的严重的不良事件发生率分别为11%(阿法替尼组)和4%(吉非替尼组)。由于药物相关的不良事件,两组治疗相关停药事件发生率较低,均为6%。
第三代EGFR-TKI靶向药
AZD9291,又叫Osimertinib,是第三代EGFR TKI。该化合物是不可逆突变体选择性EGFR TKI(外显子19缺失型EGFRIC50=12.92nM,L858R/T790M EGFR IC50=11.44nM,野生型EGFR IC50=493.8nM)。
AZD9291是第一个批准的用于EGFR T790M突变阳性NSCLC患者的EGFR TKI。在一项三期、随机、开放的国际多中心临床研究中,对Osimertinib和化疗双药治疗T790M突变的肺腺癌患者的疗效进行了研究。该项研究入组了419位经过一线EGFR-TKI药物的治疗产生了T790M突变的肺腺癌患者,研究者将参与者以2:1的比例随机分为两组,一组接受Osimertinib口服治疗(80mg,PO QD),另一组接受培美曲塞(500mg/m2)加卡铂(AUC取值为5)或者顺铂(75mg/m2)治疗。使用Osimertinib治疗T790M突变的肺腺癌患者的中位PFS明显高于铂加培美曲塞组(10.1个月 vs 4.4个月;HR:0.30;95%CI:0.23-0.41;P<0.001)。Osimertinib组(71%;95%CI,65-76%)的客观缓解率明显优于铂加培美曲塞组(31%;95%CI,24-40%)。在144例转移至中枢神经系统(CNS)的患者中,接受Osimertinib治疗的患者的无进展生存期的中位持续时间长于接受铂加培美曲塞的患者(8.5个月 vs 4.2个月;风险比为0.32;95%CI,0.21-0.49)。上述结果表明,与化疗相比,Osimertinib可以成为经一线EGFR-TKI药物治疗产生了T790M突变的肺腺癌患者的另一种更佳的选择[9]。
目前,另一项比较Osimertinib与吉非替尼或厄洛替尼作为一线药物治疗EGFR突变NSCLC (NCT02296125)患者的III期研究正在进行。患者在对照组疾病进展后允许被交叉到AZD9291组。根据OncLive非小细胞肺癌高端科学峰会的讨论结果,AZD9291将会转型为一线治疗药物,虽然这些消息听起来很让人振奋,但仍然要面对一个残酷的问题,AZD9291也会产生耐药,C797S突变是最常见的类型,T790M患者在经AZD9291治疗5-17个月后便会出现C797S突变引起耐药[10]。
小结
介绍过这三代药物以后,说说我个人的看法,(据二期临床实验的研究)与第一代药物相比,虽然阿法替尼在疗效上有一定的优势,但不良事件方面,现有的数据表明吉非替尼低于阿法替尼,关键的是,第一代靶向药出现耐药后,第二代EGFR-TKI靶向药并不能解决耐药问题,这会大大限制其临床使用。再从另一个角度出发,吉非替尼在中国的结构专利(喹唑啉衍生物,专利号:ZL96193526.X)及厄洛替尼在中国的结构专利(喹唑啉衍生物,专利号:ZL96102992.7)的保护期分别于2016年4月23日及2016年3月28日到期。所以,目前国内已有两家企业(齐鲁制药,齐鲁安替)拿到吉非替尼仿制药生产批文。国产吉非替尼(伊瑞可)在2017年已经进入国家医保,大大增加了药品的可及性,而价格仅为1680元(进口易瑞沙为5400元),优质仿制药的介入和价格因素也构成了与阿法替尼及其他一代药物的市场竞争。纽约纪念斯隆凯特林癌症中心(MSKCC)医学专家Jamie E参加了2017年OncLive非小细胞肺癌高端科学峰会,会后接受了采访并分享了关于肺癌中可用的EGFR TKIs的见解:我们讨论了第一代与第二代药物哪个更具有优势。基于我对数据的理解,第二代药物阿法替尼(Gilotrif)具有更高的毒性,并且没有比第一代药物更明显的治疗优势。
以上内容引自原文如下:
What are the current challenges we face with sequencing therapies,if any?
Today,there is not much of a challenge. The treatment algorithm is fairly obvious,in terms of approvals. The third-generation drug will follow either a first- or second-line agent.
At this meeting,we talked about the controversy over the superiority of first- versus second-generation drugs. My interpretation of the data is that the second-generation drug afatinib (Gilotrif) has more toxicity and does not have an obvious therapeutic advantage over the first-generation drugs.)。
关于AZD9291,由于EGFR T790M突变存在于约50-60%的耐药病例中,而根据目前公开的信息,此药物进军一线治疗药物的可能性极大,所以,未来的市场空间很大。可是如果把第三代EGFR-TKI当做第一代用,也存在一些问题。例如当第三代TKI出现耐药后,我们后续治疗还能有哪些药物可用?而且,使用AZD9291的治疗费用一年大概需要20几万,是很多普通的家庭承受不起的。以经济实用的角度来考虑,当基因检测为L858R或者del19突变时,首先选择吉非替尼做为一线药物治疗,出现T790M耐药以后,再选择AZD9291来治疗,这样的治疗方式貌似更合理一些。
参考文献
1.Winton T,Johnson D,et al. Vinorelbine plus cisplatin vs. observation in resected non-small-cell lung cancer. N Engl J Med 2005;352:2589–2597.
2.Ranson M,et al. ZD1839, a selective oral epidermal growth factor receptor-tyrosine kinase inhibitor,is well tolerated and active in patients with solid,malignant tumors: results of a phase I trial. J Clin Oncol 2002;20:2240-50.
3.Ramalingam S,Belani C. Systemic chemotherapy for advanced non-small cell lung cancer: recent advances and future directions. Oncologist 2008;13:5-13
4.Valentina Guarneri,et al. Multi-institutional randomized phase II trial of gefitinibfor previously treated patients with advanced non-small-cell lung cancer. J Clin Oncol. 2003; 21 (12):2237-46.
5.WuYL, et al.Tumor response and health-related quality of life in clinically selected patients from Asia with advanced non-small-cell lung cancer treated with first-line gefitinib: post hoc analyses from the IPASS study. Lung Cancer2013.Aug;81 (2):280-7
6.Wu JY,Wu SG,Yang CH,etal. Lung cancer with epidermal growth factor receptor exon 20 mutations is associated with poor gefitinib treatment response. Clin Cancer Res 2008;14:4877-82.
7.Yun CH,Toms AV,et al. The T790M mutation in EGFR kinase causes drug resistance by increasing the affinity for ATP. Proc Natl Acad Sci U S A 2008;105:2070-5
8.L. Paz-Ares,et al. Afatinib versus gefitinib in patients with EGFR mutation-positive advanced non-small-cell lung cancer:overall survival data from the phase IIb LUX-Lung 7 trial. Ann Oncol. 2017 Feb;28 (2): 270–277.
9.TonyS. Mok,M.D, et al.Osimertinib or Platinum–Pemetrexed in EGFR T790M–Positive Lung Cancer.N Engl J Med 2017; 376:629-640
10.Niederst MJ, Garcia AR, et al. Piotrowska Z, Sequist LV, Engelman JA. The allelic context of the C797S mutation acquired upon treatment with third-generation EGFR inhibitors impacts sensitivity to subsequent treatment strategies. Clin Cancer Res. 2015;21 (17):3924–33.
来源:药渡(微信号 Pharmacodia) 作者:郭晶涛
为你推荐
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34
 资讯
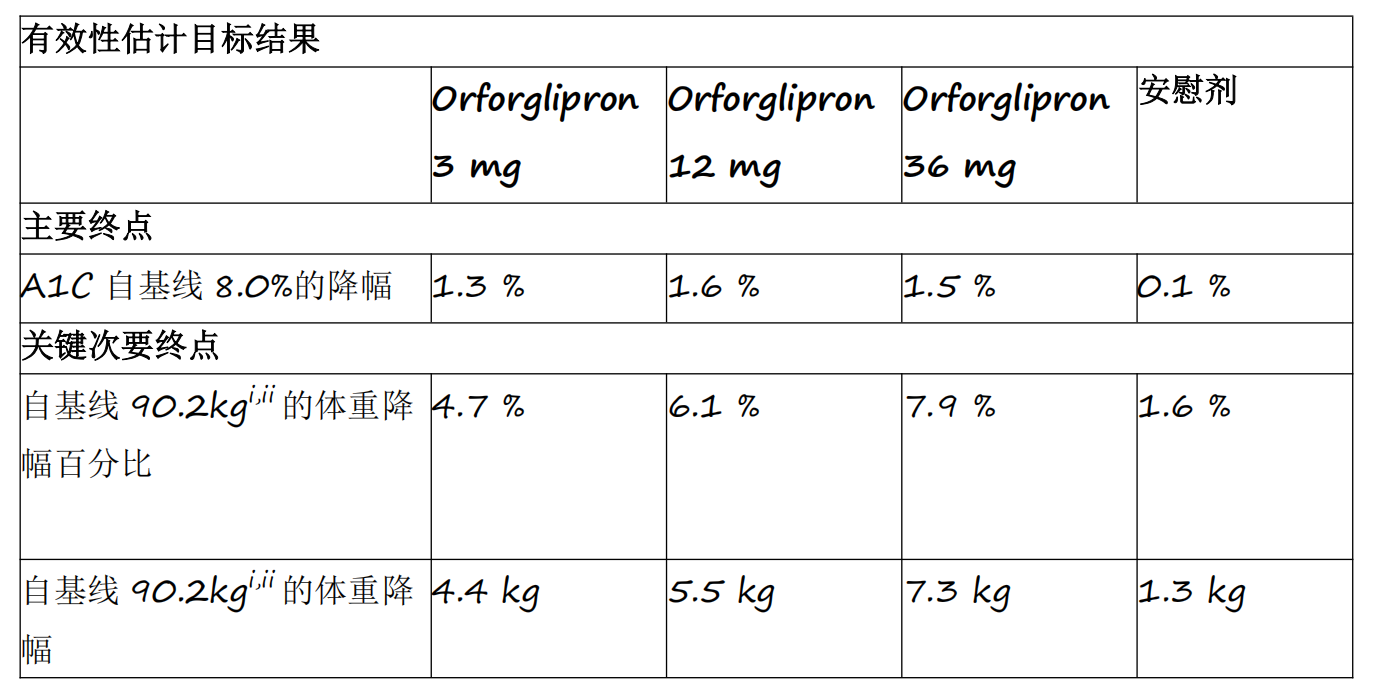
资讯 礼来首个小分子口服GLP-1RA药物orforglipron 3期临床研究成功
Orforglipron是首个成功完成3期临床研究的小分子GLP-1类药物,各剂量组平均A1C降幅为1 3%至1 6%
2025-04-18 14:12
 资讯
资讯 WSOPRAS 2025落幕:中国眼整形闪耀国际舞台,李冬梅教授代表爱尔眼科获2027年大会主办权
4月10日至12日,世界眼整形重建外科学会(WSOPRAS)2025年国际峰会在土耳其伊斯坦布尔盛大举行。
文/李林 2025-04-18 09:27









