最近,默沙东生产免疫明星药Keytruda的喜讯频频传出,之前,该药已被FDA批准用于治疗黑色素瘤、肺癌和头颈癌等癌症适应症。3月16日,该药用于治疗难治性或复发性经典霍奇金淋巴瘤的治疗获FDA批准;5月8日,同一适应症获欧盟批准;同月,该药适应症扩大到局部晚期或转移性尿路上皮癌的一线治疗获得FDA的批准。然而,Keytruda更“威猛”的用途得到了FDA的优先许可。
昨日(5月23日),FDA官网宣布,由默沙东公司(MSD)研发的免疫疗法明星药Keytruda (pembrolizumab)获得FDA加速批准,用于成人和儿童特定癌症基因特征(生物标志物)的广谱实体瘤的治疗。这也是FDA首次批准基于共同生物标志物的癌症治疗,而不受肿瘤起源身体哪个部位的限制。
据FDA官网显示,此次获批的该款药物Keytruda (pembrolizumab)是针对患有不可切除或转移性实体瘤的成人或儿童患者,其肿瘤中确定含有微卫星不稳定性高(microsatellite instability-high,MSI-H)或错配修复缺陷(mismatch repair deficient,dMMR)的生物标志物。这一指标涵盖了在先前治疗后取得进展的实体瘤患者,和没有令人满意的替代治疗方案的患者以及在接受过某些化疗药物治疗后病情有所改善结直肠癌的患者人群。
在所有含有MSI-H 和 dMMR两种异常生物标志物的肿瘤当中,细胞内的DNA正常修复都会受到影响。这两种生物标志物最常见于大肠癌、子宫内膜癌和胃癌,但是也极少数存在于乳腺癌、前列腺癌、膀胱癌、甲状腺癌等其它癌症。大约5%的转移性结直肠癌患者含有MSI-H 或 dMMR的肿瘤标志物。
Keytruda作为肿瘤免疫疗法中最为引人注目的药物之一,其作用机理是以一种人源化单克隆抗体有效阻断PD-1与配体PD-L1/PD-L2之间的结合,从而激活T淋巴细胞对肿瘤展开进攻。
KEYTRUDA与免疫系统展开合作的示意图 来源默沙东官网
为了验证Keytruda治疗携带MSI-H或者dMMR实体瘤患者的有效性和安全性,研究团队开展了5项临床试验,共招募了149名癌症患者,涉及15种肿瘤类型。其中,最常见的癌症是结直肠癌、子宫内膜癌和其它消化道癌症。他们每3周接受200毫克KEYTRUDA,或每两周接受每公斤体重10毫克KEYTRUDA的治疗,直至出现不可接受的毒性或是出现疾病进展。如果患者没有出现这些情况,治疗总时长上限则为24个月。从这149名受试患者的总体反应率((overall response rate)和持续时间(durability of response)的结果来看,39.6%的患者达到了完全或部分缓解。78%的患者药物响应持续了6个月或更长时间。
Keytruda的临床试验还在进一步的验证当中,受试者含有MSI-H或dMMR肿瘤的突变基因。FDA有望在接下来的六个月内完成对该药物的审批。
一位担任FDA药物评价与研究中心的血液和肿瘤药品开发办公室主任兼FDA肿瘤研究中心主管Richard Pazdur博士表示:“该款药物对于癌症领域的治疗是很重要的里程碑,”“截至目前,FDA批准的癌症治疗药物都基于发病部位,比如,肺癌、乳腺癌。如今,我们正式批准了一种基于肿瘤标志物而不用考虑肿瘤的原始位置的药物。”
据美中药源形象的分析,目前,针对特定致癌基因的所谓“篮子试验”(basket trials)悄然兴起。这种针对致癌基因的治疗在一定程度上很容易理解。如同警察打击犯罪分子,小偷有小偷的治理办法、毒贩有毒贩的治理办法,这些办法应该和罪犯在纽约还是在北京关系不大。
之前,FDA已批准该款药物用于治疗某些转移性黑色素瘤、非小细胞肺癌、复发性或转移性头颈癌、难治性经典霍奇金淋巴瘤和尿路上皮癌多种适应症。
Keytruda的FDA批准历史
此次,Keytruda的获批得到了FDA的快速批准通道,这意味着FDA很可能会加速批准对尚未满足医疗需求的病种和显示具有某些特定疗效并可能会对病人的临床疗效有一定的预判的治疗药物,为其开辟“绿色通道”。
然而,FDA官网也特别注明了Keytruda 的常见副作用和不适宜人群,其中副作用包括疲劳、皮肤瘙痒、腹泻、食欲减退、皮疹、发热 (发热)、咳嗽、呼吸困难、肌肉骨骼疼痛、便秘和恶心。严重时会引起健康器官的炎症, 如肺部 (肺炎), 结肠 (结肠炎), 肝 (肝炎), 内分泌腺体炎症和肾脏 (肾炎)。不适宜人群包括病危患者或怀孕、哺乳期的妇女,这因为他可能对发育中的胎儿或新生儿造成伤害。在携带MSI-H生物标志物的中枢神经系统的癌症患儿中,Keytruda的疗效和安全性也尚未确定。
另据悉,默沙东同时宣布Keytruda用于三线治疗复发性或晚期胃癌、胃食管交界腺癌的补充申请(sBLA)已被FDA受理,并获得优先审评资格,预定审评时间(PDUFA)为2017年9月22日。
PD-1/PD-L1免疫疗法是当前备受瞩目的新一类抗癌免疫疗法,旨在利用人体自身的免疫系统抵御癌症,通过阻断PD-1/PD-L1信号通路,就如肿瘤细胞失去了护身符,裸身面对外界,从而遭受淋巴细胞的免疫袭击而使癌细胞死亡,具有治疗多种类型肿瘤的潜力,有望实质性改善患者总生存期(OS)。目前,各大巨头正在火速推进各自的临床项目,除了默沙东的Keytruda,还有百时美的Opdivo,罗氏的atezolizumab和阿斯利康的durvalumab(MEDI4736),据医药市场调研机构EvaluatePharma预测,Opdivo将成为PD-1/PD-L1领域最成功的免疫疗法,2020年销售额将达到88亿美元,而Keytruda也将达到55亿美元,罗氏atezolizumab为20亿美元。
原文检索
《FDA approves first cancer treatment for any solid tumor with a specific genetic feature》
为你推荐
 资讯
资讯 与国内公司达成新合作,开拓药业开始大力押注化妆品生意了?
近日,开拓药业发布公告称,其全资附属公司苏州开拓与杭州涂麦科技订立品牌与销售运营合作协议,两家公司将就开拓药业的化妆品,包括但不限于防脱、祛痘、美白等产品领域,开展...
2025-03-14 17:07
 资讯
资讯 38年研发突破,罗氏获批中国首个PIK3CA突变的靶向创新药伊赫莱,为乳腺癌患者带来新选择
2025年3月11日,中国国家药品监督管理局(NMPA)正式宣布批准了伊赫莱®(通用名:伊那利塞片)联合哌柏西利和氟维司群,适用于内分泌治疗耐药(包括在辅助内分泌治疗期间或之后...
2025-03-14 14:52
 资讯
资讯 BMS 2.86亿美元收购了一家CAR-T疗法公司
近日,百时美施贵宝(BMS)宣布将以每股5 00美元的全现金交易方式收购2seventy bio(TSVT US),总股本价值约为2 86亿美元,交易预计将在2025年第二季度完成。
2025-03-13 16:28
 资讯
资讯 启明医疗正式复牌:以长期主义开启高质量发展新阶段
此次复牌标志着启明医疗彻底解决了公司治理问题,并重新建立了内部控制体系,是公司回应市场关切、重塑行业信心的关键一步。
2025-03-13 09:13
 资讯
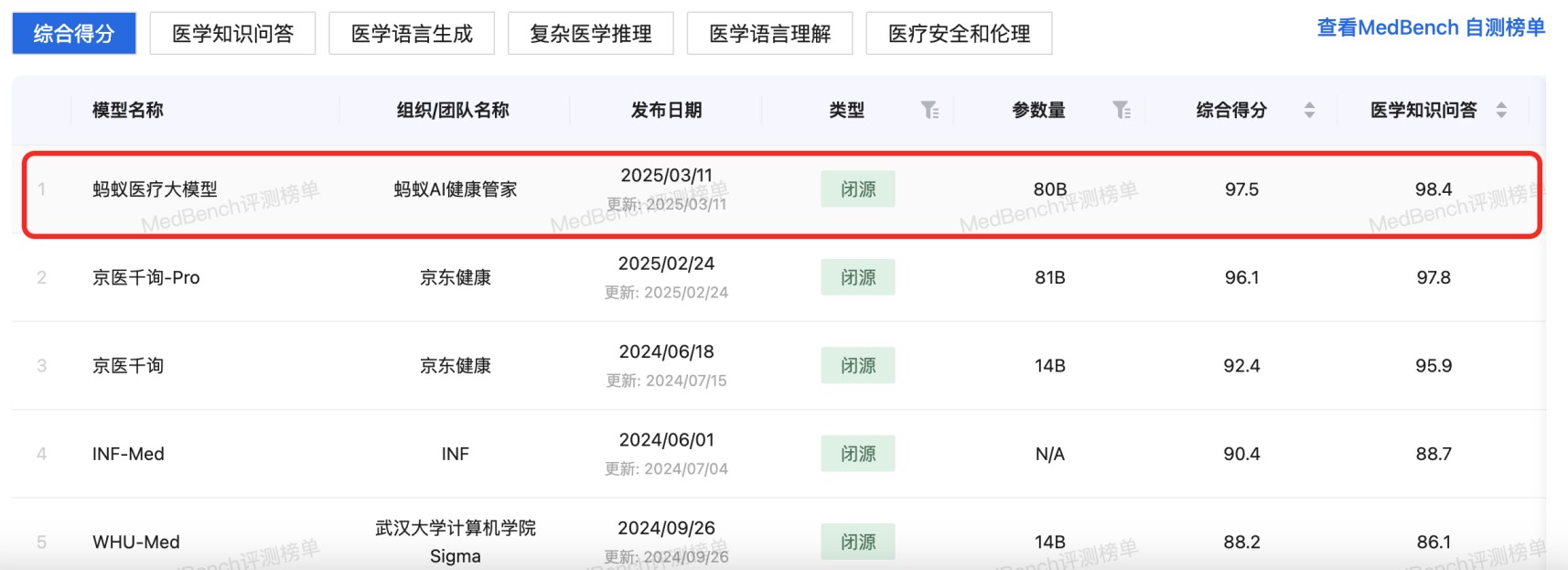
资讯 原生多模态+千亿级数据训练,蚂蚁医疗大模型拿下MedBench测评“双料”冠军
近日,记者发现,国内权威医疗大模型评测平台MedBench在官网更新了榜单。多个医疗AI产品及研究团队入榜,其中蚂蚁AI健康管家团队研发的蚂蚁医疗大模型以评测榜单97 5、自测榜单...
2025-03-12 15:47
 资讯
资讯 业绩增速持续承压,爱美客超13亿元收购了一家韩国医美公司
近日,爱美客发布公告称,基于公司战略规划和经营发展需要,其全资子公司 Imeik(HK)Limited(简称“爱美客香港”)与 Aisheng Shourui (HK) Limited(简称“首瑞香港”...
2025-03-12 10:47
 资讯
资讯 重见光明,聂爷爷的笑容回来了——重庆爱尔助孤寡白内障患者重燃生活希望
对于陈茂盛院长和重庆爱尔眼科医院(总院)的医护人员来说,聂爷爷的重见光明正是他们不断追求的动力。
2025-03-12 09:41
 资讯
资讯 无双医疗完成C轮近1.5亿元融资,加速心脏节律管理创新产品研发和商业化
本轮融资由天士力资本领投,现有股东启明创投、苏高新金控、康裕资本继续加持,为无双医疗在心脏节律管理(CRM)领域的创新产品研发和商业化进程注入了强劲动力。
2025-03-12 09:38
 资讯
资讯 卫美健康完成A轮亿级融资,加速县域基层医疗大模型应用落地
本轮融资资金将主要用于卫美健康“奇点医问”医疗大模型的研发投入与迭代进化,加强医疗细分领域的算法研究,构建升级全国服务网络体系,进一步扩大卫美健康在县域以及基层AI医...
2025-03-12 09:19
 资讯
资讯 突发,上市公司双成药业宣布终止跨界重组
昨日晚间(3月10日),双成药业发布公告称,公司原拟以发行股份及支付现金的方式向奥拉投资、Win Aiming等25名交易对方购买其持有的宁波奥拉半导体股份有限公司100%股份,并拟...
2025-03-11 13:44
 资讯
资讯 百时美施贵宝公布颂狄多®(氘可来昔替尼)POETYK PsA-2 III期试验最新数据 证实其在治疗成人银屑病关节炎中优于安慰剂
治疗第 16 周时,颂狄多治疗组患者的 ACR和 PASI应答率显著高于安慰剂组,且患者报告生活质量有更明显改善。与安慰剂和阿普米司特相比,颂狄多耐受性良好,安全性特征与既往...
2025-03-11 09:38
 资讯
资讯 华东医药全球首个卵巢癌ADC爱拉赫®补充申请获受理
申报适应症为用于既往接受过1-3线系统性治疗的叶酸受体α(FRα)阳性的铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌成年患者。
2025-03-10 19:36
 资讯
资讯 用于治疗复发或难治性多发性骨髓瘤,辉瑞靶向免疫疗法易瑞欧(埃纳妥单抗)在华获批
今日(3月10日),辉瑞公司宣布,靶向免疫疗法易瑞欧®(埃纳妥单抗)获国家药品监督管理局附条件批准,适用于既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂...
2025-03-10 12:07