5月22日消息,优时比(UCB)制药和安进制药公司表示,骨质疏松药物Romosozumab的临床3期研究ARCH达到了主要试验终点和关键次要终点。初步分析,相比较阿仑唑奈单药治疗,对于具有骨折高风险的绝经后骨质疏松女性患者,Romosozumab在治疗12个月后联合阿仑唑奈显著降低了新的椎体骨折发生率并达24个月之久,同时降低了临床骨折(主要终点)和非椎体骨折(关键次要终点)发生率。但是研究观察到了心血管严重不良反应裁定事件的不平衡(Romosozumab2.5% vs 阿仑唑奈1.9%)。
优时比公司首席医学官Iris Loew-Friedrich博士表示:“Romosozumab对于降低骨折风险是显著优于阿仑唑奈(现今骨质疏松症的标准治疗方法)的,并具有统计学意义。已经出现骨折的患者,其骨折后治疗的重要性还没有得到足够重视。我们将继续分析心血管不良事件的数据,并会同骨质疏松领域的专家和各国的审评机构就这些结果进行沟通。”
Romosozumab属于成骨制剂,可以快速增加骨形成并降低骨吸收;增加骨矿物质密度并降低骨折风险。ARCH研究中,女性患者接受一月一次的Romosozumab皮下注射并持续12个月,随后该患者会接受每周一次口服阿仑唑奈的治疗并持续12个月,在第24个月后,相比阿仑唑奈单药治疗,Romosozumab组患者的新脊柱骨折相对风险降低了50%;Romosozumab组患者临床骨折(非椎体骨折和临床脊柱骨折)相对风险同样也降低了27%;另外,Romosozumab组非椎体骨折风险降低了19%(包括髋部骨折风险降低)。
安进制药研发部高级副总裁Sean E. Harper表示:“Romosozumab相比对照药的治疗优势是显而易见的,新发现的心血管事件将作为Romosozumab整体获益的一部分进行相应评估,我们将同优时比公司协同合作,加强同相关领域专家的接触并促进该药的行政注册工作。”
ARCH研究的整体不良事件和严重不良事件方面与对照组中整体是相似的,在起初的Romosozumab12个月用药过程中也是相似的。在12个月 Romosozumab用药过程中,最常见的3种不良反应为:鼻咽炎、背痛、关节痛,Romosozumab组的注射部位不良反应的发生率为4.4%,对照组为2.6%,大多数注射部位反应轻微。在随后开标的阿仑唑奈用药过程中,有两例下巴骨坏死的裁定事件,一例发生在Romosozumab合并用药组,一例发生在阿仑唑奈单药组;同时有6例非典型股骨骨折裁定事件(2例发生在Romosozumab合并阿仑唑奈组,4例发生在阿仑唑奈单药组)。Romosozumab组12个月治疗后严重心血管不良反应裁定事件的发生率为2.5%,对照组为1.9%。没有在7180名患者参与的大型FRAME研究中观察到心血管严重不良事件的不平衡。
目前, 基于FRAME临床研究的药物注册审评审评已经提交给美国FDA、加拿大卫生部及日本PMDA,均处在审批中。安进制药同时会将ARCH研究的数据提交给FDA作为上市审批所需资料的一部分,按照计划Romosozumab暂时不会在今年内获得上市批准,同时向欧洲EMA的注册工作目前也仍在准备之中。临床3期研究ARCH的进一步的分析工作正在进行中并会在未来的医学会议上进行结果公布。(新浪医药编译/David)
参考来源
UCB and Amgen announce top-line phase 3 data from active-comparator study of Evenity? (romosozumab) in postmenopausal women with osteoporosis
来源:新浪医药新闻 作者:David
为你推荐
 资讯
资讯 圣因生物完成超 1.1 亿美元 B 轮融资,加速 RNAi 疗法全球布局
本轮融资由知名产业机构领投,国际主权基金、中国生物制药、君联资本等十余家机构跟投,全球制药巨头礼来公司战略入局,高瓴创投、启明创投等现有股东持续加码支持,融资规模创...
2025-12-12 16:59
 资讯
资讯 投后估值达21.37亿元,实体瘤细胞治疗领军企业君赛生物递表港交所
君赛生物共有5款在研产品,其中核心产品也是进展最快的是GC101,正开展上市前的关键II期临床试验,有望成为国内首个获批上市的TIL细胞创新药
2025-12-12 09:24
 资讯
资讯 ESMO-IO | ORR达41.7%!君赛生物GC101 TIL治疗晚期后线非小细胞肺癌I期数据首次公布
这不仅是全球首个无需高强度清淋化疗、无需IL-2给药的TIL疗法治疗肺癌的临床研究,也是国内首个公开披露该领域数据的注册性临床研究。
2025-12-12 09:17
 资讯
资讯 君合盟生物启动重组 A 型肉毒毒素治疗成人上肢痉挛状态临床 III 期试验,并完成首例患者入组
该临床试验由复旦大学附属华山医院李放教授和上海市养志康复医院(即上海市阳光康复中心)靳令经教授联合牵头
2025-12-11 21:06
 资讯
资讯 Medidata发布全新调研报告:临床试验AI应用价值凸显,超七成用户反馈“达到或超预期”
基于对来自全球制药公司、生物科技公司及合同研究组织(CRO)中超200位核心决策者的深度调研,报告显示,目前AI在改善患者招募、优化数据管理、控制运营成本和提升试验效率等方...
2025-12-11 20:57
 资讯
资讯 近20年首个全新类别抗菌药物醋酸来法莫林纳入医保,开启中国成人社区获得性肺炎治疗普惠新篇章
该产品继2025年6月30日获得国家药品监督管理局批准用于治疗成人社区获得性肺炎(CAP)后又纳入国家医保目录
2025-12-11 20:50
 资讯
资讯 专注 “生物学 + AI” ,普瑞基准完成超亿元 D 轮融资,加速 AI 驱动新药研发
本轮融资由信立泰、广投资本、申宏中恒基金联合领投,老股东金谷汇枫、聚翊投资持续跟投
2025-12-10 15:55
 资讯
资讯 别把“嗜睡”当懒癌!新型促觉醒药翼朗清®获批,专注维持日间清醒
促觉醒药物翼朗清®(盐酸索安非托片)正式获得中国国家药品监督管理局(NMPA)批准,用于改善阻塞性睡眠呼吸暂停(OSA)伴有日间过度嗜睡(EDS)的成人患者的觉醒程度。
2025-12-10 11:04
 资讯
资讯 复星医药将其GLP-1产品全球化权益授权辉瑞,总里程碑付款近150亿人民币
12月9日晚间,复星医药发布公告称,公司控股子公司药友制药、复星医药产业与辉瑞共同签订《许可协议》,(其中主要包括)由药友制药就口服小分子胰高血糖素样肽-1受体(GLP-1R)...
2025-12-10 09:12
 资讯
资讯 Capricor Therapeutics公司宣布外泌体疗法Deramiocel在DMD三期中取得积极成果
近日,专注与外泌体疗法的Capricor Therapeutics(纳斯达克代码:CAPR)公司宣布其核心管线Deramiocel在杜氏肌营养不良症关键三期 HOPE-3 研究中取得积极成果。
2025-12-09 16:38
 资讯
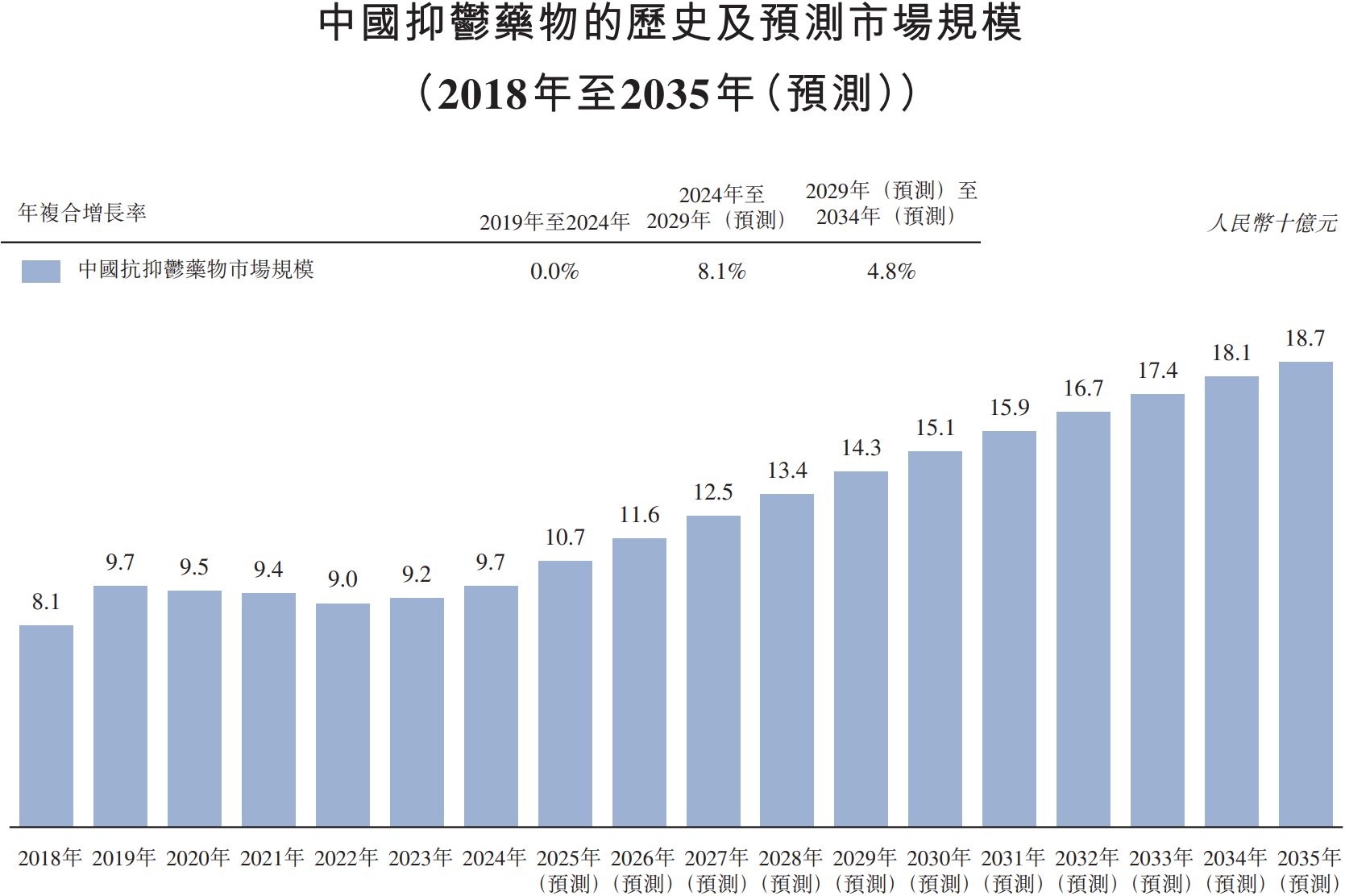
资讯 中药1类创新药剑指抑郁症治疗蓝海,远大医药GPN01360成功达到国内II期临床终点
国产抗抑郁症药物研发取得重大进展。近日,远大医药(0512 HK)的1 1类中药创新药GPN01360国内II期临床研究成功达到临床终点,产品表现出显
2025-12-08 18:27