多年前,美国FDA曾统计过,美国的创新药物开发效率大体为,“10000个化合物中有250个可以进入临床前研究,这其中仅有5个能够进入临床研究,而最终只有1个能获得上市”,总体的成功效率为“万分之一”。新药研发之所以具有如此高风险的特征,与其研发的过程以及药审部门对药物与日俱增的高要求密不可分。从基础研究到药物发现、从药物发现到进入开发期、再到后期的注册审评和生产上市,化合物向药物蜕变的每一个过程,都面临着重重困难,而要克服这些困难,最初阶段的研究工作,就显得尤为重要,毕竟好的开始是成功的一半。在这里,有关“类药性、成药性”问题,就不得不好好的捋清一下!
1、新药研发流程简介
通常情况下,新药研发须经过以下过程:发现功能基因组、疾病病理机制等为新药发现提供新的靶标和理论为上游的基础研究阶段;利用新靶标和理论,结合现有技术形成专利和候选化合物为新药发现阶段;对候选药物开展临床前综合评价、临床评价、产业化工艺研究等为新药开发阶段;在前面的基础上经过注册,获得上市为上市阶段。而最后,对于销售所带来的获益,需要借助专业的销售团队,毕竟好产品被卖砸了的案例也是数不胜数!
2、类药性~先导化合物的选择!
所谓类药性,表示的是一个理想药物应基本具有的特性,是成为药物所表现出来的理化性质(如相对分子质量、脂水分配系数等)以及结构特征(如环结构、可旋转键数目等)的综合反映。类药化合物所表现出的结构和理化性质必须与体内药动学参数具有良好的相关性,其可以看做是对苗头或先导化合物最基本的要求!
类药性的判别方法大体可以分为三类:基于理化性质、基于特定结构片段和基于判别分析模型。药物分子在化学空间中的分布并不均匀,而是集中在一个相对较小的区域。人们对药物动力学性质和生物利用度相关的理化性质进行了大量研究,并以这些性质作为类药性评价指标。对于类药性,不得不提一下广为流传的Lipinski “类药五规则”,即:相对分子质量< 500、氢键供体数< 5、氢键受体数< 10、Log P< 5,如果一个化合物违背Ro5中的2个及以上的规则,该化合物成为口服药物的可能性较低。这里的五规则是指这套规则中每个参数都是5的倍数,而不是指5条规则。Ro5被广泛用于对化合物库的初筛,以期摒除那些不适合成为药物的分子,缩小筛选的范围并降低药物研发成本,是目前应用最广泛的类药性评价指标。
药物的理化性质集中在一定的范围之内,药物分子在结构上也存在这样的规律。有些结构片段与化合物的毒性或副作用有关,有些则可以表现出良好的药理活性和药动学性质(如芳胺、芳硝基和硫原子、卤素的含量等对于化合物的成药性有积极作用),所以总结药物结构方面的规律,依据特定的结构特征也可以指导组合化合物库的评价和优化。最近几年随着计算机技术的迅速发展和组学研究的兴起,人们对类药结构片段的研究上升到了片段组学(scaffoldomics或fragmentomics)的高度,提出了基于片段的药物设计(Fragment-based Drug Design,FBDD)理论与方法。根据化合物的理化性质和结构特征,利用各种计算机学习方法,通过对药物和非药物化合物进行训练,也可以建立自动区分类药化合物和非类药化合物的计算模型,如此一来,就大大提高了类药性的研究。
3、成药性~候选药物的选择!
所谓“成药性”,则是指具有足以使活性化合物能够进入临床I期试验的ADME性质和安全性质,其包括适宜的物理化学、生物化学、药代动力学、安全和结构新颖性等属性。简言之,成药性是对候选药物、乃至药物的必备特征。对于候选药物成药性的评价,属于药物的开发阶段,其包括临床前综合评价、临床评价和产业化研究三个方面。我国现阶段新药创制效率低下的瓶颈当属临床前的成药性综合评价。
临床前综合评价是所有药物开发的共同通路,所有药物都要经过这一阶段的工作,以确定安全、有效、质量可控,其可以分为生物学评价和药学评价。生物学评价主要是明确候选药物的药效、作用机制、毒理学反应、药代特点及药物相互作用等。药效评价的关键在于根据将来的临床适应症,利用合理的动物疾病模型进行评价;毒理学评价需要严格按GLP要求,发现候选药物可能的毒性作用及毒性靶器官,为可能的临床不良反应提供参考方向;药代评价是为临床给药方案提供参考数据;药学评价的目的主要是确定合适的制备工艺路线和建立可靠、稳定、简便的质控标准及方法,特别要考虑到将来工业化的可行性。
而临床评价,则是新药开发的决定性阶段,由各大医院按GCP要求进行,要求新药开发单位必需要有相应的临床专业人才贯彻开发意图,不能单纯被动地依赖临床单位。研究方案的合理性,研究数据的完整性、客观性、规范性是评价的核心内容。对于与预期目标不一致的结果不要轻易放弃,应进行细致的分析,可能会发现意想不到的结果。产业化研究,则是以环保、成本、质量为目标进行新药的规模生产工艺的研究,产业化目标应该贯穿新药开发的整个过程,这类的工作在我国目前的新药研发单位已越来越受重视。
4、小小感触
我们在做创新药物时,活性问题的重要性自不必说。别说是mM级别的化合物,μM级别的化合物通常都会被我们pass掉,但当我们真拿到了nM级别的化合物时,却真心不能高兴太早,因为其离成为一个真正的药物还需踏实的经历好多好多。认真考虑、模拟、测试其在药物发现阶段的“类药性”,做好坚实的基础,再转移到药物开发阶段的“成药性”,将大大提高新药发现与创制的效率,尽量减少、避免当一个候选药物因“突发状况”而止步于临床的无奈与可惜!
参考文献
1.Sugiyama Y. Druggability: selecting optimized drug candidates [J].Drug Discovery Today,2005.
2.Harry J,Tom LB,David B A. Flexibility and small pockets at proteineprotein interfaces: New insights into druggability [J].Progress in Biophysics and Molecular Biology,2015.
3.Hussein HA,Geneix C,Petitjean M,et al. Global vision of druggability issues: applications and perspectives [J].Drug Discovery Today,2016.
4.李晓,孔德信. 化合物成药性的预测方法[J].计算机与应用化学,2012.
5. 徐为人,汤立达. 加强成药性综合评价提高我国新药创制效率[J].中国医药技术经济与管理,2007.
来源:药渡(微信号 Pharmacodia)
为你推荐
 资讯
资讯 全国预防接种日:“健康中国家,疫苗护万家”健康社区“免疫行动”促进计划启动
由新华网主办,中国医药卫生文化协会疫苗与健康分会、《中国社区医师》杂志联合支持的“健康中国家,疫苗护万家——健康社区‘免疫行动’促进计划”于4月23日在北京正式启动。
2025-04-24 14:07
 资讯
资讯 带状疱疹疫苗“遇冷”,百克生物2024年净利润腰斩
近日,国内疫苗龙头企业百克生物发布2024年年报,数据显示,其报告期内实现营收12 29亿元,同比下降32 64%;归属于上市公司股东的净利润2 32亿元,同比下降53 67%。对于营收...
2025-04-23 12:59
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
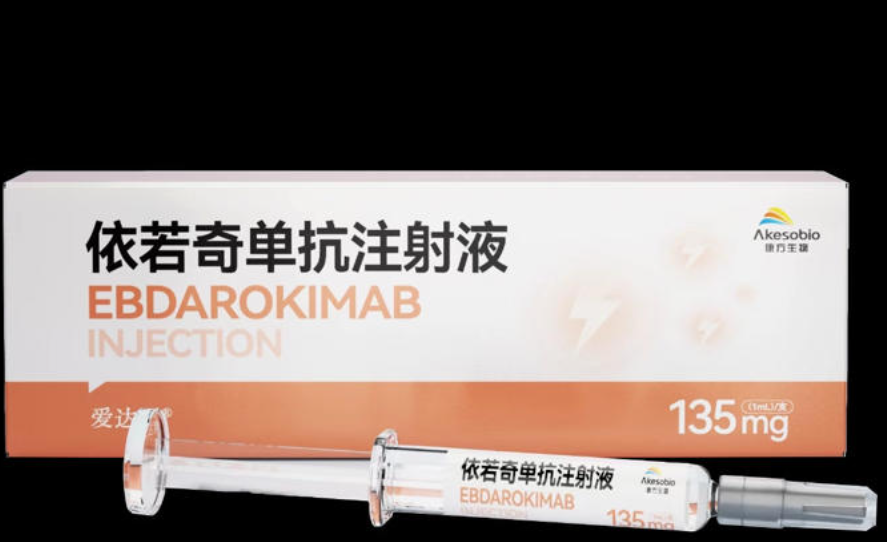
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54










