上个月,位于马萨诸塞州的CoLucid Pharmaceuticals宣布了一条好消息:其在研新药lasmiditan在一项关键性的3期临床试验中取得了良好结果。它达到了主要临床终点,也达到了关键的次要疗效临床终点。这个好消息或许意味着lasmiditan距离FDA的批准上市又近了一步。
偏头痛也许是最为常见的神经系统疾病之一。根据世界卫生组织的估计,全世界大约有10%的人曾出现过偏头痛。在中国地区,偏头痛患者的比例约为9.3%,与世界平均水平接近。偏头痛的主要症状为中度或重度单边或搏动性头痛,病发时,患者往往对光敏感和恶心,持续时间可从数小时到数天。由于偏头痛通常会陪伴终身,这种疾病对患者的正常工作与生活影响很大。
尽管影响了世界上十分之一的人群,偏头痛的治疗手段还较为有限。目前的常规治疗药物会增加心血管疾病的风险,并且有将近40%的患者使用后疗效不佳。因此,广大的偏头痛患者人群需要一种新药来缓解自己的病情。
Lasmiditan的分子式
Lasmiditan就是为了满足这一巨大医疗需求而研发的新药。它最早由礼来公司发现,并由CoLucid Pharmaceuticals进行研发。Lasmiditan是一种5-羟色胺受体激动剂,能渗入中枢神经系统,并特异激活5-羟色胺1F类受体。经激活后,这类特殊的受体能影响到三叉神经的通路,缓解偏头痛症状。
在3期临床试验中,lasmiditan的疗效与安全性得到了验证。这项3期临床试验招募了2231名患有偏头痛的患者,平均偏头痛史超过了19年。这些患者被随机分为试验组与对照组,并分别服用lasmiditan与安慰剂。和对照组相比,试验组在两小时内偏头痛症状得到完全缓解的比例显着上升,达到了主要临床终点。此外,恶心、厌光等与偏头痛有联系的症状也能在2个小时之内得到显着缓解。在安全性方面,由于不作用于血管系统,它不会引起血管收缩,因此也不会提高使用者心血管疾病的发病风险。
“Lasmiditan有潜力成为一种重要的治疗方案,这对于那些有高心血管疾病风险的患者来说尤其如此”,阿尔伯特?爱因斯坦医学院的神经学系副主任Richard Lipton博士说道。
CoLucid目前正在招募第二个关键3期临床试验的患者,具体的研究数据有望在明年下半年问世。倘若两项临床试验都获得成功,公司将启动lasmiditan的上市批准流程。
来源:药明康德
为你推荐
 资讯
资讯 全国预防接种日:“健康中国家,疫苗护万家”健康社区“免疫行动”促进计划启动
由新华网主办,中国医药卫生文化协会疫苗与健康分会、《中国社区医师》杂志联合支持的“健康中国家,疫苗护万家——健康社区‘免疫行动’促进计划”于4月23日在北京正式启动。
2025-04-24 14:07
 资讯
资讯 带状疱疹疫苗“遇冷”,百克生物2024年净利润腰斩
近日,国内疫苗龙头企业百克生物发布2024年年报,数据显示,其报告期内实现营收12 29亿元,同比下降32 64%;归属于上市公司股东的净利润2 32亿元,同比下降53 67%。对于营收...
2025-04-23 12:59
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
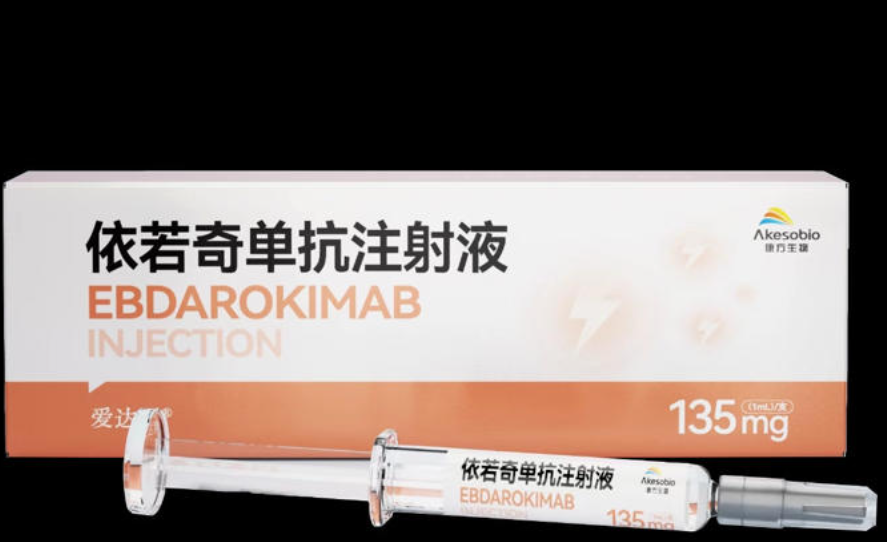
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54













