罕见病亦称孤儿病,就单个病种而言累及的患者人群较小,鉴于每种疾病的患者人数都不多,故这一领域一直未成为主流制药公司的研发重点。即使是在美国,绝大多数罕见病迄今仍然是无药可治。
如果想要帮助更多的患者,最好的办法就是为他们开发更多的新药。好在制药公司开始意识到未满足医疗需求的孤儿药市场具有盈利潜力。
而通过投资,可以撬动更多的药物研发,最好的商业就是最大的公益。
孤儿药的定义
美国FDA认可6000种罕见病,欧盟认可8000种罕见病,美国FDA批准约350种孤儿药(包括生物药)用于治疗大约200种罕见病,所以孤儿药还有很大的市场空间。
美国的孤儿药法案实施前(1983年前),FDA批准的所有新药中,总共只有38种是用来治疗孤儿药的;而该孤儿药法案通过以后,从1983-2004年,共有1129种不同的化合物或生物制品以孤儿药审批途径进入临床实验,最终有249种孤儿药被批准上市。如今,美国通过认证上市的孤儿药已有410种。
同样的情况也发生在在欧盟,在1999年《罕见病治疗药物管理规定》实施前,欧盟仅有8种孤儿药被审核通过,但1999-2009年间,便有619种罕见病产品得到认定,47种孤儿药被审核通过。而到目前为止,欧洲药物管理局已经授予1000多种孤儿药。
中国并没有一个官方的明确的罕见病定义,也没有一个明确的数字(发病率)来划分罕见病和普通病,但在药品注册管理办法的第三十二条、以及新药注册特殊审批管理规定中,有提及罕见病、特殊病种等情况,可减免临床试验例数。但两者世界卫生组织(WHO)将罕见病定义为患病人数占总人口0.65‰-1‰的疾病,均无对罕见病有具体的界定。
孤儿药的特点:政策优惠大、研发费用低、临床实验规模更小
在国际上尤其美国,对于孤儿药的各种政策无需再累述,美国FDA已经批准约350种孤儿药(包括生物药)用于治疗大约200种罕见病。所以即使是在美国,绝大多数罕见病迄今仍然是无药可治,但这也显示孤儿药还有很大的市场空间,以三期临床统计,目前孤儿药的研发费用是非孤儿药的一半,政府的各种优惠主要体现在:
1、联邦政府对药企在孤儿药的研发经费退税(最高可达50%),以及相关竞争性联邦经费支持;
2、增强专利和孤儿药市场化保护;
3、快速审批程序;
4、规模更小的临床实验
在新药研发过程中据统计,超过6成的开销是在临床实验上,有的甚至高达8成。除了研发金额庞大,所需的临床人数也是一个很困扰药品研发机构的难题。尤其III期临床,可能涉及多达一千至数千病人(对于罕见病这个是不可能的),周期长达5年以上。
不但研发过程中可以得到联邦经费支持,临床实验阶段的开销也大大降低。有的孤儿药,即使是在3期临床阶段只有几十个病人也最终批准上市了(因为适应症是罕见病不可能集结数千病例)。并且,孤儿药一般定价都很高,一般每个病人需要花费20万到50万美元。
而美国的商业保险公司也愿意为此买单,在欧洲的情况也类似,这类药品虽然价高,但是患病率很低。在一个大的投保人群基数中,该风险将讲的非常低,很容易进入医保目录。
孤儿药的治病机理往往是机理相对明确的病,如单基因疾病等,研发的时候容易确定靶点,有的放矢,成功率较高。据FDA2011年的一个关于罕见病和孤儿药介绍的文件记载,4/5的罕见病都是有相应的遗传背景的。
由于受众很少,难以满足III期临床的病例要求,往往得以减免临床试验例数,从而可以加快注册进程和注册成本,潜在的好处则是,孤儿药相比受众巨大的慢性病,更容易出于人道因素考虑,进入医保许多制药公司为了加快产品的上市,往往是从孤儿药做起,然后再扩大应用,开发多适应症。先上市,再谋求更大的利益上市后研发公司独占市场若干年(美国为7年,欧盟为10年)以及通过绿色通道直接进入医疗保险支付名单。
实际上,前景最好的孤儿药通常针对的是一些常见病(如肿瘤和血液病)中的一些亚型。以美国为例,FDA批准的孤儿药40%左右是肿瘤领域,从目前全球最畅销的10种孤儿药来看,主要都是治疗如肿瘤疾病和血液病等看起来似乎常见的疾病的;2011年FDA批准的11种孤儿药中有7种是肿瘤领域(癌症)的某个亚型,2012年15种孤儿药中有8种是治疗肿瘤的某个亚型,2013年批准的12个孤儿药中有7个是治疗肿瘤的的某个亚型。
2014上半年FDA批准的27个新药里面,14个药物以优先审评的方式获批,其中10个药物拥有孤儿药资格(6个用于肿瘤领域),以我自己熟悉的例子来讲,Roche的重磅炸弹利妥昔单抗当年作为孤儿药获批用于治疗CD20 阳性弥漫大B 细胞性非霍奇金淋巴瘤,在后面国内的临床中我们也会根据文献的报道在滤泡淋巴瘤、套细胞淋巴瘤等上使用,也遇到过在自免疾病上的使用,回过头来看当时的超适应症使用现在都变成了FDA批准的适应症,现在利妥昔也已经成为全球最畅销的药品之一。
孤儿药投资要全面考虑疾病、药物开发、市场价格、政府监测、政策
孤儿药是一个社会问题,如果你想要帮助更多的患者,最好的办法就是为他们开发更多的新药。
据调研报告《孤儿药报告(2014)》(来自Evaluate Pharma)预期,从2014年至2020年,全球孤儿药销售规模的年增长率将达到11%,是处方药(仿制药除外)的两倍;市场规模将从2014年的970亿美元增长到2020年的1760亿美元,占处方药(仿制药除外)市场规模的19%。而法国咨询公司Alcimed则表示,治疗罕见病的药物已成为医药行业最盈利的板块之一,几乎所有国际大型制药公司都加大了罕见病药物的研发投入。
在具体投资过程中,个人认为主要分为以下思路来进行投资:
1、罕见病有很多都是儿童的疾病,这一块我们是可以利用这些相应政策。国家现在对儿童用药的研发是非常支持的。然后罕见病有很多都是儿童的疾病,我们是可以利用这些政策来做的,去年美国DiaVacs的DV-0100 取得孤儿药资格,成为获得1型糖尿病治疗药物上市许可的公司,可在美国市场享有长达七年的市场独占权,1型糖尿病(T1DM)治疗在国内还未引起较多人的关注,其实既能作为孤儿药也能作为儿童药,两项政策同时享受,我们也很喜欢这类似的项目,利用各种政策降低成本同时降低风险。
2、选择在美国属于孤儿药,但在中国却有大量病人的药物进行立项和开发,这也是大家最常用的办法,立足于国内市场的企业可以重点开发具有多重适应症方向(包含罕见病方向)的药物。或开发具有多重身份的药物(兼有罕见病和儿童用药方向----比较好的方法是药物再定位,对于以往已经上市的药物,重新定位其新的适应证,尤其是找到罕见病适应证,已经上市或停研的一系列化合物重新定位。巧用捷径跳跃,某些常规药物鉴于某些疾病细分领域(如基因分型属于罕见病)或国内外疾病谱差异(如肝癌、胰腺癌在美国属于罕见病)。
3、 505B(2)申请也有机会享有孤儿药带来的额外独占权,从孤儿药做起,然后再扩大应用,开发多适应症。先上市,再谋求更大的利益立足于本土进行一些药物的开发,放眼全球进行临床试验以及上市的申请两边申报,主要是充分的利用一下国外对于孤儿药支持的政策,利用我国相对较低的临床前研发成本,在国内开展临床前研究,在研发过程中严格保持高素质实验和高水平的数据记录,以备日后在海外申报临床。
关于这方面我记得Pentamidine最早被用于治疗睡眠疾病 。随后的研究发现该药物可用与预防和治疗与AIDS相关的肺孢子虫性肺炎 (PCP),公司将Pentamidine 制成了该新适应症的喷雾剂,并通过505(b)(2)进行新药申请。该适应症被FDA批准并被授予孤儿药资格和7年的市场独占期。最终公司的收购价达到了10亿美元。
4、另外我们可以通过转让国外的权益给国外的药厂这样的方式,能够得到一笔比较大的转让的费用,而中国的权益留在中国,让出海外权利部分风险共担。在美国把孤儿药分成两类,一类是孤儿药,另一类是超级孤儿药。美国FDA组织的团队非常严格,他们会挑战申请者的设计和统计方法,想顺利通过不容易。所以到一定阶段出让海外权益不失为一种策略。
5、另外投资孤儿药不是一个要点满足即可,应全方位的考虑,包括疾病、药物开发、市场价格、政府监测、政策等,是需要一个综合考虑。第一,该孤儿药对应的疾病领域确实是医学上的一个空白;第二,一定要了解疾病的进程和恶化。比如有的罕见病,患者必须在出生3 个月之内治疗才有效,6 个月之后再治疗就没用了。3这些数据在我们当时提出免临床的过程中,起到了关键作用。研究罕见病,如果能专注于建设相关数据库,你在全球就是一个领先者。
孤儿药开发面临的各种挑战
谈论这么多孤儿药的投资,公司本身也有过投资孤儿药的经历,但其实我有更多的担心点和大家一起分享:
1、CRO公司,国内的公司对CRO稽查不到位甚至没有,当然也是国内的特色说来话长不在此讨论。而国外企业无论做什么,Ⅰ期到Ⅲ期,甚至Ⅳ期试验,一律用中心实验室、影像中心、病理中心和EPG中心,这是国内很难达到的,所以我们也会配合投资企业一起在美国寻找合适自己的CRO。
2、临床试验方案的制定,孤儿药很多情况是单一的临床实验,单臂实验设计。即使单臂非双盲的实验研究中,孤儿药的关键实验一般不是用的硬指标,用的是替代指标。也是对方案设计提出较高要求。
3、适应症的选择,孤儿药并不是简单的孤儿病即可,应该根据自身药物的特点或者说在早期试验上的数据来做出一定的倾向。
4、孤儿药其临床实验中受试者的死亡率更高一些,严重不良事件发生率以及死亡率高于非孤儿药的抗肿瘤药的研究,即独立的临床安全数据监察委员会审查每一例死亡及严重不良事件,以更客观地评价安全性事件。考虑到这一点,在中国进行临床实验时必须有应对的预案。加之国内医患关系的紧张,死亡病例会产生很大的纠纷。建议,在中国做孤儿药,必须成立DSMB或DMC,即独立的临床安全数据监察委员会审查每一例死亡及严重不良事件,以更客观地评价安全性事件
5、要找到罕见病病患已经很不容易,还得保证“每个病患对应每个不同的指标数据点”。为罕见病专设方案一个临床试验项目的运行预算必须把试验中可能出现的失误考虑进去,以防失误出现时试验必须第一时间从头开始。
总之,孤儿药的开发面临诸多挑战。其中另外两个较大的障碍是发现和招募患者以及试验机构的物流。
在谈论孤儿药的各种特征和投资孤儿药的看法后,其实还有最大的问题没谈到就是支付的问题,当然这也是我无能为力的。从地区来讲,青岛在罕见病医疗保障方面做得很不错,有近20个不同的高值昂贵药物(大多数是治疗罕见病的药物)被纳入医保范围内,当地居民的报销比例甚至可达100%。从单病种来讲,目前全中国医疗报销最好的单病种的罕见病是血友病,不同省份可以报销到55%-85%。
在国内,目前采取的政策是单病种先走(血友病等患者数量较多的药物),地区先行(经济发达、改革走在前方的地区)的模式,目前在青岛模式中,药物报销的资金并不来自医保,而是来自市政府专项资金,社保部门只负责谈判与经办。“将利益相关方捆绑在一起,政府成立专项资金,承担大部分费用,药企降低市场进入价格,患者家庭也出一小部分。政府、药企和患者形成的三方共担机制。先财政给钱,再民政给钱,然后慈善和企业基金会给钱,最后个人负担一点。
从我国的”十二五“生物制药领域的规划来看,”十二五“期间药物研发还是以我国重大疾病为主。这个从国家层面也可以理解,我国连重大疾病都是以仿制药为主(或者说基本都是),就更没有财力和精力来研发孤儿药了。但是即使是仿制,由于孤儿药以生物药为主,仿制难度和成本都远非化学仿制药可比。所以,孤儿药的仿制也需要我国政策上的扶植。
国内做孤儿药一定要面向全球,利用海外优惠政策做全面全球的药物而不仅仅是针对国内的患者,否则有了情怀亏了自己。
有句广告词:用实力让情怀落地,而做孤儿药既需要实力也需要情怀! 我只希望当关于”孤儿药“,引起各方重视多部门联动,资助鼓励”孤儿药“研发,加快”孤儿药“的上市速度;建立政府、社会、患者共担机制……相信到那时”孤儿药“将不再是个”孤儿“。
作者简介:本文作者周毓,分享投资VP,华西医科大学临床药学专业;超过10年医疗领域工作经验,曾任职于罗氏、美敦力、波士顿科学、圣犹达、史赛克等知名跨国医疗企业。欢迎联系zhouyu@sharecapital.cn。
来源:贝壳社(微信号 iBio4P) 作者:周毓
为你推荐
 资讯
资讯 带状疱疹疫苗“遇冷”,百克生物2024年净利润腰斩
近日,国内疫苗龙头企业百克生物发布2024年年报,数据显示,其报告期内实现营收12 29亿元,同比下降32 64%;归属于上市公司股东的净利润2 32亿元,同比下降53 67%。对于营收...
2025-04-23 12:59
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34
 资讯
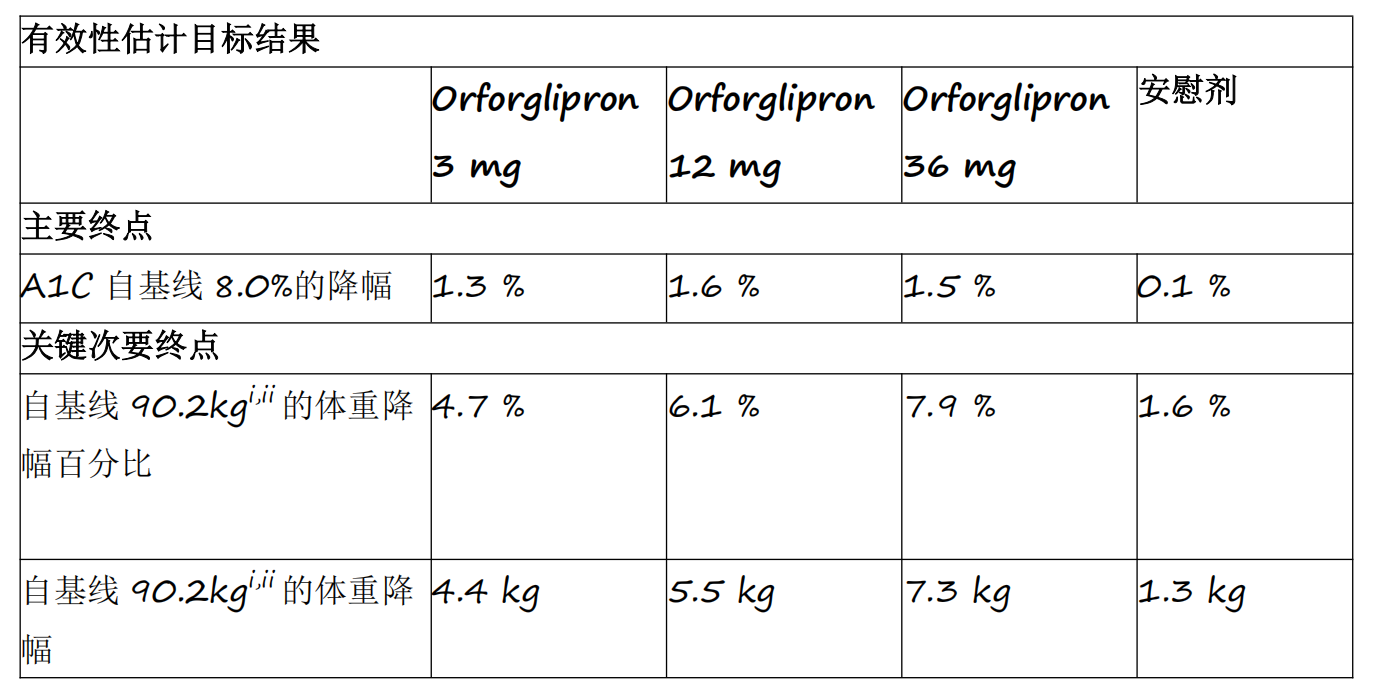
资讯 礼来首个小分子口服GLP-1RA药物orforglipron 3期临床研究成功
Orforglipron是首个成功完成3期临床研究的小分子GLP-1类药物,各剂量组平均A1C降幅为1 3%至1 6%
2025-04-18 14:12









