FDA8月30日批准诺华子公司Sandoz的Erelzi(etanercept-szzs)上市,用于治疗以下多种自身免疫性疾病:
单药或与甲氨蝶呤联用,治疗中重度类风湿关节炎
2岁以上的多关节性幼年特发性关节炎
活动性银屑病关节炎,包括对甲氨蝶呤单药治疗响应不足的银屑病关节炎患者。
中重度强直性脊柱炎
适合系统疗法和光线疗法的18岁以上慢性中重度斑块状银屑病
Erelzi 是Enbrel(依那西普,anti-TNF FC融合蛋白)的生物类似物。Enbrel最早1998年在美国上市,2015年全球销售额达到86.97亿美元,其中辉瑞33.33亿美元,安进53.64亿美元。
Erelzi 的药品标签带有黑框警告,警示医疗人员和患者使用Erelzi可能会增高严重感染风险,甚至导致住院和死亡。
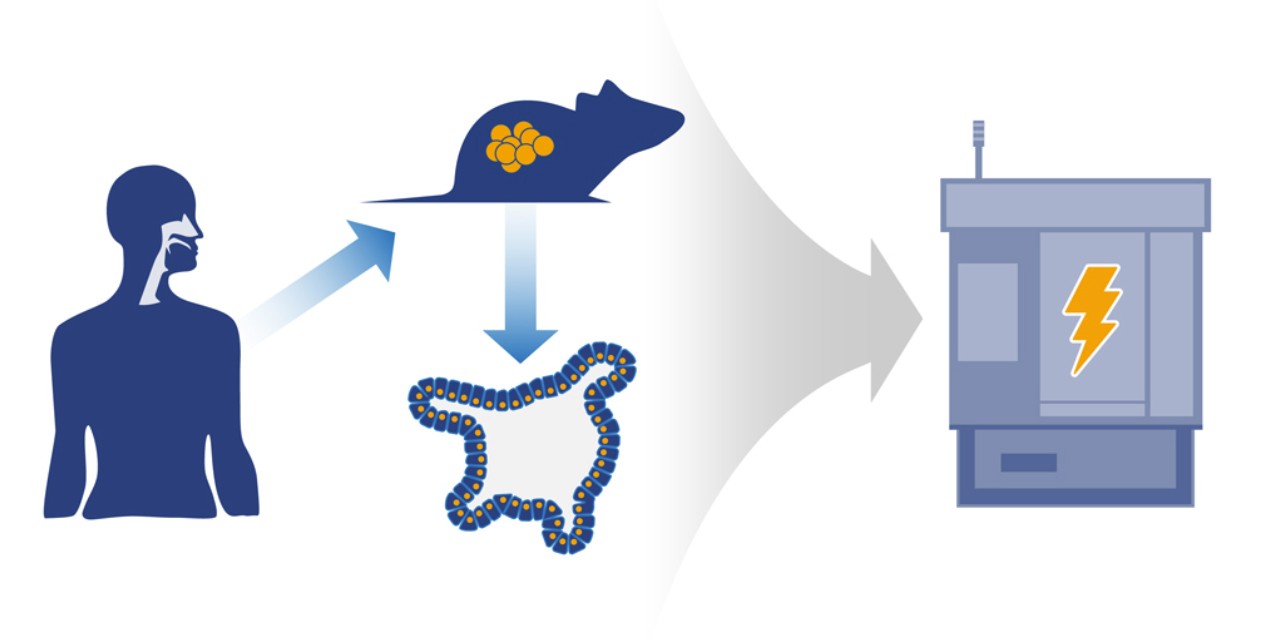
FDA批准Erelzi是基于一些结构和功能表征、动物实验研究、人体药动学研究和药效学资料,其与Enbrel的生物等效性已在临床免疫原性、安全性和疗效方面获得证实。Erelzi作为生物类似物获批,而非可替换产品(interchangeable product)。
Biogen/三星Bioepis合作开发的Enbrel的生物类似物Benepali已于1月底获得EMA批准,用于治疗中重度类风湿关节炎,银屑病关节炎,非放射性中轴性脊柱关节炎,成人银屑病。
参考资料
http://www.fda.gov/Drugs/DevelopmentApprovalProcess/HowDrugsareDevelopedandApproved/ApprovalApplications/TherapeuticBiologicApplications/Biosimilars/ucm241718.htm
来源:医药魔方数据(微信号 iyiyaomofang) 作者:大圣
为你推荐
 资讯
资讯 强生公司宣布锐珂(埃万妥单抗注射液)在华上市,携创新机制药物开启肺癌诊疗新时代
今日(4月12日),强生公司宣布,旗下创新肺癌治疗药物锐珂®(埃万妥单抗注射液)正式在华上市。
2025-04-12 17:25
 资讯
资讯 2025全国爱鼻日:科学防治鼻病 技术赋能健康
今天(4月12日)是全国爱鼻日,今年爱鼻日以“科学防治鼻病——科技赋能鼻腔健康,顺畅呼吸轻嗅百香”为主题,旨在提升行业及公众对鼻部疾病科学化、系统化、规范化防治的认知水平。
2025-04-12 08:23
 资讯
资讯 医院因未完整上传追溯码数据,被医保基金拒付处理
能够实时监测追溯码采集数据,从完整性、规范性、及时性等方面配置监测指标,向医保智能监管子系统推送追溯码采集不达标明细数据,由医保智能监管子系统配置事中审核规则,形成...
2025-04-11 19:10
 资讯
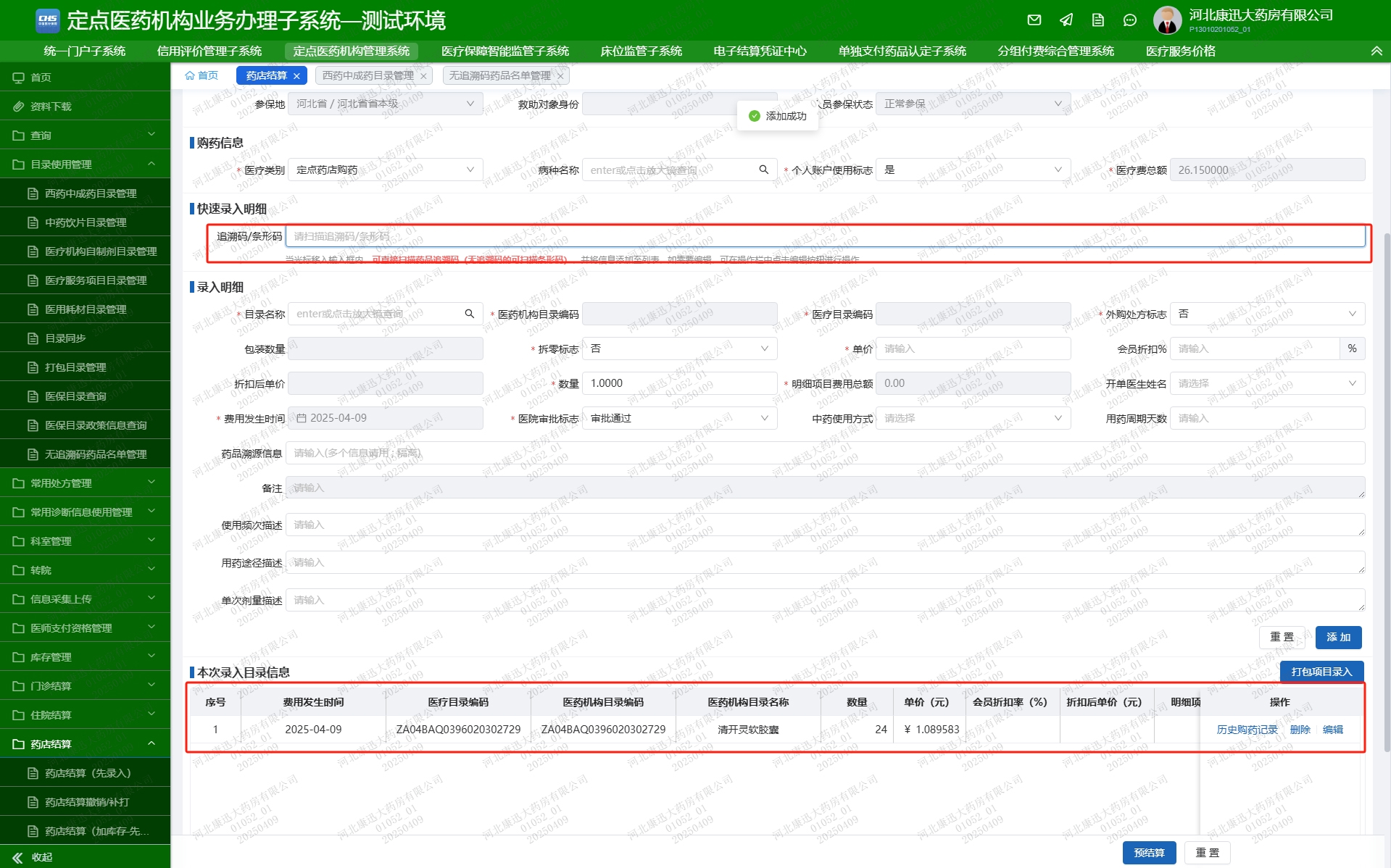
资讯 河北省统一规划,推动定点零售药店实现“无码不结”
近日,石家庄参保市民王先生在去药店购药时,发现药店工作人员仅使用扫码枪扫描了药盒上的追溯码,就完成了医保结算,比以往买药结算要高效很多。
2025-04-11 18:52
 资讯
资讯 巴可携数字化手术室等亮相CMEF2025,以领先科技赋能精准医疗
巴可携标准医用显示与定制化方案、4K全光纤数字化手术室解决方案,以及Coronis OneLook多模态诊断成像显示器等创新产品亮相
2025-04-11 10:50
 资讯
资讯 健康消费有哪些,《促进健康消费专项行动方案》发布
提升健康饮食消费水平;优化特殊食品市场供给;丰富健身运动消费场景;力发展体育旅游产业;增强银发市场服务能力;壮大新型健康服务业态;引导健康产业多元发展;强化药店健康...
2025-04-10 22:25
 资讯
资讯 美的楼宇科技亮相2025CMEF,全维智变助力智慧医院绿色焕新
2025年4月8日-11日,第91届中国国际医疗器械博览会(CMEF)于上海国家会展中心拉开帷幕。在这场全球医疗健康科技的风向标盛会上,美的医疗携旗下万东医疗、楼宇科技、生物医疗等...
2025-04-10 11:41
 资讯
资讯 科赴支持权威协会发布中国首个常见轻微病症管理专家共识
近日,由中华医学会全科医学分会、中国医药教育协会药学服务专业委员会、中国健康促进与教育协会医防融合分会联合编撰的《常见轻微病症健康管理专家共识(2025版)》(以下简称...
2025-04-09 15:50
 资讯
资讯 Cytiva蛋白A层析填料新品发布 推动单抗药物纯化工艺降本增效
全新发布的MabSelect SuRe 70与MabSelect PrismA X蛋白A层析填料将大幅降低生产成本,提高生产效率
2025-04-09 13:23
 资讯
资讯 国家药监局要求进一步做好《药品生产许可证》发放有关事项
2025年7月1日以后发放的《药品生产许可证》,各省级局应统一以本行政区域内电子证照二维码形式管理,《药品生产许可证》正本、副本的纸质版和电子证照应分别标注二维码。
2025-04-08 21:34
 资讯
资讯 第91届CMEF开幕:盈康一生携AI+创新成果亮相 共建数智医疗生态
本届展会,盈康一生以“AI在海尔,因AI盈康”为主题,携旗下明星产品、AI创新场景解决方案亮相。
2025-04-08 15:54
 资讯
资讯 @医疗人士 生物相容、抗菌、精密注塑...梦寐以求的创新方案在哪?都给您归纳好了!
2025-04-08 15:10
 资讯
资讯 德国默克集团宣布与恒瑞医药再度达成合作,推进辅助生殖领域口服GnRH拮抗剂的商业化落地
根据协议条款,默克公司将向恒瑞支付1500万欧元首付款;在此基础上,恒瑞有权收取许可产品的里程碑付款及在许可区域的年度净销售额两位数百分比的销售提成。
2025-04-08 13:32
 资讯
资讯 恒瑞医药、瀚宇药业、贝达药业等医药企业对特朗普“对等关税”的回应
恒瑞医药(600276 SH)在互动平台上表示,公司海外销售业务占营业收入的比例很小,根据2024年年报数据,海外销售业务占比仅为2 56%,美国加征关税对公司业务影响非常有限。
2025-04-08 12:49
 资讯
资讯 诺和诺德与腾讯健康启动战略合作 构建数字化肥胖防控新生态
今日(4月7日),全球肥胖症治疗领域领导者诺和诺德,与腾讯健康宣布达成战略合作。在国家持续推进“体重管理年”行动的背景下,双方将依托基于微信平台的“腾讯健康”小程序与...
2025-04-07 17:52