2016年4月25日,哈尔滨誉衡药业股份有限公司(简称誉衡药业)发公告称,公司与药明康德共同研发的抗PD-1单抗产品GLS-010注射液取得阶段性进展,通过了黑龙江省食品药品监督管理局经形式审查,认为公司递交的申报材料基本符合《药品注册管理办法》等有关规定的要求,予以受理,受理编号为CXSL1600045 黑。
此前,医谷曾报道过《誉衡药业“牵手”药明康德签署创新化学药与抗肿瘤生物药协议》,《框架协议》签订后,双方就合作事宜进行了多次洽谈。2015年5月22日,誉衡药业与无锡药明康德生物技术有限公司(以下简称“药明康德”)签订了《抗PD-1全人创新抗体药合作开发协议》,双方决定采用风险共担、收益共享的方式,就开发抗PD-1抗体产品相关的发现研究、临床前药学研究、临床前动物实验研究、产品各阶段注册申请、临床实验、临床样品生产、上市许可及销售等各环节开展合作。
据公告显示,此次申报的抗PD-1单抗产品GLS-010注射液是由国内研发机构完成临床申报的首个全人源抗PD-1单克隆抗体,在国内PD-1抗体药物研发领域具有重要里程碑意义。与传统的放化疗等治疗手段相比,以PD-1单克隆抗体为代表的免疫检查点抗体药物在近期引发了抗肿瘤药物的一场革命,它具有疗效显著、副作用小等突出优点,尤其在与其它抗肿瘤药物的联合用药方面具有广泛前景。
虽然誉衡药业GLS-010注射液的注册申请已受理,最终是否批准须经过国家相关部门审查后决定,药品研发的程序复杂,时间周期较长,但是本次阶段性进展依然为誉衡药业与药明康德合作共赢奠定良好的基础。
医谷链
为你推荐
 资讯
资讯 带状疱疹疫苗“遇冷”,百克生物2024年净利润腰斩
近日,国内疫苗龙头企业百克生物发布2024年年报,数据显示,其报告期内实现营收12 29亿元,同比下降32 64%;归属于上市公司股东的净利润2 32亿元,同比下降53 67%。对于营收...
2025-04-23 12:59
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
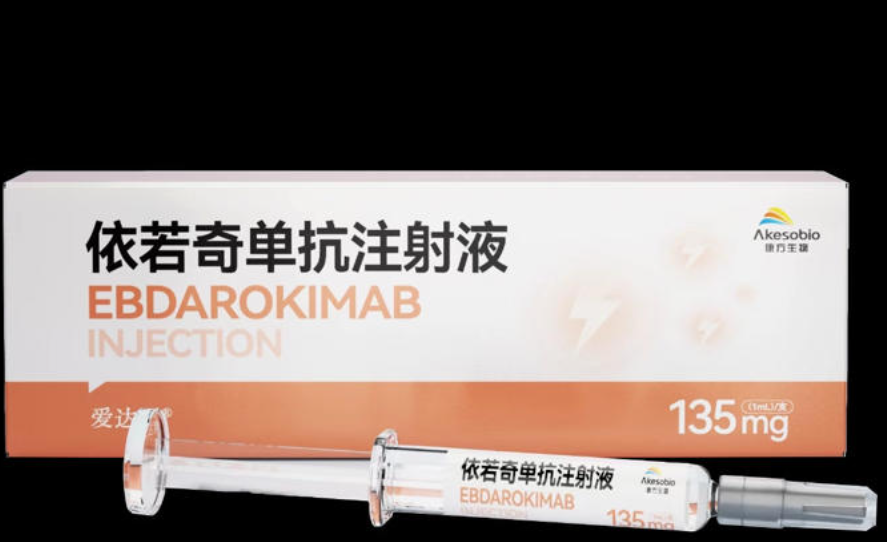
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
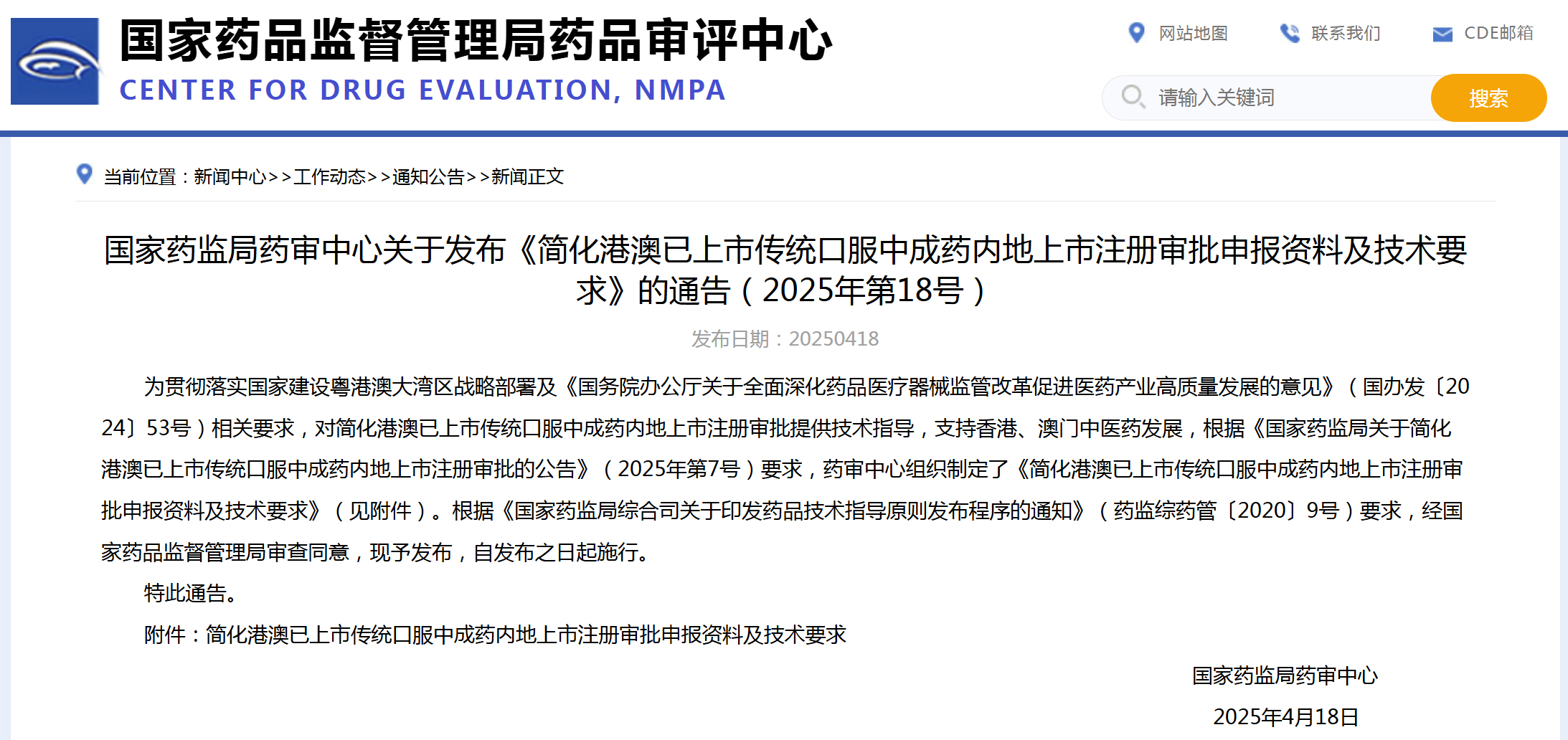
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34










