7月22日,CFDA发布《关于开展药物临床试验数据自查核查工作的公告》,决定对1622个已申报生产或进口的待审药品注册申请开展药物临床试验数据核查。CFDA用“最严谨的标准、最严格的监管、最严厉的处罚、最严肃的问责”四个最严来作为此次自查核查的要求,要求自该公告发布之日起,所有已申报并在总局待审的药品注册申请人,均须按照《药物临床试验质量管理规范》等相关要求,对照临床试验方案,对已申报生产或进口的待审药品注册申请药物临床试验情况开展自查,确保临床试验数据真实、可靠,相关证据保存完整。最为急迫是自查电子版报告要求在8月25日前上交,或者撤回。
7月23日,CFDA通过官网发布了两个自查报告模板——《生产注册申请的人体生物等效性试验数据自查报告表》和《生产注册申请的药物临床试验数据自查报告表》。
关于药物临床试验数据的大规模自查正式展开。业界人士对CFDA此番雷霆动作的理解集中在四个层面:其一,数年来,临床试验数据的不规范,甚至造假的动作已经有了需要集中治理的阶段,或者说“要揭盖”了;其二,撤回还是不撤回?给申报路上的制药企业留的考虑时间并不多,许多药企老板集中性失眠;其三,接下来一个月,可能对于CRO、SMO来说是一个大洗牌的时节;其四,也是最重要的,这对于现阶段积压的待审药品注册申请将是一次挤压、清洗的过程。
自查范围规模最大
CFDA的《药物临床试验数据自查核查品种清单》公布了1622个受理号,其中进口药171个受理号,新药948个受理号,已有国家标准503个受理号。化药需要自查1283个受理号,占79.1%,中药大多是2005年至2006年的受理号,共237个,占14.6%。生物制品共102个受理号。
“这是自查范围最大的一次,此前虽然也有专项调查,但是尚无如此规模。”一位药监体系人士表示。
查什么?
(一)核对锁定的数据库与原始数据一致性,统计分析以及总结报告数据与原始记录及数据库的一致性;数据锁定后是否有修改以及修改说明等。
(二)生物样本分析测试仪器(如HPLC、LC-MS/MS)等主要的试验仪器设备运行和维护、数据管理软件稽查模块(Audit trail)的安装及其运行等。
(三)各临床试验机构受试者筛选、入组和剔除情况,受试者入选和排除标准的符合情况,抽查核实受试者参加临床试验的情况。
(四)临床试验方案违背例数、剔除例数、严重不良事件例数等关键数据;医院HIS系统等信息系统中的受试者就诊信息、用药及检查化验的临床过程情况等。
(五)试验药物和对照药品的生产或购进、检验、运输、保存、返还与销毁以及相关票据、记录、留样等情况。
(六)生物样本的采集过程及运送与交接和保存等记录;生物样本分析方法确证,生物样本分析过程相关的记录以及样本留样情况。
(七)有关方在临床试验项目中主要职责的落实情况、合规情况。
撤还是不撤,违法成本如何?
国家局在公告中表示,申请人自查发现临床试验数据存在不真实、不完整等问题的,可以在2015年8月25日前向国家食品药品监督管理总局提出撤回注册申请。
那么撤还是不撤呢?对于申报药企来说,这可是重大损失。毕竟,已经投入那么多的,国家又提高了注册成本和要求,再申报的难度加大了不止一点点。心有不甘的是肯定的。
但是如果真的不符合国家规定,还是撤了吧。
CFDA飞行检查中发现临床试验数据弄虚作假的,临床试验数据不完整不真实的,将依据《中华人民共和国药品管理法》第七十八条、《药品注册管理办法》第一百六十六条的有关规定,追究申请人、临床试验机构、合同研究组织的责任,并向社会公开申请人、临床试验机构、合同研究组织及其法定代表人和相关责任人员。
此外,在公告中,CFDA强调:对核查中发现临床试验数据真实性存在问题的相关申请人,3年内不受理其申请。药物临床试验机构存在弄虚作假的,吊销药物临床试验机构的资格;对临床试验中存在违规行为的人员通报相关部门依法查处。将弄虚作假的申请人、临床试验机构、合同研究组织以及相关责任人员等列入黑名单。
涉及103家上市公司
据咸达数据分析,1622个受理号中有309个受理号分别属于国内103家上市公司。华海药业(600521.SH)涉及的受理号数最多,达9个。
若以药品名称数排名,排第一的是恒瑞医药(600276.SH)和国药一致(000028.SZ),各14个产品名需要自查。有27个申报1类或1.1类的产品名需要自查,其中9个属于上市公司,包括天津红日的甲苯磺酰胺注射液、江苏恒瑞的磷酸瑞格列汀片和盐酸卡屈沙星葡萄糖注射液、贵州景峰的黄芪甲苷葡萄糖注射液、上海仁会生物的贝那鲁肽注射液等产品。
“需要自查的受理号中,有13个受理号属于重大专项,国内上市公司占了8个受理号。21个受理号属于特殊通道,国内上市公司占了11个;加快品种共有7个受理号需自查,其中有一个属于国内上市公司。曾经状态为‘批准生产’的102个受理号也同样面临自查,有11个受理号属于国内上市企业。”咸达数据创始人、香港中文大学副研究员张玉峰表示。
自查报告将与注册申请挂钩
文件称:药品审评过程中,发现申请人有下列情形之一的,将依据《药品注册管理办法》第一百五十四条的有关规定,注册申请不予批准。包括:(一)拒绝、逃避或者阻碍检查或者毁灭证据的;(二)临床试验数据不能溯源,数据不完整的;(三)真实性存疑而无合理解释和证据的;(四)未提交自查报告的。
哪类品种自查目录中最多?
哪些地方监督品种数量过百?
据统计,江苏、山东、浙江、北京、广州四地需要监督的品种过百;以江苏199个品种为例,从8月25日自查结束到9月8日短短15天内,如果每个产品都组织监督,江苏省药监部门平均每天需要监督的品种数量为13.3个。对于国外品种的监督,CFDA未予指定监督的相应机构。
哪些企业自查产品最多?
据统计,1622个品种来自815家企业。自查数量超过(含)10个品种的企业有11家。其中,华海药业、恒瑞医药、石药集团分别以21、18、17个品种待查位列榜首。仅1个品种在自查目录中的企业数量占总企业数的六成。同样是33天,不知道这些企业将会如何度过。奉上自查品种数量超过5家的企业名单。
混乱和腐败的临床数据
“自查并不是行政审批的一道程序,之前也没有这么大规模地要求企业进行自查工作。因为当前审批人数有限,申报品种数量多,很多资料可能存在造假。如果在审批这个环节一个个去审核资料,需要很长时间,导致很多审批工作挤压,所以现在要求企业先自查。”一位接近CFDA的人员表示。
对于药品安全,审批无疑是最为重要的关口。CFDA也坦承,这次自查正是落实党中央、国务院用“最严谨的标准、最严格的监管、最严厉的处罚、最严肃的问责,确保广大人民群众饮食用药安全”的要求,从源头上保障药品安全。但分析药物临床试验的数据和信息质量,更是关键环节之关键。这道关守不住,谈不上从源头上监管药品的安全问题。
临床试验数据就是药品的生命,没有这个临床试验数据,药品无法谈及生产和市场推广。可在中国药品市场上,临床试验数据仍存在一定水分。
“食药监总局的做法是对的,应该严格,临床数据太乱了,我估计50%以上都造假。造假的方法很多,成为行业潜规则,造假水平高的根本查不出来。这个问题是该管管了,但能否管得住是另外一回事。”一位长期从事药品研发的人员表示。
“临床试验很复杂,一期、二期、三期,都有很严格的管理过程,如果没有科学的管理,没有一定的流程管理、资格,是做不了临床试验的。现在药品审批的报件要求越来越高,可能有些企业不能按照要求去做,或者委托的试验中心不能严格管理,就会出现不能满足申报要求,不能满足安全科学的临床结果就报上来了,这种现象是存在的。”北京大学医药管理国际研究中心教授史录文向记者表示。
史录文说,在国外,临床试验考察非常严格,采用双盲、严格数据和统计,对于数据批件,有不同的部门来核查,以此来观察企业是否造假。
“咱们没有这么严格,所以免不了有些不法企业做一些违法的事情,很难去查、很难去一一核对。所以让企业自查,自己去保证,也是让企业自我提高、自我约束的一个方式。”史录文表示。
但是在药品研发人员眼中,试验数据造假都不是症结,问题是腐败逼迫的造假。
这位研发人员向记者表示:“因为腐败导致审批不公平,一个好药,能赚钱,但就不批准,理由很容易找,就是安全性有问题,谁也不敢说安全性没问题,万一死人谁承担责任?所以就不批了,也不退审,一直拖延。当利益足够大时,就批了,利益不一定是现金,有可能是股权,有可能是帮助晋升等。之前腐败猖獗时,大家都觉得,不是在审查技术资料,而是在比拼谁能够进入这个腐败圈子进行腐败,试验数据就没有那么重要了。”
正因这种参差不齐的临床试验数据存在的不准确性,导致医药行业人士认为,市场上有很多无效药。“很多临床试验都只是动物阶段的数据,并不是人体数据,就拿来申请了,导致很多无效药出现。”一位药品专家表示。
药品申报积压难题
在CFDA药品审评中心网站上,可以看到受理品种目录有5074个,在审品种目录有4883个,但审评人员只有120人。如此多的药品资料和专业数据,单纯靠审批环节的行政人员用火眼金睛挑出来,难度何其大。
审评人员太少、药品申报量太大是导致审评时限过长最突出的矛盾。这一关如何把控?考验的不仅仅是药品安全问题,更考验审批人员的能力和人力问题。
“通过自查的方式,让一些存在假资料的企业自动退出,可以节省一部分审批环节的人力,现在审批环节人手也不够,不可能一个个进行核查。”上述接近CFDA的人员表示。
对于这次自查,张玉峰认为,CFDA可以一箭双雕。这1622个受理号中,不少是2008年以前的受理号。国家药品审评中心曾承诺3年内解决药品申报积压的事宜,但目前处理能力有限,远远比不上药企申报产品的热情。以目前对临床数据的高要求去自查2008年以前申报的临床项目,基本没有多少项目能符合要求现有的标准。
企业若不主动撤回注册申请,则大多项目历史数据都不完整,现在重做也不现实,按规定数据不完整也要受罚。博弈后项目数据不过关的产品企业只能选择撤退。通过临床数据自检让药企知难而退,顺道还解决了一大批受理号积压的问题。
在史录文看来,这个方式自查可以对企业起到警示效果,可以给企业一个提升的机会。事实上,如果真的严格按照临床试验程序来走,很多的小企业是没有能力研发出药品的。
张玉峰认为,此次自查会让行业重视临床基础数据的重要性,这只是药监局对行业药品注册进行规范的第一步,后续可能还有其他措施在加快药品审批的速度的同时,保证药品审批的严谨性。只有在研发生产中坚持高标准的企业才能在这场政策洗礼中“剩者为王”。
CFDA处理问题脉络
今年两会期间,国家食药监总局(CFDA)药品注册司官员在医药界两会代表座谈会上指出,争取用三年时间解决药品审评时限过长的问题。国家局的表态出来之后,业界普遍反应是不可能,但是看看国家局的动作,先是提高了注册成本,让以后药品注册费用大幅度涨上来,然后现在是清理存货。
医谷+
国家食品药品监督管理总局关于开展药物临床试验数据自查核查工作的公告(2015年第117号)
为落实党中央、国务院用“最严谨的标准、最严格的监管、最严厉的处罚、最严肃的问责,确保广大人民群众饮食用药安全”的要求,从源头上保障药品安全、有效,国家食品药品监督管理总局决定对附件所列已申报生产或进口的待审药品注册申请开展药物临床试验数据核查。有关事宜公告如下:
一、自本公告发布之日起,所有已申报并在总局待审的药品注册申请人,均须按照《药物临床试验质量管理规范》等相关要求,对照临床试验方案,对已申报生产或进口的待审药品注册申请药物临床试验情况开展自查,确保临床试验数据真实、可靠,相关证据保存完整。
二、自查的内容包括:(一)核对锁定的数据库与原始数据一致性,统计分析以及总结报告数据与原始记录及数据库的一致性;数据锁定后是否有修改以及修改说明等。(二)生物样本分析测试仪器(如HPLC、LC-MS/MS)等主要的试验仪器设备运行和维护、数据管理软件稽查模块(Audit trail)的安装及其运行等。(三)各临床试验机构受试者筛选、入组和剔除情况,受试者入选和排除标准的符合情况,抽查核实受试者参加临床试验的情况。(四)临床试验方案违背例数、剔除例数、严重不良事件例数等关键数据;医院HIS系统等信息系统中的受试者就诊信息、用药及检查化验的临床过程情况等。(五)试验药物和对照药品的生产或购进、检验、运输、保存、返还与销毁以及相关票据、记录、留样等情况。(六)生物样本的采集过程及运送与交接和保存等记录;生物样本分析方法确证,生物样本分析过程相关的记录以及样本留样情况。(七)有关方在临床试验项目中主要职责的落实情况、合规情况。
三、2015年8月25日前,申请人应就附件列出的品种,向国家食品药品监督管理总局食品药品审核查验中心提交电子版自查报告、临床试验合同扫描件、研究团队主要人员情况等材料,以及法定代表人签字的真实性承诺。自查报告的具体要求详见国家食品药品监督管理总局食品药品审核查验中心网站:www.cfdi.org.cn(联系电话:87559031)。
四、申请人自查发现临床试验数据存在不真实、不完整等问题的,可以在2015年8月25日前向国家食品药品监督管理总局提出撤回注册申请。
五、各省(区、市)食品药品监督管理部门负责对行政区域内申请人的自查工作进行监督。根据监督工作需要,可以组织对临床试验情况进行调查,调查对象应包括临床试验机构、合同研究组织等相关机构。对调查中发现的问题应及时锁定证据并提出处理意见,于2015年9月8日前将相关情况报告国家食品药品监督管理总局。
六、国家食品药品监督管理总局将组织专家对申请人的自查材料等进行数据分析并视情况开展飞行检查。检查中发现临床试验数据弄虚作假的,临床试验数据不完整不真实的,将依据《中华人民共和国药品管理法》第七十八条、《药品注册管理办法》第一百六十六条的有关规定,追究申请人、临床试验机构、合同研究组织的责任,并向社会公开申请人、临床试验机构、合同研究组织及其法定代表人和相关责任人员。
七、药品审评过程中,发现申请人有下列情形之一的,将依据《药品注册管理办法》第一百五十四条的有关规定,注册申请不予批准。包括:(一)拒绝、逃避或者阻碍检查或者毁灭证据的;(二)临床试验数据不能溯源,数据不完整的;(三)真实性存疑而无合理解释和证据的;(四)未提交自查报告的。
对核查中发现临床试验数据真实性存在问题的相关申请人,3年内不受理其申请。药物临床试验机构存在弄虚作假的,吊销药物临床试验机构的资格;对临床试验中存在违规行为的人员通报相关部门依法查处。将弄虚作假的申请人、临床试验机构、合同研究组织以及相关责任人员等列入黑名单。
特此公告。
食品药品监管总局
2015年7月22日
来源:E药经理人 第一财经 医谷综合
为你推荐
 资讯
资讯 全国预防接种日:“健康中国家,疫苗护万家”健康社区“免疫行动”促进计划启动
由新华网主办,中国医药卫生文化协会疫苗与健康分会、《中国社区医师》杂志联合支持的“健康中国家,疫苗护万家——健康社区‘免疫行动’促进计划”于4月23日在北京正式启动。
2025-04-24 14:07
 资讯
资讯 带状疱疹疫苗“遇冷”,百克生物2024年净利润腰斩
近日,国内疫苗龙头企业百克生物发布2024年年报,数据显示,其报告期内实现营收12 29亿元,同比下降32 64%;归属于上市公司股东的净利润2 32亿元,同比下降53 67%。对于营收...
2025-04-23 12:59
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
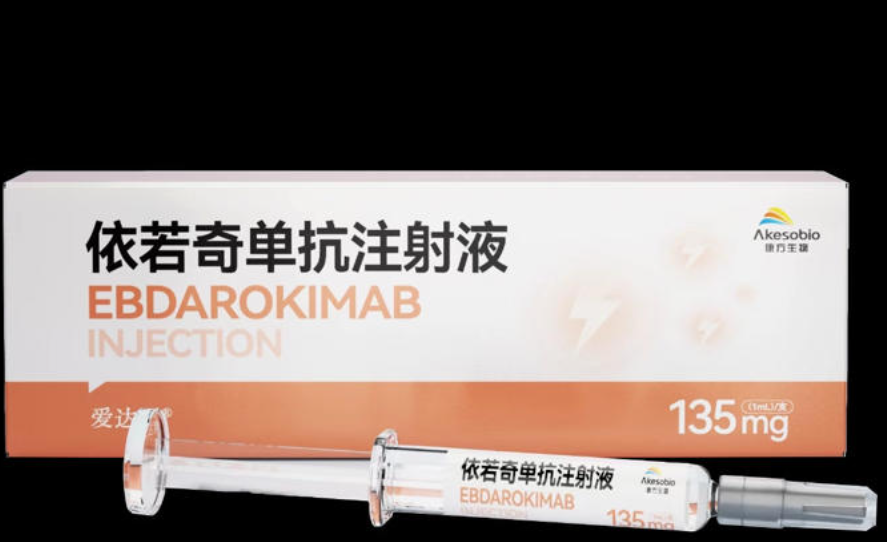
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54













