目前有多个慢性淋巴细胞白血病新药处于临床试验阶段,新药的作用机制涵盖了PI3Kδ和PI3Kγ抑制剂、BCL-2抑制剂、脾酪氨酸激酶抑制剂、趋化因子CXCL12抑制剂、抗CD20单克隆抗体、抗CD19单克隆抗体、抗CD44肽类药物等。其中III 期临床慢性淋巴细胞白血病新药包括口服PI3Kδ和PI3Kγ抑制剂Duvelisib、口服BCL-2抑制剂Venetoclax、抗CD20特异性单克隆抗体Ublituximab;II 期临床新药包括免疫调节剂Lenalidomide、选择性脾酪氨酸激酶抑制剂Entospletinib、抗CD19单克隆抗体MEDI- 551和MOR- 208、抗CD44肽类药物A6、抗趋化因子CXCL12寡核苷酸药物Olaptesed pegol、SMO抑制剂Vismodegib和化疗药物Sapacitabine;I 期临床慢性淋巴细胞白血病新药如PI3Kδ抑制剂TG- 1202。
一、III 期临床慢性淋巴细胞白血病新药
(一)口服PI3Kδ和PI3Kγ抑制剂Duvelisib
III 期临床药物中进展最快的是Infinity/AbbVie公司联合研发的Duvelisib(曾用名IPI-145)。Duvelisib是一种口服PI3Kδ和PI3Kγ抑制剂, PI3Kδ和PI3Kγ对恶性B细胞的生长和存活有重要的作用。 Duvelisib的I期临床试验结果显示,复发/难治型慢性淋巴细胞白血病患者,包括那些细胞遗传学特征不良的患者使用Duvelisib后显示了很好的响应率。Duvelisib开展了一项名为DUO的III 期临床,研究Duvelisib治疗复发/难治型慢性淋巴细胞白血病的疗效,预计在2015年下半年完成受试者招募。
(二)口服BCL-2抑制剂Venetoclax
AbbVie/罗氏联合研发的Venetoclax(曾用名ABT- 199或GDC-0199)目前处于III期临床试验阶段。Venetoclax为口服药物,通过选择性抑制B淋巴细胞瘤-2基因(BCL-2)而发挥作用,调节细胞凋亡。 临床前研究表明Venetoclax和利妥昔单抗联用存在潜在的协同作用。Ib期临床试验结果显示,Venetoclax和利妥昔单抗联用治疗慢性淋巴细胞白血病患者客观反应率为88%,完全反应率为31%。 Venetoclax的III期临床试验以苯达莫司汀联用利妥昔单抗为对照组,研究Venetoclax联用利妥昔单抗治疗复发/难治型慢性淋巴细胞白血病的疗效,该项III期临床试验是决定Venetoclax未来命运的关键。复发/难治型慢性淋巴细胞白血病临床治疗上存在较大难度,如果Venetoclax治疗此类患者能实现持久性应答,那么Venetoclax将在竞争中脱颖而出。但是使用Venetoclax时需密切监测患者以防出现肿瘤溶解综合征,这是Venetoclax的一个缺点。
(三)抗CD20特异性单克隆抗体Ublituximab
TG Therapeutics公司研发的抗CD20特异性单克隆抗体Ublituximab(曾用代码TG - 1101) 目前开始招募III期临床试验的受试者。Ublituximab的II期临床试验取得了喜人的结果, 慢性淋巴细胞白血病高危患者用药后客观缓解率达95%(19/ 20)。Ublituximab的III期临床试验旨在评估Ublituximab联用Ibrutinib,治疗曾经接受过治疗、具有慢性淋巴细胞白血病高危细胞遗传学特征如17 p缺失,11q缺失和/或p53突变患者的疗效。
二、II 期临床慢性淋巴细胞白血病新药
(一)免疫调节剂Lenalidomide
Lenalidomide(商品名Revlimid)为免疫调节剂,已经上市用于治疗套细胞淋巴瘤、多发性骨髓瘤、骨髓增生异常综合征。目前Lenalidomide治疗慢性淋巴细胞白血病的临床试验处于II期阶段,主要研究Lenalidomide对接受过一线治疗、具有复发可能性高危慢性淋巴细胞白血病患者无进展生存期的延长程度。
(二)选择性脾酪氨酸激酶抑制剂Entospletinib
吉列德公司研发的Entospletinib(GS- 9973),目前处于II期临床试验阶段,用于治疗复发/难治型慢性淋巴细胞白血病。Entospletinib为口服制剂,通过选择性抑制脾酪氨酸激酶(Spleen tyrosine kinase,Syk)而发挥作用。脾酪氨酸激酶对激活B细胞内信号转导具有至关重要的作用。 在II期临床试验中Entospletinib单药治疗临床效果较好,毒性在可接受范围内。然而联用PI3Kδ抑制剂Idelalisib毒性太大,导致这种方法的中止。
(三)抗CD19单克隆抗体MEDI- 551和MOR- 208
CD19是一种 B细胞特异抗原,介导B细胞下游信号的传导,是近年来科研人员感兴趣的慢性淋巴细胞白血病治疗靶点。 MedImmune /阿斯利康公司和MorphoSys公司都针对CD19研发了各自的药物MEDI- 551和MOR- 208。这两种药物都是CD19特异性人性化单克隆抗体,具有较强的细胞毒性,目前处于II期临床试验阶段。
(四)抗CD44肽类药物A6
Angstrom公司研发的A6目前处于II期临床试验阶段。A6为肽类物质通过与CD44结合而发挥作用。A6的II期临床试验研究初始治疗、不能使用FCR标准疗法治疗或不愿接受化疗的慢性淋巴细胞白血病患者使用A6的治疗效果。
(五)抗趋化因子CXCL12寡核苷酸药物Olaptesed pegol
NOXXON公司研发的Olaptesed pegol(NOX-A12),目前处于II期临床试验阶段。Olaptesed pegol是一种寡核苷酸,通过拮抗趋化因子CXCL12(也称为SDF-1)而发挥作用。 在血液学恶性肿瘤中CXCL12被中和后,将促进恶性肿瘤细胞从骨髓动员到外周血中,因在更容易消灭肿瘤细胞。Olaptesed pegol的II期临床试验主要是研究Olaptesed pegol与苯达莫司汀和利妥昔单抗联合应用治疗复发型慢性淋巴细胞白血病的疗效。 2014年阶段性成果表明Olaptesed pegol治疗患者取得了令人鼓舞的客观反应率,与历史数据相比全部反应率也有所提高。
(六) SMO抑制剂Vismodegib和化疗药物Sapacitabine
罗氏研发的Vismodegib和Cyclacel研发的Sapacitabine,目前处于II期临床试验阶段。 Vismodegib为跨膜受体smoothened homologue (SMO)抑制剂,目前已经批准用于治疗基底细胞癌(商品名Erivedge)。Vismodegib治疗复发 / 难治型慢性淋巴细胞白血病的临床试验处于II期,试验名称为VISMOLY试验。Sapacitabine为核苷类似物药物前药,干扰DNA合成,与环磷酰胺和利妥昔单抗联用。
三、I 期临床慢性淋巴细胞白血病新药
TG Therapeutics公司研发的TG- 1202处于I期临床试验阶段,该药为PI3Kδ抑制剂,用于治疗复发/难治型慢性淋巴细胞白血病。TG- 1202与其公司旗下III 期临床药物Ublituximab联用,可以治疗高危的慢性淋巴细胞白血病患者。
来源:新康界 作者: 金伊
为你推荐
 资讯
资讯 带状疱疹疫苗“遇冷”,百克生物2024年净利润腰斩
近日,国内疫苗龙头企业百克生物发布2024年年报,数据显示,其报告期内实现营收12 29亿元,同比下降32 64%;归属于上市公司股东的净利润2 32亿元,同比下降53 67%。对于营收...
2025-04-23 12:59
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34
 资讯
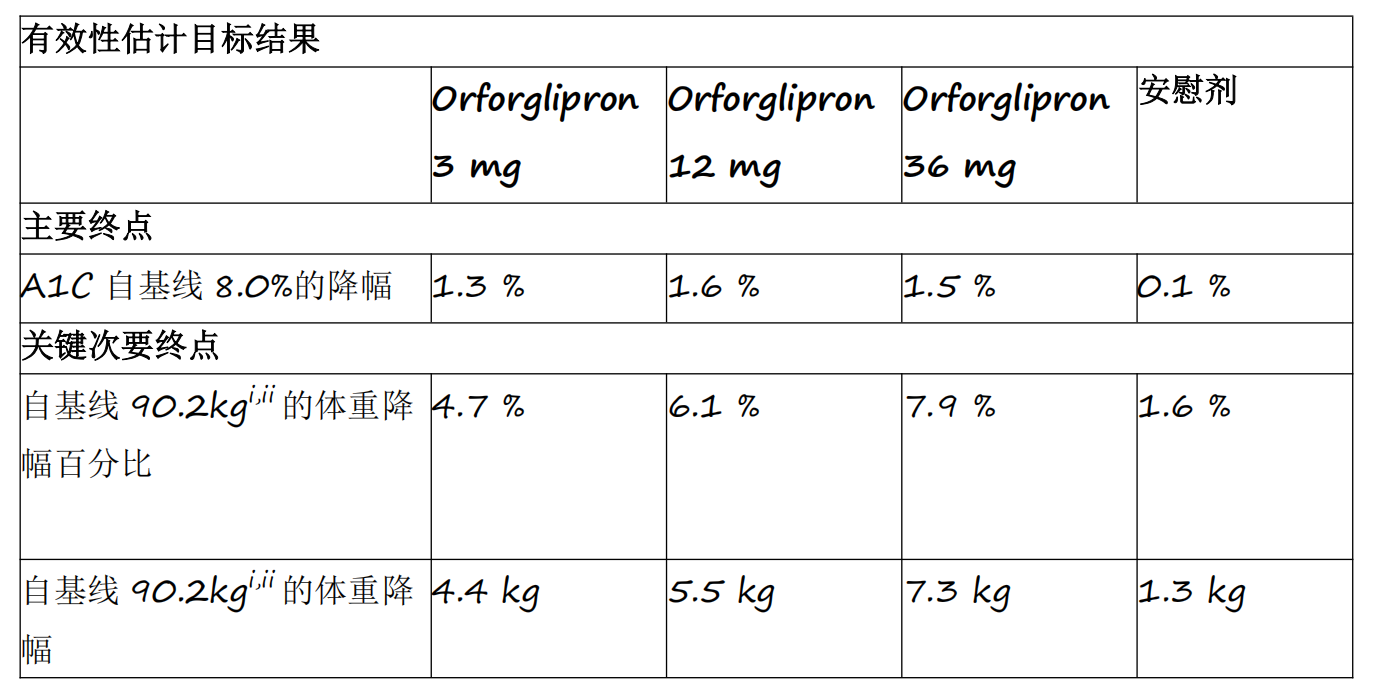
资讯 礼来首个小分子口服GLP-1RA药物orforglipron 3期临床研究成功
Orforglipron是首个成功完成3期临床研究的小分子GLP-1类药物,各剂量组平均A1C降幅为1 3%至1 6%
2025-04-18 14:12










