2015 ASCO今天正式开幕,万众瞩目的癌症免疫疗法开始向世人公开最近临床实验细节。今天施贵宝公布了哨卡抑制剂Opdivo一个叫做Checkmate-057的三期临床细节。这个实验是作为二线针对非鳞状非小细胞肺癌。和多西他赛比,Opdivo组的中值生存期延长2.8个月(12.2对9.4个月)。但对于PD-L1阳性患者,二者的生存期分别为17和9个月。这个结果比投资者预想要差,施贵宝股票下滑6.5%,70亿市值灰飞烟灭。Opdivo的主要竞争者Keytrduda厂家默沙东股票则上扬2%。
对于没有参加ASCO的读者来说今年ASCO有几个主要事件。明天ASCO主席将讨论大数据,而主题发言是哈佛商学院的Michael Porter,此人是按质论价政策的支持者。所以从宏观上看精准医学和控制药价是现在肿瘤治疗两个重要问题。据Bruce Booth统计,在近6000份摘要中HER2和PD-1是出现次数最多的两个关键词。HER2代表上一代重要靶标,现在还在这个领域的估计或者是为了延长产品寿命,或者是赫赛汀成功吸引的大批me-too药物。PD-1则是现在最为火爆的靶点,但是今天赛尔基因的BD领导人说第5个以后上市的PD-1抑制剂前景暗淡。所以表面上看大家都在风风火火去淘金,其实只有少部分人最后能淘到金。
PD-1抑制剂最令人关注的是施贵宝的Opdivo和默沙东的Keytruda。我们曾开玩笑说ASCO 2015是白雪公主和一群小矮人,而今天白雪公主打个喷嚏施贵宝就险些重感冒。Opdivo已经被批准用于鳞状肺癌,但这是一个较小适应症。这个Checkmate057上个月因为疗效显著被提前终止,但当时并没有公布比多西他赛好多少。今天投资者失望有两点,一是虽然无进展生存期延长不少(17.1对5.6个月),但总生存期2.8个月比预期值低。另一个更关键的是和鳞状肺癌不同(Opdivo在这个人群应答和PD-L1水平无关),在非鳞状肺癌患者PD-L1的表达和疗效有正相关,即PD-L1阳性病人应答更好。而有50%的病人为PD-L1阴性。主要竞争对手默沙东只招募了PD-L1阳性患者,所以投资者原来以为Opdivo的适用人群会更大。但现在看来Opdivo和Keytruda的标签可能会基本一样。
但是Opdivo和Keytruda有一个关键区别,即Keytruda没有生存数据。现在默沙东的申请是根据应答率,这可能会成为Keytruda的一个软肋。这两个药价格都是一年15万美元,无论从机理还是已有临床数据看几乎没有什么本质区别。但是如果我要是花那么多钱我会选择一个有生存数据的药物。当然默沙东很可能会补上这个生存数据。
Opdivo和Keytruda还有很多肺癌以外的适应症要在本届年会公布。Opdivo已经在肝癌显示20%应答,而Keytruda则在头颈癌有25%应答率。另一个关键进展是默沙东在直肠癌等几类肿瘤中发现一个叫做mismatch repair deficiency的基因标记可以预测应答。如果这个得到证实,则可以更加准确的细分人群。这既符合ASCO主席的精准医学思路,也满足主题报告的按价值消费原则。
对于癌症患者而言,只要有一线希望,许多人也愿意做小白鼠去尝试,因此国内部分患者也通过其他渠道获得Opdivo等PD-1制剂进行尝试,与其他靶向药类似,PD-1依然有非常严重的副作用,这可能是目前靶向药普遍需要解决的一个问题,对于目前进行靶向药研发的企业,未尝不可以考虑联合组合制剂的方式实现药物增长空间的利益化。
PD-1抗体使用,安全第一
PD1抗体确实是很多患者的希望,国内部分患者使用也有很好的疗效。我们比较了日本和美国PD1临床对患者的要求,他们临床都比较谨慎;一位患者翻译了使用PD1引起肝炎副作用的处理方法;最后,我们总结了国内几位使用PD1患者的情况。我们提醒患者在使用PD1的过程中能够多注意一些可能的副作用,避免一些可以避免的事情发生。
日本和美国的PD-1临床对患者的要求
患者在初次用药7日前检查结果应满足以下基准:白细胞数2000/mm³以上且中性粒细胞数1500/mm³以上;血小板数100000/ mm³以上;血红蛋白在9.0g/DL以上;AST(GOT)以及ALT(GPT)在设施正常值上限3.0倍以下;总胆红素在设施正常值上限2.0倍以下;肌酸酐在2.0mg/DL以下。另外,排除标准中明确规定了自身免疫病患者、移植患者和HBV/HCV检测阳性的患者不能入组。
仔细搜索clinictrial网站,MK-3475(Keytruda)的临床有100个,仔细看看这些临床的排除入组标准,很多都规定自身免疫病、间质性肺炎、长期服用免疫抑制剂、HBV/HCV感染和脑转的患者不能入组。比如一项Keytruda针对肉瘤患者的二期临床的排除入组标准中规定:活动性乙肝炎患者(乙肝表面抗原阳性)和丙肝患者;患有自身免疫病或者曾经患有自身免疫病或者患有需要类固醇或免疫抑制剂系统治疗的疾病的患者(感觉这里面包括了移植患者);患有非感染引起的肺炎,需要口服或是静脉注射类固醇治疗的患者,还有间质性肺炎患者。
以下来自日本的opdivo使用指南
10%以上的可能性会导致淋巴球减少症、白血球减少症、腹泻、疲劳、白斑、瘙痒症、皮肤色素减少。临床检查易发现血中CK、血中LDH、crp增加,噬酸细胞增加。
1%-10%的可能性会导致中性粒细胞减少症、葡萄膜症、视力低下、便秘、口干、恶心、口腔炎症、倦怠感、末梢性浮肿、疼痛、发热、口渴、蜂巢炎、细菌性肺炎、牙周炎、高钙血症、低钙血症、高尿酸症、食欲减退、糖尿病、肌肉痉挛、四肢疼痛、味觉异常、末梢性神经刺、打嗝、猴头痛、口腔咽头痛、脱毛症、湿疹、皮脂缺乏性湿疹、斑状丘疹性皮疹、脂溢性皮炎、荨麻疹、中毒性皮疹等。
白细胞、粒细胞、血小板和血红蛋白反应血象;ALT、AST和胆红素反应患者的肝功能;肌酸酐是患者肾功能的指标。跟这些指标相对应的是临床研究发现使用PD1抗体之后容易发生的副作用是:白细胞减少、血小板减少;肝功能损伤;肾功能损伤。记得还有对甲状腺激素的检测。
所以,对于身体状况不是很好的患者,使用PD1之前最好慎重考虑一下可能的后果。国外报道的这些副作用都是在有临床试验筛选的情况下发生的,如果国内的患者盲试,出现意外的情况可能会增加,也就意味着副作用的概率会增加。
肝炎的处理办法
之前我们总结过肺炎的处理方法,这个是Opdivo肝功能异常的处理方法,感谢癌友的翻译,一位癌友发给我们的这个。
国内PD-1使用情况
简单总结了下国内几位患者使用PD1的情况,注意,我们总结的肯定不全,仅供参考。
肝移植患者使用PD-1:
患者男,肝移植。2015年1月17号使用PD1抗体(1月9号也使用E7080);1月22号肝功和胆红素异常升高,怀疑是7080副作用,23号停掉;29号,肝功和胆红素继续飙升,细胞亚群检测CD4/CD8=3,确定会中轻度急排和胆道吻合口狭窄,保肝加FK治疗,直到2月13号出院也没降下来;2月16号ERBD术解决胆道问题,之后依然飙升;3月6号,肝穿刺确认依然是急排。然后大量激素冲击,指标开始下降,然后就是一直在对抗排斥以及随之而来的感染。下面这段话是经由家属同意发出来的对大家的警示:
PD1引起急排、免疫性肝功能损伤,然后一直做保肝治疗,用了大量的激素冲击治疗以及使用了大量的免疫抑制剂,导致他的免疫力大幅度下降,在医院肺部感染导致间质性肺炎,差点要了他的命。而且大量的激素和免疫抑制剂的使用,导致肺部转移灶疯狂生长,现在已经满肺都是了,还经常咳嗽咳血。而他肝功能这么差,也不能进行任何抗肿瘤治疗,连用靶向药都不行,所以下面的路真的更艰难。一切只因为用了一次PD1,所以我奉劝大家一定要了解清楚,但是国内估计没有什么医生真正了解可不可用,包括香港,养和医院也有病人用了后出现严重副作用,而他们也无法应对。目前我了解的就是与癌共舞网上的“老公天天开心“他们在加拿大,去了西雅图癌症中心,那里从PD1临床开始就使用,到现在已经好几年了,有丰富的经验,用之前病人不同情况要如何调整到什么状态才可以用,可以避免出现什么情况,感觉人家是非常有经验,心里有数该如何用这个药的,而我们盲试风险真的很大!仅供大家参考!
我们替这位患者祈福。如果有医生有好的意见或是建议也请联系我们,谢谢。
腹泻
患者女,宫颈癌。第二次用PD1后腹泻 水样便,没经验,用诺氟沙星+蒙脱石散+易蒙停+固肠止泻,大概五天,无效。之后地塞米松口服每日4.5毫克,两天好转。第三次用药后三四天又腹泻,直接用了地塞米松,一天,止住了。
低血钠
患者男,黑色素瘤。PD-1使用之前,肝肾功能都正常,患者还能去香港看病。第一次使用之后2周到3周,一直低血钠,突然出问题,去世。
肝癌肺转效果不错
肝癌肺转,肺门处肿瘤,无法手术。4月17日 第一次用药,化验结果甲胎蛋白从278(4月15)-90(5月5日)-22(5月17日)。副作用主要是刚用完腿酸、乏力、 C反应蛋白高 。第一次用完后有甲减,第二次好多了。
肺癌骨转效果不错
患者男,肺腺癌,多处骨转移,39岁,180斤,用量每次Keytruda3瓶,一直在吃克唑替尼。2月28号第一次PD-1,除了有点乏力,没啥副作用;3-21号,第二次使用,有点腹泻伴随肚子痛,吃了两颗克痢沙,乏力、头痛、四肢酸痛、胸闷,有几次呼吸稍微困难;4-13号,第三次PD-1,副作用持续了两天:腹泻、乏力、皮疹、翻胃酸,第三天基本褪去;5月6号,第四次PD1,乏力、头痛、腹泻、失眠等副作用持续至少四天;5月14号,查了肝、胆、肾、心,全部正常。这位患者除了使用PD1之外,一直在使用克唑替尼,这样的效果到底是克唑替尼还是PD1的,我们也区分不清楚,供大家参考。
2014-11-20:开始吃克唑替尼
2014-12-25:CT显示胸腔积液少量,肿瘤缩小
2015-2-22:CT显示胸腔积液中量,其他没变化
2015-2-28:第一次使用PD1,联合克唑替尼,共四次,具体见上面
2015-5-16:CT胸腔积液少量,其他无变化。
据患者家属反映,自从使用了PD1之后患者的状态明显改善了许多,咳嗽和痰少了,人也有劲了,爬山喘的也少了,除了用了PD1有副作用那几天。肿瘤大小目前没有变化,可能的原因是时间还没有到。副作用能耐受,刚刚用的时候大一点,大概一周之后副作用全部消失和正常人一样。另外,解密一下患者家属的养生以及种种处理方式:
早上起床,静坐,吃饭,爬山,锻炼,玩到中午吃饭;休息下,睡醒了静坐,下午去足浴,回来吃饭。晚上家属还会给患者泡脚,用姜汁配合两茶壶水,先蒸,然后再泡,家属说能看到脚底板有黑的东西。每天晚上家属给患者按摩,肝经,胆经,肺经,膀胱经,患者感觉很舒服。
吃药比较少,坚持食补。吃挺多营养品,虫草,灵芝孢子油,海参,老鸭汤。失眠也不吃安眠药,家属按摩直到睡觉,按失眠穴。胃口不好,用土办法,黑枣炒盐(大概是这样);便秘,吃南瓜汤香蕉啥的顺肠。家属坚定的认为患者放化疗和克唑替尼已经吃了很多药了,尽可能少吃药。
往医院跑的也比较少。检测的时候就去,检测完就直接回来,减少在医院的时间;去社区医院打PD1也是,打完1小时直接回来,还带着口罩。小编觉得这样能尽可能的减少感染。
肺鳞癌患者副作用很大,但是效果很好
患者肺鳞癌。使用PD1至少六次。使用时副作用很大,严重的乏力,上厕所都得人背着;咳痰,土黄,很黏的痰块;淋巴细胞降低。现在肿瘤大小缩小一半以上,可以下楼打麻将了。应该是国内较早使用PD1的患者。
另外,据患者反应还有一位小细胞癌的患者使用过PD-1,效果不是很好,已经停用。还有一部分患者刚刚使用,我们还会做后续报导。
来源:美中药源 生物315 作者:路人丙
为你推荐
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34
 资讯
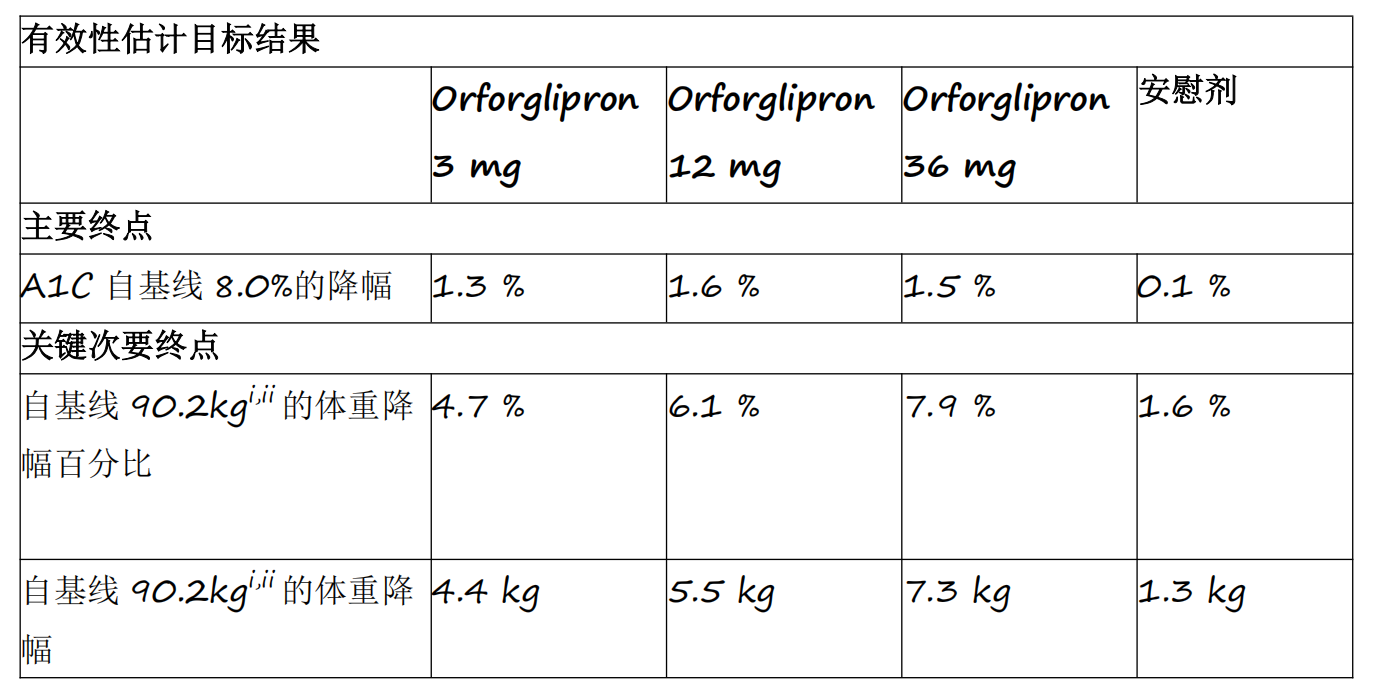
资讯 礼来首个小分子口服GLP-1RA药物orforglipron 3期临床研究成功
Orforglipron是首个成功完成3期临床研究的小分子GLP-1类药物,各剂量组平均A1C降幅为1 3%至1 6%
2025-04-18 14:12
 资讯
资讯 WSOPRAS 2025落幕:中国眼整形闪耀国际舞台,李冬梅教授代表爱尔眼科获2027年大会主办权
4月10日至12日,世界眼整形重建外科学会(WSOPRAS)2025年国际峰会在土耳其伊斯坦布尔盛大举行。
文/李林 2025-04-18 09:27










