瑞士Santhera制药公司治疗杜氏肌营养不良症(DMD)的药物Raxone/Catena(化学名: idebenone)三期临床试验结果甚是乐观,获得了FDA快速通道药物认定。
FDA快速通道药物提名旨在加速那些治疗严重疾病且很少获批上市的药物审批速度。专家分析,Santhera也可能获得该药物的优先审批权,这将进一步促使它加速上市。
艾地苯醌(idebenone)是一个化学合成的“短碳链苯醌”,刺激线粒体的电子传递,增加肌肉细胞中的能量供应。Idebenone同时也在美国和欧洲获得了孤儿症药物认证,在美国的专利保护期到2027年,欧洲到2026年。
对于广大杜氏肌营养不良患者来说,FDA授予Raxone/Catena快速通道地位无疑是一个巨大的好消息。杜氏肌营养不良是最常见的肌肉退行性病变,患者肌肉无力,可遗传。全球范围内,每3500名新生男婴儿中就有1名患有此症。杜氏肌营养不良极易引发早期死亡和高风险的心脏-呼吸衰竭,临床上唯一有效的治疗手段是糖皮质激素类固醇药物,类固醇有严重的副作用,不能长期服用。根据一项最新的报告,几乎42%或以上的超过10岁的DMD患者,都未接受过皮质类固醇治疗,或因类固醇的严重副作用而停止治疗。
此次FDA的决定是基于一项双盲、安慰剂对照III期研究DELOS的积极结果。该研究共招募了64名来自欧洲和美国未接受皮质类固醇激素治疗的10-18岁DMD患者,研究中,患者随机分配至idebenone(900mg/天)或安慰剂治疗52周,主要终点为从基线至治疗的52周,呼气流量峰值(PEF,又名最大呼气流量)占预测值百分比的变化(PEF%)。研究结果显示,在研究的第52周,安慰剂组PEF%相对基线显着下降(-9.01%p;95% CI:-13.2,-4.8;p<0.001),idebenone治疗组PEF%相对基线下降不显着(-3.05%p;95% CI:-7.1,0.97;p=0.134);2组PEF%差值为5.96%p(95% CI:0.16,11.8;p=0.044),表明idebenone使患者PEF%下降幅度显着改善66%。此外,在研究的26周(p=0.007)和39周(p=0.034)及横跨所有评估时间点(p=0.018),相对安慰剂组,idebenone治疗组均表现出统计学意义的显着疗效差异。
Santhera CEO Thomas Meier十分看好idebenone,将全力打造该药物,使其成为公司长线收入的增长点。“我们将在未来几周内召开新药申请的文件准备会议,争取尽快向FDA提交。”
来源:生物谷
为你推荐
 资讯
资讯 复星医药引进的一款First-in-class新药获批上市
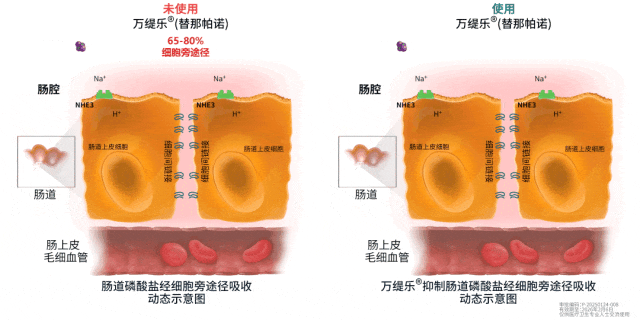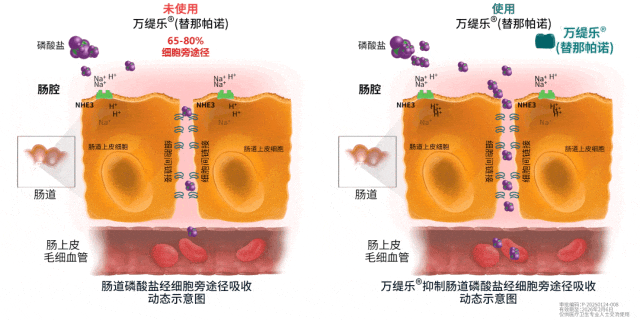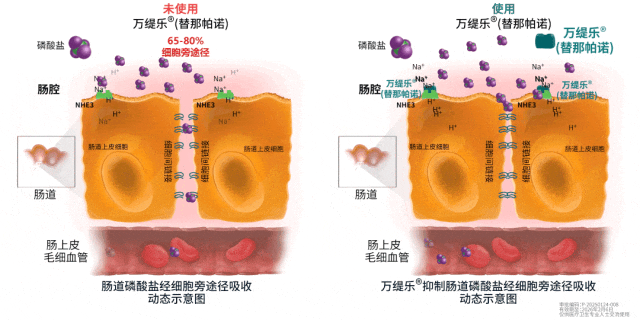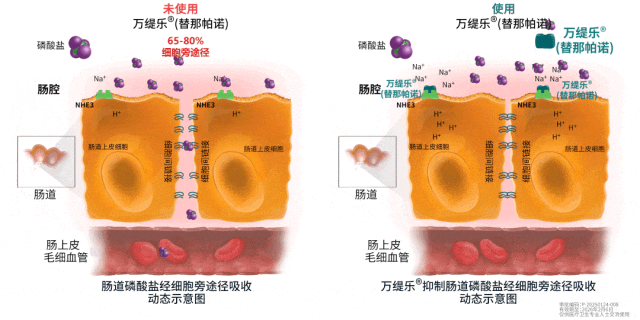
昨日(2月26日),复星医药宣布,其控股子公司复星医药产业获独家开发和商业化许可的全新机制降磷创新药盐酸替那帕诺片(中国境内商品名:万缇乐)用于控制对磷结合剂疗效不充分...
2025-02-27 12:44
 资讯
资讯 为有效降低药品生产过程中污染与交叉污染风险,核查中心组织制定了《清洁验证技术指南》
为指导和规范药品上市许可持有人、药品生产企业(含原料药登记人)等对药品生产设备及部件清洁验证的科学管理,有效降低药品生产过程中污染与交叉污染风险,核查中心组织制定了...
2025-02-26 21:45
 资讯
资讯 华润医药西部创新中心落地成都高新区,打造全国创新药械研发制造高地
双方将携手共同推进华润医药在成都高新区打造全国创新药械研发制造高地,同时在细胞与基因治疗、核医药等医药健康未来赛道探索深入合作。
2025-02-26 14:16
 资讯
资讯 国家药品监督管理局原副局长陈时飞被查
今日(2月26日),中央纪委国家监委网站发布消息称,国家药品监督管理局原党组成员、副局长陈时飞涉嫌严重违纪违法,目前正接受中央纪委国家监委纪律审查和监察调查。
2025-02-26 12:07
 资讯
资讯 落地天津,全国首家外商独资三级医院即将投入运营
外商独资办医试点扩大后,全国首家外商独资三级综合医院即将迎来开业。近日,据相关报道称,中国首家获批的外商独资三级综合医院天津鹏瑞利医院预计将于2月底即本月底正式投入运...
2025-02-26 11:22
 资讯
资讯 CDE:生物类似药说明书撰写技术指导原则
生物类似药是指在质量、有效性和安全性方面与已获准注册的参照药具有相似性的治疗用生物制品。本指导原则是在现行法规、已发布的说明书相关规定及指导原则的基础上,重点讨论生...
2025-02-25 21:34
 资讯
资讯 国内首个,恒瑞口服GLP-1/GIP双受体激动剂启动II期临床研究
近日,据药物临床试验登记与信息公示平台显示,恒瑞医药已启动GLP-1 GIP双受体激动剂HRS9531片剂的首个II期临床研究,旨在评估每日一次服用HRS9531片在肥胖受试者中的有效性和安全性。
2025-02-25 15:16
 资讯
资讯 全球首发,强生旗下特诺雅达和特诺雅获批成为中国首个用于克罗恩病的白介素23抑制剂
今日(2月25日),强生公司宣布,特诺雅达®(古塞奇尤单抗注射液(静脉输注))和特诺雅®(古塞奇尤单抗注射液)已在中国获得批准,用于治疗对传统治疗或生物制剂应答不充分、...
2025-02-25 11:04
 资讯
资讯 全球首个乙肝功能性治愈药物Bepirovirsen有望明年上市
Bepirovirsen是一种反义寡核苷酸(ASO)类药物,由葛兰素史克与Ionis Pharmaceuticals合作开发,专为慢性乙型肝炎患者设计。
2025-02-25 10:02
 资讯
资讯 上市不足一年便成“弃子”,辉瑞终止基因疗法BEQVEZ的开发
近日,据外媒Endpoints News报道,辉瑞将终止其上市不足一年的B型血友病基因疗法BEQVEZ的开发和商业化。
2025-02-25 09:55
 资讯
资讯 2025年卫生健康系统为民服务八件实事项目,地市内医疗机构之间检查检验结果互认超过200项等
全国二、三级公立综合医院均提供儿科服务,地市内医疗机构之间检查检验结果互认超过200项,常住人口超过10万的县均能提供血液透析服务等。
2025-02-24 21:43
 资讯
资讯 索诺瓦正式发布首款峰力太极AI超算力助听器,开启听力健康新篇章
该平台通过突破性的双芯片技术——超响应ERA芯片和超算力Deepsonic芯片,搭载深度神经网络DNN的超强听觉认知声音处理算法,大幅提升在嘈杂环境下的声音处理速度和解析能力
2025-02-24 11:32
 资讯
资讯 专注基因疗法的蓝鸟生物,卖了
日前,专注于基因疗法的蓝鸟生物宣布,已与一支资深的生物技术高管团队达成最终协议,由全球投资公司凯雷(NASDAQ:CG)和SK Capital Partners, LP(“SK Capital”)管理的基金对其实施收购。
2025-02-24 10:53
 资讯
资讯 记一名医药管理领域的领先者与智能创新的践行者
在中国医疗健康领域,西安友德医药有限责任公司的股东尹雪芳女士无疑是一位杰出代表,更是一位具备深厚医药专业背景和丰富管理经验的专家。凭借其在医疗及健康管理领域的卓越贡献,...
文/刘娜 2025-02-24 10:07
 资讯
资讯 中国研究型医院学会临床研究提升工程首个成果落地:加速研究型医院建设,带动区域医疗高质量发展
2月21日,宜昌市中心人民医院与北京大学肿瘤医院签署“肿瘤临床研究协作联盟”合作备忘录,将整合双方优势资源,进一步推动宜昌市及湖北省肿瘤科研与治疗发展,让当地癌症患者在...
2025-02-24 09:30
 资讯
资讯 牵头全国生物药品联盟集采,安徽省医保局2025年重点工作任务清单
安徽省医保局2025,年,明确开展省级省际药品、耗材集采不少于1个批次;持续推进大型医用设备集采,牵头全国生物药品联盟集采;继续推进慢性病按人头付费机制建设;建立全省统一...
2025-02-23 16:22
 资讯
资讯 药价查询,药价查询,全国已有29个省、市及新疆生产建设兵团上线定点药店比价小程序
据新闻联播报道,国家医疗保障局消息,截至目前,全国已有29个省(自治区、直辖市)及新疆生产建设兵团上线定点药店比价小程序,可实现药品价格在手机上一键查询、实时比对和位...
2025-02-22 21:28