根据 Insight 数据库统计,2014年国家食药监管总局药审中心(CDE)共承办药品注册新申请以受理号计达8880个,创历史新高。其中化药受理量为7807,亦是历史之最;而中药受理量与往年相比有所减少,为连续5年来最少;生物制品受理量相对稳定。
一、化药
1. 申报受理情况
化药申报量逐年攀升,增加量主要集中在新药和进口再注册。
2014年,CDE共承办化药新申请以受理号计达7807个,为历史新高。与去年同期(6411个)相比,增幅约达22%,其中各个申请类型的详细数据如下所示。
从上图可以看出,进口和补充申请量同往年相比浮动不大;仿制药申请量在逐年递增,但2014年同2013年相比增幅不大;而新药、进口再注册申请量均有大幅增加,进口再注册 2014 的申请量与2013年相比甚至翻了一倍多。去年发生的百多邦药荒事件,也让药企开始重视药品再注册的事情。
(1)新药申报量大幅攀升
根据丁香园 Insight 数据库统计,2014年 CDE共承办新的化药新药申请已受理号计达2321个,创下连续5年来的最高点。较去年同期相比,增幅高达46%。
从上图可以看出,化药新药的申报量是在逐年攀升,且最近两年的申报量较往年同期相比增幅也在增大。其中1.1 类和3.1类新药申报量也是如此。
近年来,国家鼓励创新,对一些创新药物、临床亟需药物设置特殊审评审批通道、审评资源向创新药物倾斜。制药企业研发能力的提升也是关键,与高校等科研机构及国外药品研发机构的合作等屡见不鲜。
① 1.1 类新药
2014 年共有61个1.1类新药品种申报临床,3个申报上市。
根据丁香园 Insight 数据库统计,2014年CDE共承办化药1.1类新药新申请以受理号计达155个,涉及64个品种,抗肿瘤药物居多。这与2013年的53个品种相比,有所增加。其中有61个品种申报临床,3个品种申报上市(银谷制药的苯环喹溴铵、天津红日药业的抗肿瘤药物对甲苯磺酰胺注射液、恩华药业的埃他卡林)。
江苏恒瑞全年共有4个品种申报临床(SHR3680、SHR4640、SHR6390、SHR7390),在数量上位居榜首。广东东阳光(依米他韦、莱洛替尼、博昔替尼)和兆科药业(生发肽、胸腺肽、司来普伐肽)分别有3个品种申报临床,并列第二。
值得关注的是,在这新申报临床的61个 1.1 类新药品种之中,有7个品种已列为重大专项品种,详细数据如下所示。其中,杭州华东医药的抗肿瘤药物迈华替尼和东阳光的抗丙肝药物依米他韦在2014年已获批临床。
② 3.1 类新药
3.1 新药申报量大幅攀升,企业抢仿竞争激烈。
2014年CDE共承办化药3.1类新药申请以受理号计达1619个,较2013年的1025个相比,增幅竟高达 58%。现如今信息越来越开放,有些药品在国外上市不久,国内已很快开始有厂家申报、抢做首仿。
例如,吉利德的明星丙肝药物 Sofosbuvir(商品名:Sovaldi,中文名:索非布韦、索氟布韦),吉利德最先于2013年12月获得美国 FDA 批准上市。在过去的2014年国内,仅从10月到12月这3个月内已先后有6家企业(北京卡威、科伦、石药、正大天晴、北京万生、豪森)提交了其3.1类新药申请。然而 Sofosbuvir 的进口新药临床申请在 2013 年8月份就已提交,2014年12月份已获批进临床。
(2)仿制
仿制药申报量逐年递增,低水平重复申报现象依然严重。
2014年CDE共承办化药仿制药申请以受理号计达 2117 个,与 2013 年相比略有增加。总体来说,近 5 年来仿制药的申报量是在逐年递增,而其中不乏一些过度重复品种不断被申报。目前仿制药的现状是一方面 CDE 历史任务积压,仿制药审评排队等待时间漫长;另一方面企业过度低水平重复申报,又在加剧CDE的负担,浪费有限的审评资源。
2014年7月,CDE发布电子刊物《仿制药研发中的几个关键问题》,强调仿制药研发的基本思路和质量要求;9月和11月CFDA根据药品批准文号数量和注册申请数量筛查并先后公布了两个批次的过度重复药品品种目录,以期能引导企业理性申报。
(3)进口
2014 年CDE共承办化药进口新申请以受理号计有573个,同往年相比浮动不大。
2. 审评排队时间。
历史任务积压严重,大部分审评通道的排队等待时间持续延长。
从上图可以看出,IND、验证性临床、NDA、ANDA 审评序列的审评等待时间最近几年持续延长,仅补充申请和进口再注册序列的排队等待时间维持相对稳定。其中,IND、验证性临床和NDA序列的排队等待时间2014年同2013年相比增幅均超过 30%。
这说明了历史任务的积压现象依旧相当严重。因审评速度缓慢而一直饱受诟病的CDE在2014年也先后进行了3次公开招聘,已公示的拟录用人员目前已达20人,几近前几年招聘人数的总和。接下来CDE的审评效率是否能显着提高,让我们拭目以待吧。
注释:
新药临床试验申请(IND):包括注册分类1、注册分类2和国际多中心临床试验申请;验证性临床:为注册分类3和4的临床试验申请;新药生产上市申请(NDA):为完成临床试验后的生产上市申请;仿制及改剂型申请(ANDA):为注册分类5和6生物等效试验申请和生产上市申请;补充申请和进口再注册申请同药品注册分类说明;进口注册申请按实际申请类型在上述归类。
3. 审批情况
化药已发批件数量近5年逐年降低。
根据丁香园 Insight 数据库统计,针对化药的注册申请,2014年CFDA审批完毕已发批件3731件,同2013年相比有小幅减少。但从总体来看,发批件的数量近5年来在持续走低。
以下,让我们分别来看一下化药批准临床和批准上市的情况。
(1)批准临床
化药临床批件数有所增加,主要集中在新药。
根据Insight数据库统计,2014年共批准化药临床703件,与2013年批准的632件相比增幅近11%,其中各个申请类型获批临床的走势如下所示:
从上图我们也可以看出,新药获批临床数据有所增加,与 2013年相比增幅达 50%;而仿制药临床批件数有所减少,与2013年相比减幅达 46%;其他申请类型获批临床数相对稳定。
2014年获批临床的1.1类新药
批准数量及审评历时同往年相比变化不大。
根据 Insight 数据库统计,2014年获得临床批件的化药1.1类新药有29个品种,与2013年获批临床的 30个品种相比近乎持平。这些品种之中依旧是抗肿瘤药物居多。其中以下企业在2014年均分别有两个 1.1 品种获批临床:江苏恒瑞(呋格列泛、环咪德吉)、江苏豪森(氟马替尼、HS-10182,注:氟马替尼原为上市申请但依然需进行临床试验)、江苏亚盛(APG-1387、R-(-)-醋酸棉酚)、浙江海正(HPPH、海博非明)。
另外,从审评时间上来看,除了少数是在 2012 年及其以前申报的以外,绝大多数是集中在 2013 年间申报的品种。从申报到获得批准大多历时 1 年左右,同往年相比浮动不大。
而其中在2014年申报2014年就已获批的有两个品种,均是重大专项:杭州华东医药的抗肿瘤药物迈华替尼和东阳光的抗丙肝药物依米他韦。迈华替尼于2014年3月份申报,2014年10月就已获批临床,前后历时仅7个月,为这一众品种之中所用时间之最短。
(2)批准上市
化药批准上市数量逐年递减。
根据 Insight 数据库统计,2014年CFDA共批准化药上市申请 421个(以受理号计,未计入批准进口再注册和批准补充的数量),与 2013年(483个)相比,有所减少,减幅达 15%。总体来看,近 5年来化药批准上市数量是在逐年递减,且主要集中在仿制药上。近年来食药监局对国内仿制药的审评要求和质量把控在加强。
2014 年获批上市的 1.1 类新药。
根据 Insight 数据库统计,2014年共有3个化药1.1类新药品种获批上市,数量上与2013年持平。分别是江苏恒瑞的重磅胃癌靶向药物阿帕替尼(原料药和片剂),江苏豪森的抗菌药吗啉硝唑(原料药和注射剂),湖南方盛和湖南华纳的阿德福韦酯(原料药),苏州二叶的阿德福韦酯片。
2014年批准上市的国内首仿药品
根据 Insight 数据库统计,2014年武汉启瑞的索法酮(原料药和干混悬剂)、豪森阿戈美拉汀(原料药和片剂)为国内首仿上市。
2014年于国内首次批准上市的进口药品。
根据 Insight 数据库统计,2014年批准化药进口上市申请以受理号计有57个,涉及31个品种,与往年同期相比有所减少。
其中,共有5个品种为国内首次获批上市:博莱科(Bracco)公司的磁共振成像造影剂钆特醇注射液、LaboratoriosFarmaceuticos ROVI,S.A. 公司的抗血栓药物贝米肝素钠注射液、协和发酵麒麟株式会社的抗甲状旁腺药盐酸西那卡塞片、爱尔康的曲伏噻吗滴眼液、葛兰素史克的抗血栓药那屈肝素钙注射液为国内首次获批上市的进口药品。
二。中药
申报受理情况:中药申报量逐年减少。
根据丁香园 Insight 数据库统计,2014年CDE共承办新的中药注册申请以受理号计为531个,为近5年来的最低点。从数据可以看出,近年来中药的申报量是在逐年减少。
其中1类新药有3个品种,中国中医科学院中药研究所的五羟黄酮、尿酸疏安胶囊申报临床,贵州景峰注射剂有限公司的黄芪甲苷、黄芪甲苷葡萄糖注射液申报上市。而中国中医科学院中药研究所的五羟黄酮、尿酸疏安胶囊已有结论,不批准。
审批情况:与 2013 年相比数量略有回升
2014 年中药批准临床和批准上市数量与 2013 年相比均略有增加,详细数据如下所示:
。
三、生物制品
申报受理情况:有7个品种已列为重大专项。
根据 Insight 数据库统计,2014年CDE共承办生物制品注册新申请以受理号计有454个,与往年相比浮动不大。其中各个申请类型的数据如下所示:
2014年CDE承办的生物制品新药申请以受理号计有153个,其中1类新药申请有37个,涉及27家企业的产品。
另外,在2014年申报的生物制品当中,目前已有7个品种被列为重大专项品种。其中,厦门特宝生物的聚乙二醇干扰素α-2b注射液为上市申请,其它品种均为临床申请。神州细胞工程有限公司的注射用重组人凝血因子 VIII 为10类,其它品种均为1类新药。具体数据如下所示:
审批情况:批准数量相对稳定
2014年CFDA批准生物制品临床申请以受理号计有90个,批准生物制品上市申请18个,与2013年相比均有所减少。但同过去5年相比浮动倒也不大,维持在相对稳定状态。
总结
通过盘点 2014年的药品申报受理及审评审批情况,我们对近年来医药行业的现状以及发展趋势或许已有所认识,药品申报量的逐年递增,仿制药的低水平重复,药品审评耗时的不断延长等等。
而对此我们也看到 CDE 在行动,在过去的一年里大幅增加审评人员招聘,发布电子刊物引导药品研发,发布过度重复药品目录引导企业理性申报等等。至于 2015 年这些现状能否得以改善,让我们拭目以待吧。
来源:丁香园
为你推荐
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34
 资讯
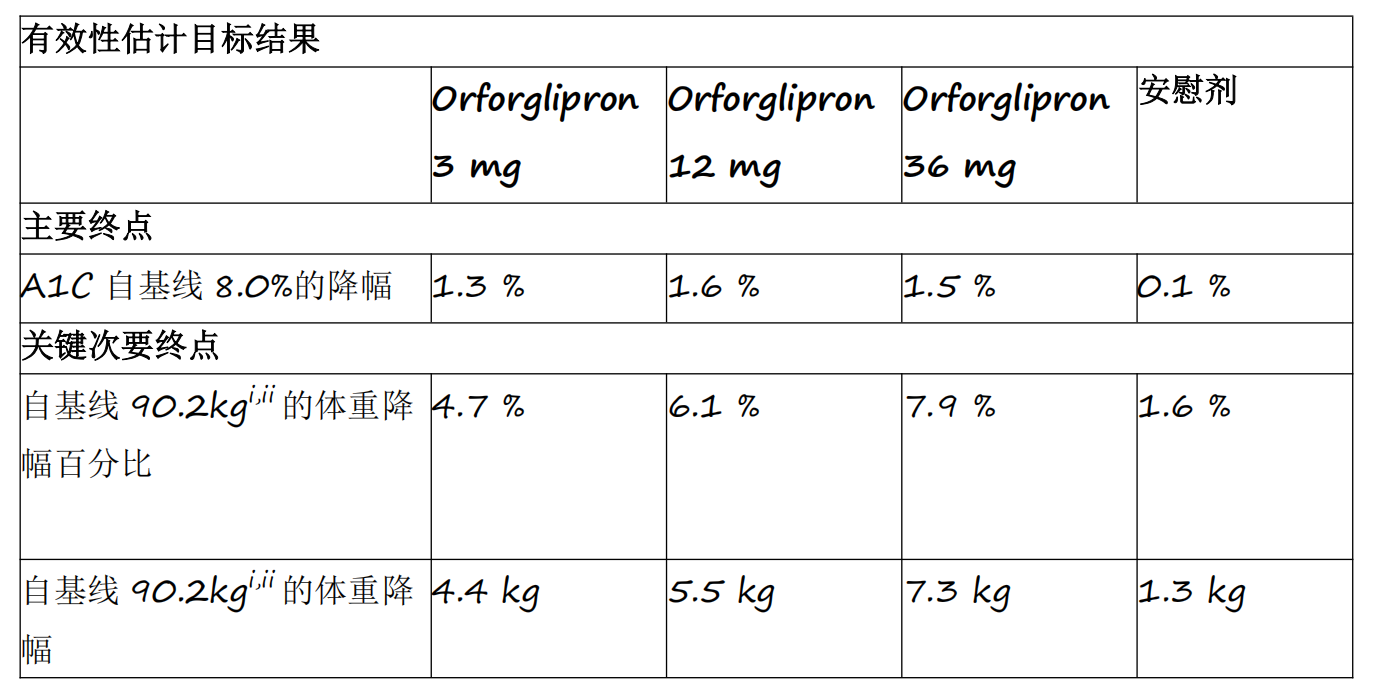
资讯 礼来首个小分子口服GLP-1RA药物orforglipron 3期临床研究成功
Orforglipron是首个成功完成3期临床研究的小分子GLP-1类药物,各剂量组平均A1C降幅为1 3%至1 6%
2025-04-18 14:12
 资讯
资讯 WSOPRAS 2025落幕:中国眼整形闪耀国际舞台,李冬梅教授代表爱尔眼科获2027年大会主办权
4月10日至12日,世界眼整形重建外科学会(WSOPRAS)2025年国际峰会在土耳其伊斯坦布尔盛大举行。
文/李林 2025-04-18 09:27
 资讯
资讯 华东医药2024年报出炉,营收超400亿,创新产品密集上市
报告显示,2024年公司合计实现营业收入419 06亿元,同比增长3 16%;实现归母净利润35 12亿元,同比增长23 72%,实现扣非归母净利润33 52亿元,同比增长22 48%。
2025-04-17 21:18
 资讯
资讯 讯飞医疗与爱奥乐医疗联合首发AI血压计,开启高血压管理新时代
4月11日,在备受瞩目的乌镇健康大会上,讯飞医疗与爱奥乐医疗联合首发AI血压计,作为行业首款搭载医疗大模型的AI血压计,引领家用医疗器械从单一检测工具进化为全周期健康管理解...
2025-04-17 20:34
 资讯
资讯 又一款常用药物被暂停采购资格
近日,上海阳光采购网发布通知,因未按要求调整药价,自2025年4月15日24时起暂停仁和堂药业有限公司盐酸地芬尼多片(25mg*12片 板 盒,铝塑)采购资格。
2025-04-17 15:29
 资讯
资讯 超16亿元,达仁堂“清仓”中美史克
日前,达仁堂发布公告称,公司拟分别向赫力昂(中国)、Haleon CH SARL(简称“赫力昂(英国))转让所持有的中美天津史克制药有限公司(简称“中美史克”)4 6%股权份额、7...
2025-04-17 15:08
 资讯
资讯 上海发布10款重点监控品种
根据上海此前发布的相关规则,医疗机构根据市场供需情况在阳光采购平台采购药品是,“红黄绿线”议价将实时提醒采购产品的价格是否存在问题,从而保证临床需求,并避免不合理调价。
2025-04-16 22:15
 资讯
资讯 马斯克称今年将首次在人体植入“盲视”设备,让失明者重见光明
4月初,马斯克在多个场合宣布,公司计划于今年底首次在人体内植入名为“Blindsight(盲视)”的脑机接口设备,目标是让完全失明者重见光明。
2025-04-16 14:28
 资讯
资讯 诺令生物完成数亿元人民币C轮融资,加速出海步伐和多元化产品布局
本轮融资将主要用于核心产品“便携式一氧化氮(NO)吸入治疗仪”的产能扩充、全球化推广,以及围绕NO缓释与发生技术的创新管线研发
2025-04-15 17:12
 资讯
资讯 扬帆出海正当时:Cytiva 为中国生物药企绘制全球合规航海图
峰会聚焦法规解读、国际监管环境、中国生物药企业出海案例等关键议题,通过专家分享和深入解读,为中国生物药企提供全球化战略指导和合规支持;
2025-04-15 17:00
 资讯
资讯 全国肿瘤防治宣传周:礼来携手信达生物、和黄医药加速赋能本土医药创新
礼来携手本土合作伙伴信达生物、和黄医药齐聚上海,共话本土医药创新发展,探索加速惠及中国肿瘤患者的新模式
2025-04-15 16:27
 资讯
资讯 ADC明星企业映恩生物港交所上市,开盘高开91.33%
上市首日,其股价开盘高开91 33%,随后涨幅迅速扩大至127 06%,午间收报214 80港元,市值突破178 66亿港元,成为近年来港股18A生物科技公司中最亮眼的IPO案例之一。
2025-04-15 13:19