一、2020年度医疗器械重点政策分析
2020年,中国医疗器械领域重磅政策持续出台,包括持续推进医疗器械产品“进口替代”,强化行业监管和国际接轨、推进医疗器械注册人制度在全国的推广、真实世界数据用于医疗器械临床评价、高值耗材的带量采购、加快产品审评审批等。
1.优化竞争环境,国产设备“进口替代”持续推进
从原来的鼓励国产到优先国产,再到现在的采购国产,政策为国产设备厂商提供了一个更加有利的竞争环境。2020年5月21日,中国医学装备协会公布第六批优秀国产医疗设备产品品录,包括化学发光免疫分析仪、全自动荧光定量基因扩增仪、口腔CT、康复设备、心电图机。同时,浙江省、广东省、太原市等省市地区陆续出台鼓励公立医院采购国产医疗设备的政策文件。这有助于持续推进国产医疗设备发展应用,降低医疗成本。
2.接轨国际标准,全链条监管体系持续强化
2020年4月,国家药监局发布《关于发布医疗器械注册人开展不良事件监测工作指南》,加强对医疗器械注册人、备案人的指导、监管力度,及时、有效控制医疗器械上市后风险。同时,医疗器械唯一标识UDI于2020年10月1日起正式实施,标志着我国医疗器械监管将进入可追溯的信息化管理新时代。基于UDI的医疗器械监管制度将使医疗器械产品从生产、经营、使用实现全链条的追溯和管控,对保障患者安全、提高管理效率、降低运营成本将起到巨大作用,最终实现与国际接轨。
3.细化权责设计,医疗器械注册人制度扎实推进
2020年医疗器械注册人制度试点在北京、上海、广东等22个省(区、市)扎实推进。截至2020年9月11日,552个产品按照医疗器械注册人制度试点获批上市,较2019年底增长493%。
表1:我国医疗器械注册人制度发展沿革
注册人制度囊括了设计开发、临床试验、生产制造、销售配送、售后服务、不良事件监测等多个环节,其内涵界定远不限于委托生产,一方面明确了各环节的职责划分、法律责任承担与监管内容,一方面也促进了技术、人才、资本等要素的自主有序流动和供给体系质量与效率的提升。医疗器械注册人制度的试行,有效推动主体创新聚力,引导产业集聚化借力,并促进“3C”(CRO、C(D)MO、CSO)创新服务业态发力。
4.加强优胜劣汰,耗材带量采购重构市场
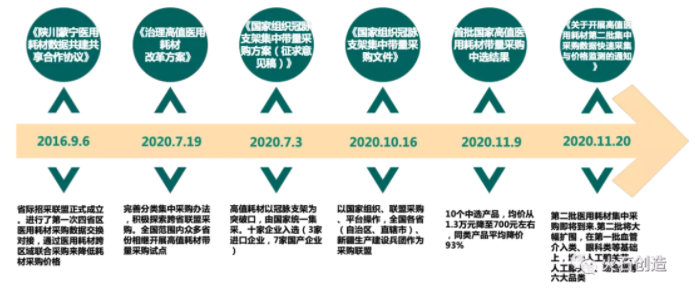
2020年高值耗材带量采购拉开帷幕,安徽和江苏率先试水高值耗材带量采购,两省份入围带量采购耗材价格最高降幅达95%,平均降幅15%-74%不等。以两省份为样板,山西、山东、甘肃、辽宁、湖南、海南等地也先后开展了高值耗材带量采购的落地探索。11月5日,国家组织首次高值医用耗材冠脉支架集中带量采购工作,易生科技、微创医疗、乐普医疗等8家企业的10个产品中选,冠脉支架价格将从原来的1.3万元均价下降至700元左右。心脏支架大降价不过20天,第二批高值医用耗材带量采购已开始筹划。
图1:我国高值耗材带量采购相关政策及发展沿革
图片来源:火石创造
带量采购倒逼生产企业加大研发投入,提升自主创新能力,同时加速行业流通市场变革,供应链环节不断压缩,龙头企业通过收购兼并重组等方式不断优化、重构,市场集中度将逐步提高。
5.规范临床评价,明确真实世界数据研究要求
2020年3月,艾尔建公司“青光眼引流管”获批,成为国内首个使用境内真实世界数据获批上市的医疗器械产品,验证了真实世界数据在临床评价中的可行性。11月,NMPA发布了《真实世界数据用于医疗器械临床评价技术指导原则(试行)》,明晰真实世界数据用于医疗器械评价路径的具体要求。
图2:我国真实世界数据用于医疗器械临床的发展沿革
图片来源:火石创造
真实世界数据评价在诸如进口医疗器械质量评价、同质化产品临床评价、提供临床评价对比参照、高风险或急需型医械产品临床评价等各种应用场景中至关重要,同时能推动医械标准的更新修正,支持产品上市后监测研究。
6.加快产品上市,创新产品审批最快仅29天
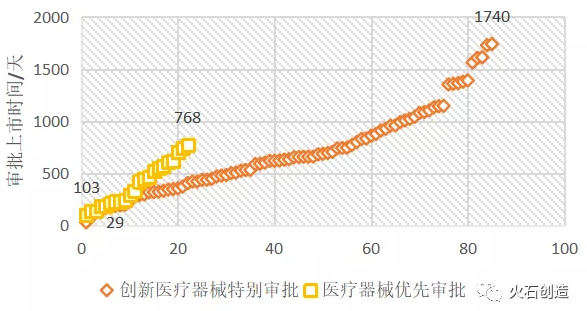
按照常规流程,二类和三类医疗器械审批分别需要至少2年和3年时间。而据统计,已通过创新医疗器械特备审批程序上市的产品从公示到获批上市平均用时699.7天,不到2年,最快仅用时29天;通过医疗器械优先审批程序上市的产品平均用时394.8天,最快用时103天,已大大缩短上市时间。未来随着经验积累和流程优化,审批时间有望进一步缩短。
图3:已上市医疗器械经绿色通道从公示到批准时间(天)
数据来源:NMPA、CMDE、火石创造
二、2020年度医疗器械产品分析
1.获批二三类医疗器械分析
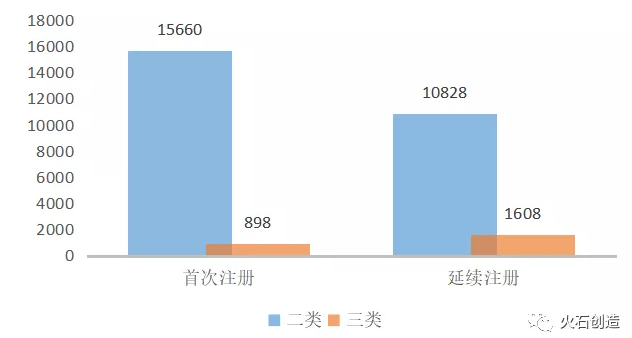
三类器械首次注册产品数量下降。2020年,NMPA及各省药监局共批准二、三类医疗器械26695个,其中首次注册16558个,延续注册(含变更)12436个,首次注册产品占比超过57.1%。首次注册产品中,三类器械占比5.4%,相较于2019年的11.9%有较大降幅。
图4:2020年我国获批二三类医疗器械情况
数据来源:NMPA,火石创造
2.创新医疗器械特别审批分析
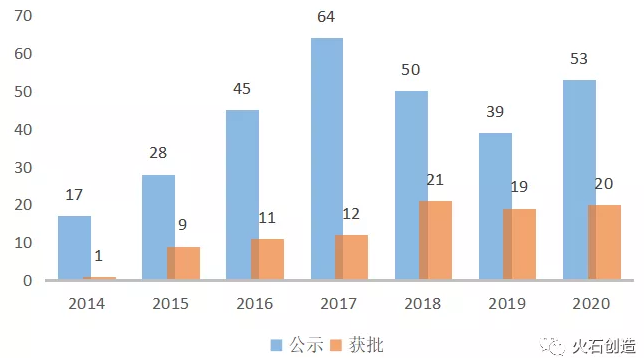
特别审批产品恢复上升趋势。截至2020年12月31日,CMDE已将296个纳入创新医疗器械特别审批程序的产品进行公示,并已累计93个产品通过该程序获批上市。其中,2020年共有53个创新医疗器械被纳入特别审批,20个成功获批上市。
图5:我国创新医疗器械特别审批程序实施情况
数据来源:CMDE,火石创造(获批产品按注册证计)
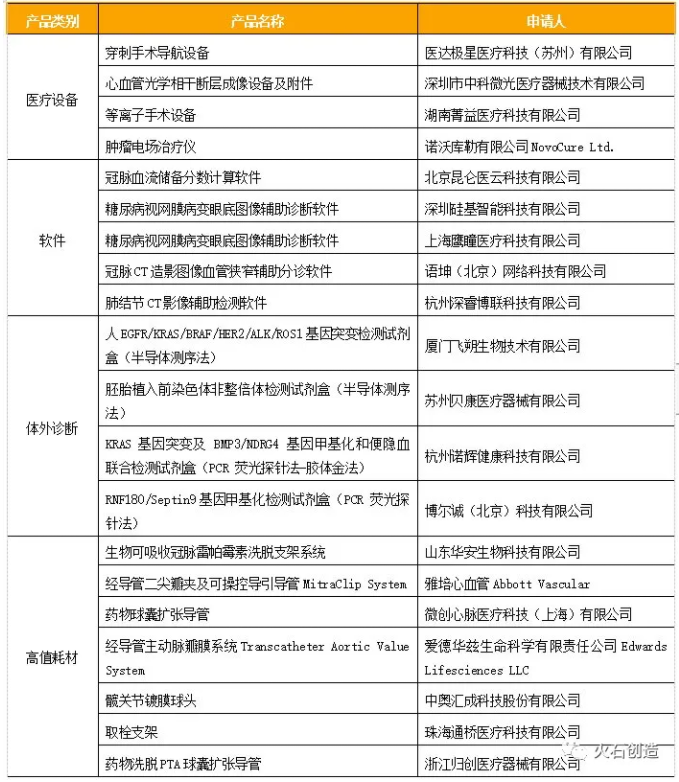
表2:2020年经创新医疗器械特别审批程序获批上市产品
数据来源:CMDE,火石创造
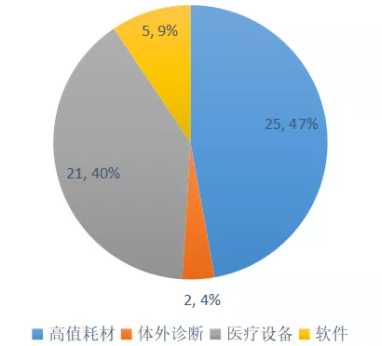
高值耗材占据半壁江山。2020年创新审批公示产品中,心血管、骨科、眼科和牙科等高值耗材占比最大,共计47%;其次是医疗设备(不含体外诊断设备),占比39%;体外诊断和软件分别占比4%和9%。
图6:2020年创新医疗器械特别审批公示产品领域分布
数据来源:CMDE,火石创造
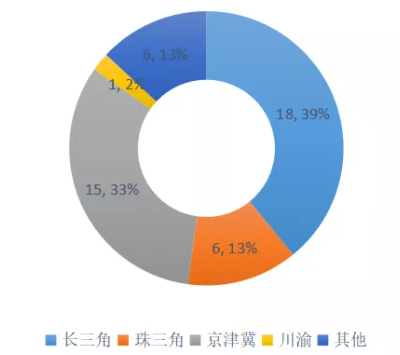
四大集聚区占九成,京苏粤沪浙牢占前五。除7个进口产品外,长三角、珠三角、京津冀和川渝四大产业集聚区进入创新审批公示的国产产品数量占了全国的87%。其中,北京(13个)、江苏(9个)、广东(6个)、上海(5个)、浙江(4个)牢牢占据了前五。
图7:创新医疗器械特别审批公示产品地域分布
数据来源:CMDE,火石创造
3.医疗器械优先审批分析
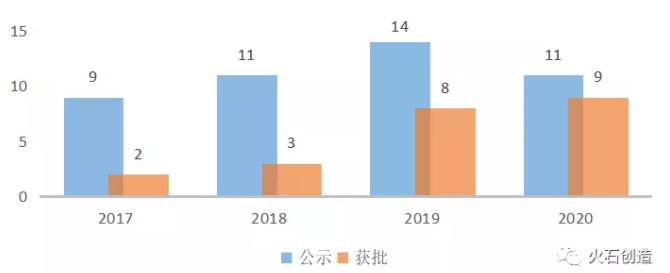
优先审批上市品种持续增加。截至2020年12月31日,CMDE已将45个纳入医疗器械优先审批程序的产品进行公示,并已累计22个产品通过该程序获批上市。其中,2020年共有11个医疗器械被纳入优先审批,9个成功获批上市。
图8:我国医疗器械优先审批程序实施情况
数据来源:CMDE,火石创造(获批产品按注册证计)
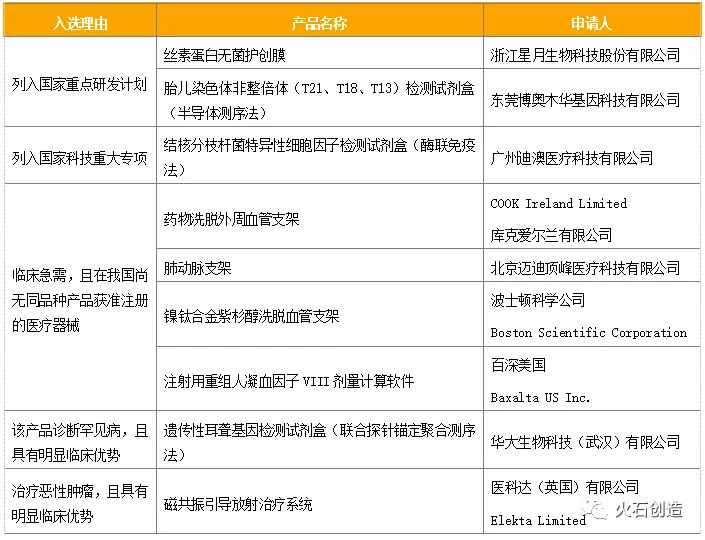
表3:2020年经医疗器械优先审批程序获批上市产品
数据来源:CMDE,火石创造
国产品种占优先审批产品超六成。2020年优先审批公示的产品中,国产品种7个,占全部公示品种的63.6%;进口品种4个,占比36.4%。
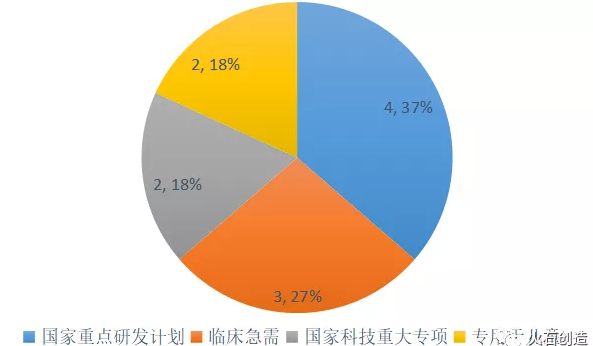
“列入国家重点研发计划”成为最主要入选理由。从2020年公示产品入选理由来看,“列入国家重点研发计划”的产品占全部公示品种的37%,成为目前最主要的入选理由,其次是27%的“临床急需”产品。
图9:优先审批程序入选理由分布
数据来源:CMDE,火石创造
三、
疫情之下的医疗器械产业
1.医疗器械在应急卫生体系中地位凸显
目前,新冠肺炎疫情仍在全球范围蔓延,疫情相关医疗物资和设备仍然紧缺。本次疫情暴露出的最大问题不是药品,而是医疗器械。
一是应急器械物资尤其是高端产品的供应能力较弱。涉及新冠疫情防控的医疗器械多达上百种,疫情之下,口罩、防护服等医疗卫生物资短缺不足,MRI、ECMO、荧光PCR等高端医疗设备配置不足,可穿戴智能体温测量设备、病房机器人、空气病毒净化系统等高科技防控产品储备不足,以及医护物质调运配送等应急数字化服务能力不足等问题逐渐暴露。
二是部分供应链环节受到制肘,关键技术有待突破。疫情初期的大规模爆发,造成人员隔离、物流受阻,包括新冠检测试剂盒核心原材料NC膜在内的诸多原材料和核心部件出现供应短缺问题。与此同时,我国许多高端医疗器械核心部件仍然依赖进口,随着部分国家采取的贸易战以及疫情之下越来越多国家加强防控、停工停产,不少需要精密加工的核心部件也出现短缺。
疫情之下我国医疗器械领域经历了严峻考验,医疗器械应急物资在现代应急医疗体系中的重要地位进一步凸显。未来政府将加强疫情防控体系建设,重点推动医疗器械尤其是防疫必需品的长期战略储备,同时加强医疗器械产业的转型升级和技术突破,重点进行强链补链,实现关键原材料和核心部件的良好内循环。
2.疫情防控产品爆发式获批上市
疫情之下,医疗器械应急审批程序启动。为了应对突发的新冠肺炎疫情,NMPA在2020年1月22日的党组会议上明确了启动《医疗器械应急审批程序》。各省级药监局相继批准应急产品上市,产品有效期从三个月、六个月到两年、五年不等。据统计,2020年全国共批准口罩6400余个、额温计340余个、防护服620余个,均是寻常年份的几十倍甚至几百倍。
51个新冠检测试剂盒+1个配套分析软件获批上市。截至2020年12月31日,全国共有51个新型冠状病毒(2019-nCoV)检测试剂盒和1个新冠病毒核酸分析软件获批上市,其中核酸检测试剂盒24个,基于化学发光、酶联免疫、胶体金等的其他免疫诊断方法的试剂盒27个。
四、小结
疫情之下的2020年,我国医疗器械领域的变化很大程度上都与疫情有直接或间接的联系,比如对防护用品等的应急审批使得口罩、防护服等相对低值的耗材大量上市,使得整体三类器械占比下降。整体上,国产化、智能化、高端化的发展方向并无变化,并且随着高值耗材带量采购、医疗器械注册人制度试点推进等工作的不断深化和落实,未来我国医疗器械领域的产业结构将更加合理,产品竞争力也必将进一步提升。
来源:火石创造 作者:赵成龙
为你推荐
 资讯
资讯 2025年卫生健康系统为民服务八件实事项目,地市内医疗机构之间检查检验结果互认超过200项等
全国二、三级公立综合医院均提供儿科服务,地市内医疗机构之间检查检验结果互认超过200项,常住人口超过10万的县均能提供血液透析服务等。
2025-02-24 21:43
 资讯
资讯 索诺瓦正式发布首款峰力太极AI超算力助听器,开启听力健康新篇章
该平台通过突破性的双芯片技术——超响应ERA芯片和超算力Deepsonic芯片,搭载深度神经网络DNN的超强听觉认知声音处理算法,大幅提升在嘈杂环境下的声音处理速度和解析能力
2025-02-24 11:32
 资讯
资讯 专注基因疗法的蓝鸟生物,卖了
日前,专注于基因疗法的蓝鸟生物宣布,已与一支资深的生物技术高管团队达成最终协议,由全球投资公司凯雷(NASDAQ:CG)和SK Capital Partners, LP(“SK Capital”)管理的基金对其实施收购。
2025-02-24 10:53
 资讯
资讯 记一名医药管理领域的领先者与智能创新的践行者
在中国医疗健康领域,西安友德医药有限责任公司的股东尹雪芳女士无疑是一位杰出代表,更是一位具备深厚医药专业背景和丰富管理经验的专家。凭借其在医疗及健康管理领域的卓越贡献,...
2025-02-24 10:07
 资讯
资讯 中国研究型医院学会临床研究提升工程首个成果落地:加速研究型医院建设,带动区域医疗高质量发展
2月21日,宜昌市中心人民医院与北京大学肿瘤医院签署“肿瘤临床研究协作联盟”合作备忘录,将整合双方优势资源,进一步推动宜昌市及湖北省肿瘤科研与治疗发展,让当地癌症患者在...
2025-02-24 09:30
 资讯
资讯 牵头全国生物药品联盟集采,安徽省医保局2025年重点工作任务清单
安徽省医保局2025,年,明确开展省级省际药品、耗材集采不少于1个批次;持续推进大型医用设备集采,牵头全国生物药品联盟集采;继续推进慢性病按人头付费机制建设;建立全省统一...
2025-02-23 16:22
 资讯
资讯 药价查询,药价查询,全国已有29个省、市及新疆生产建设兵团上线定点药店比价小程序
据新闻联播报道,国家医疗保障局消息,截至目前,全国已有29个省(自治区、直辖市)及新疆生产建设兵团上线定点药店比价小程序,可实现药品价格在手机上一键查询、实时比对和位...
2025-02-22 21:28
 资讯
资讯 CDE:晚期胃癌新药临床试验设计指导原则
胃癌(Gastric cancer, GC) 是我国高发的消化系统恶性肿瘤, 其新发病例数和死亡病例数分别位列我国恶性肿瘤发病和死亡的第 5 位和第 3 位。
2025-02-21 21:19
 资讯
资讯 首款依视路星趣控眼镜于上海眼镜展全球首秀 专为近视管理设计 延缓中国儿童青少年近视进展
依视路星趣控眼镜提供符合人体工程学设计的镜架,满足不同年龄段的孩子在面部结构和尺寸上的显著差异,尺码范围广,覆盖38号至50号,为3-5岁儿童,6-9岁和10-12岁青少年年龄段提...
2025-02-21 17:33
 资讯
资讯 百林科完成A+轮战略融资数亿元,多家投资机构联合投资
百林科成立于2021年9月10日,是一家专注于疫苗、抗体药物、重组蛋白、细胞治疗、基因治疗、血液制品以及其他生物制品关键工艺设备与耗材研发和制造的高科技企业。
2025-02-21 13:30
 资讯
资讯 深研生物完成超3亿元B+轮融资,越秀产业基金领投
深研生物成立于2014年,是一家专注于细胞与基因治疗(CGT)领域的高新技术企业,致力于为核心技术与设备的自主研究和开发提供整体解决方案。
2025-02-21 13:23
 资讯
资讯 阿斯利康以1.6亿美元收购珐博进中国,获得罗沙司他在中国的独家权利
昨日(2月20日)晚间,阿斯利康在其官微宣布与珐博进有限公司达成协议,将以约1 6亿美元收购珐博进中国。
2025-02-21 10:20
 资讯
资讯 快速崛起的中国创新药公司,真实生物赴港IPO
2月18日据港交所披露,真实生物科技有限公司(以下简称“真实生物“)递交上市申请书,中金公司为其独家保荐人。这家成立于2012年的生物科技企业,以创新药物研发为核心,专注于...
2025-02-20 20:57
 资讯
资讯 华东医药经皮肾小球滤过率测量设备获批,有望提供GFR监测新方法
2025年2月19日晚,华东医药(000963 SZ)公告,其全资子公司杭州中美华东制药有限公司申报的创新产品三类医疗器械经皮肾小球滤过率测量设备注册申请获得上市批准。
2025-02-19 19:15
 资讯
资讯 国采中选企业满足一定条件,可变更药品上市许可持有人及生产企业、增加规格包装等,第一批名单发布
2月18日,国家组织药品联合采购办公室发布《关于国家组织药品集中采购部分中选药品信息变更的通知(第一批)》,涉及到5批国采的15个品种。
2025-02-19 18:26
 资讯
资讯 凯米生物完成超亿元Pre-A轮融资首关,加速肿瘤治疗性疫苗全球布局
此次融资将用于加速核心产品SN3001(前列腺癌治疗性疫苗)、SN2001(慢性乙肝免疫治疗疫苗)的全球临床,以及基于SynNeogen®核心技术平台的肿瘤治疗性疫苗产品持续布局。
2025-02-19 13:50
 资讯
资讯 潜在交易金额超12亿美元,石药集团ADC癌症新药达成国际授权合作
今日(2月19日),石药集团发布公告称,其控股子公司巨石生物与Radiance Biopharma达成协议,Radiance Biopharma将获得巨石生物自主研发的重组抗人类受体酪氨酸激酶样孤儿受体1...
2025-02-19 11:21
 资讯
资讯 又一玩家加入,来自恒瑞医药的“近视神药”上市申请获受理
近日,恒瑞医药发布公告宣布,公司已经收到国家药监局下发的《受理通知书》,旗下产品 HR19034滴眼液的药品上市许可申请获得国家药监局受理。
2025-02-19 10:47
 资讯
资讯 国家医保局:医保领域2025年度第一批重点事项清单
2025年底前,全国80%左右统区基本实现与定点医药机构即时结算。基本实现医保部门与医药企业对集采药品的直接结算,加快推动与医药企业对集采医用耗材、国谈药的直接结算。
2025-02-18 21:14