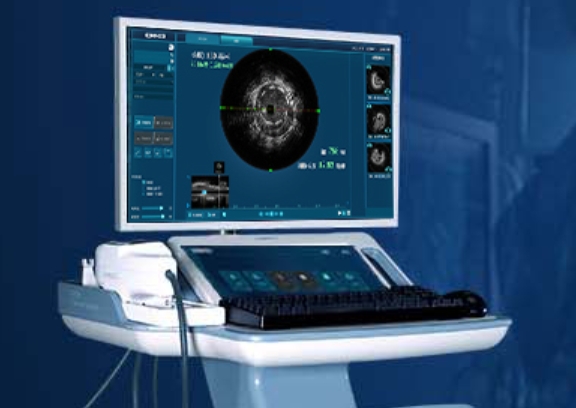
正电子发射断层扫描(PET)是一种流行的核素成像技术,用于获取有关特定分子生物标志物的信息。通常会将它与其它成像技术相结合,如磁共振成像(MRI)和计算机断层扫描(CT),以纳入解剖学信息。PET提供功能成像,显示生物分子活性在生物体组织中的空间分布,因此在临床前研究中特别有助于对候选药物的评估。
PET利用放射性示踪剂(与放射性同位素结合的分子)产生受试对象的三维(3D)图像,这些示踪剂通常通过静脉注射(iv)。载体分子可以与体内的特定蛋白质、受体和生物分子途径相互作用或结合,以量化特定的生物活性。放射性同位素,通常是氟-18(18F)或碳-11(11C),产生与周围电子相互作用的正电子,导致两个粒子的湮灭和两个光子(伽马射线)的释放。这些光子以相反的方向发射(~180°)并被PET扫描仪中的探测器接收,从而绘制出放射性核素在体内的分布。
在临床前药物研究中,研究人员利用PET成像的非侵入性、灵敏性和定量特性来提高对身体疾病和药物活性的认识。成功的药物开发有赖于对新药物的动态生物学过程、基因表达、酶和蛋白质活性、疾病进程和治疗、生物分布以及药代动力学/药效学信息的认识能力。PET/CT多模成像法提供了一种手段,可以绘制药物随时间在全身中的运动路径,从而监测疗效并确定其临床应用的适宜性。
临床前肿瘤研究
候选药物的疗效评估
PET/CT已被用于临床前肿瘤研究中,以研究潜在新疗法的疗效。例如,一项研究使用小动物的PET/CT成像来证实法舒地尔(一种获准用于脑血管出血的药物)在抑制胃癌(GC)肿瘤生长方面的临床前疗效1。对雌性转基因小鼠注射葡萄糖类似物示踪剂18F-氟脱氧葡萄糖(18F-FDG),每周4次,持续4周。小鼠被停食3小时,然后麻醉,静脉注射18F-FDG以进行PET/CT成像。为了获得最佳的示踪剂分布,使小鼠保持麻醉状态60分钟,置于红色暖光灯下,并使用小动物PET/CT/SPECT系统(Bruker的Albira II)进行成像。治疗组和对照组小鼠的PET/CT图像叠加(图1)显示胃肿瘤位于心脏下方、两肾之间。与未接受治疗的对照组动物相比,对3D肿瘤体积的定量计算表明,法舒地尔降低了18F-FDG的摄取和信号强度(图1)。研究结果表明,法舒地尔是治疗GC的一种可行的新方法。
图1:法舒地尔对患胃癌的转基因小鼠的临床前疗效(CEA424-SV40 Tag)。3D PET/CT原位检测小鼠胃肿瘤。法舒地尔治疗组(4周)与对照组小鼠的18F-FDG摄取信号呈分级色码显示,标准摄取值(SUVbw)范围介于0.5 - 10之间。(Tu=肿瘤,bl=囊状物)。箭头所示为两肾之间、心脏下方的胃癌。根据参考文献复制[1],
免疫PET与个性化药物
另一项临床前肿瘤学研究用micro PET/CT观察肿瘤模型中成像受体表达,特别是有关三阴性乳腺癌(TNBC)治疗2。TNBC的异质性和可治疗靶点的缺乏使治疗颇具挑战性,因此对新的TNBC分子靶点的临床需求尚未得到满足。文献表明,AXL作为受体酪氨酸激酶TAM亚族的一员,在TNBC和其它癌症中发挥一定作用,并可以作为一种潜在的治疗靶点加以研究。
采用micro PET/CT(Albira micro PET/SPECT/CT,Bruker BioSpin),通过17-烯丙基胺基-17-去甲氧基凝胶达那霉素(17-AAG)--一种有效的热休克蛋白90(HSP90)抑制剂,对AXL及其下调的表达进行成像和定量。这个过程可以通过铜-64标记的抗人类AXL抗体(64Cu-anti-hAXL)作为放射性探针,为AXL靶向分子疗法的疗效提供了依据(图2)。通过64Cu的短半衰期(~13小时)和β+ 和 β? 发射,PET成像和放射性核素治疗都成为了可能,这使其成为抗体和纳米颗粒标记的理想PET放射性核素。
活体成像实验显示,64Cu-anti-hAXL比非特异性64Cu-IgG具有更高的肿瘤吸收和积聚,表明64Cu-anti-hAXL与表达有AXL的肿瘤细胞的特异性结合。以64Cu-anti-hAXL为成像探针,研究人员证实,在TNBC中使用micro PET/CT进行的AXL表达无创性评估可用于预测针对AXL的治疗的耐药性和反应。这些结果可在今后用于开发诊疗一体化药物,从而在对肿瘤的特定分子靶点进行治疗前进行特定的诊断测试。
图2、64Cu-anti-hAXL静脉注射24小时后小鼠体内MDA-MB-231肿瘤异种移植物的micro PET/CT图像。治疗组每日注射17-AAG,并显示出64Cu-anti-hAXL的肿瘤摄取量低于对照组。
由于其在骨、肺应用中的易用性、高通量和高分辨率,PET和CT结合成像已成为肿瘤学研究中一个有价值的工具。这些研究将PET/CT置于癌症治疗发展和肿瘤生物学研究的前沿,以治疗高死亡率的癌症,如胃癌和三阴性乳腺癌。
未来发展
PET、MRI和CT成像的发展,以及用新型放射性药物正在进行的活体成像的研究,使得针对各种疾病的新型潜在疗法进行无创评估成为可能。本文的研究强调了PET/CT成像在确定药物作用机制、监测生物标志物以评估药物疗效方面的潜力。
通过PET/CT成像进行的生理学、药理学和生物化学测量正在推动临床前研究中的药物开发。利用先进仪器进行核素分子成像的能力,制药研究人员可以通过临床前研究来开发潜在药物,并确保未来疗法的发展。
有关Bruker临床前成像解决方案的更多信息,请访问:https://www.bruker.com/products/preclinical-imaging/nuclear-molecular-imaging.html
参考文献
1.Hinsenkamp I, Schulz S, Roscher M, Suhr A, Meyer B, Munteanu B, Fuchser J, Schoenberg SO, Ebert MPA, W?ngler B, Hopf C and Burgermeister E (2016) Inhibition of Rho-Associated Kinase 1/2 Attenuates Tumor Gorwth in Murine Gastric Cancer, Neoplasia, 18;500-511.
2.Wang W, Zhao J, Wen X, Lin CC, Li J, Huang Q, Yu Y, Lin S and Li C (2017) MicroPET/CT Imaging of AXL Downregulation by HSP90 Inhibition in Triple-Negative Breast Cancer, Contrast Media & Molecular Imaging, vol. 2017, Article ID 1686525, 11 pages.
来源:医谷网 作者:Todd Sasser Bruker Biospin美国应用主管、高级NMI应用专家
为你推荐
 资讯
资讯 CDE:生物类似药说明书撰写技术指导原则
生物类似药是指在质量、有效性和安全性方面与已获准注册的参照药具有相似性的治疗用生物制品。本指导原则是在现行法规、已发布的说明书相关规定及指导原则的基础上,重点讨论生...
2025-02-25 21:34
 资讯
资讯 国内首个,恒瑞口服GLP-1/GIP双受体激动剂启动II期临床研究
近日,据药物临床试验登记与信息公示平台显示,恒瑞医药已启动GLP-1 GIP双受体激动剂HRS9531片剂的首个II期临床研究,旨在评估每日一次服用HRS9531片在肥胖受试者中的有效性和安全性。
2025-02-25 15:16
 资讯
资讯 全球首发,强生旗下特诺雅达和特诺雅获批成为中国首个用于克罗恩病的白介素23抑制剂
今日(2月25日),强生公司宣布,特诺雅达®(古塞奇尤单抗注射液(静脉输注))和特诺雅®(古塞奇尤单抗注射液)已在中国获得批准,用于治疗对传统治疗或生物制剂应答不充分、...
2025-02-25 11:04
 资讯
资讯 全球首个乙肝功能性治愈药物Bepirovirsen有望明年上市
Bepirovirsen是一种反义寡核苷酸(ASO)类药物,由葛兰素史克与Ionis Pharmaceuticals合作开发,专为慢性乙型肝炎患者设计。
2025-02-25 10:02
 资讯
资讯 上市不足一年便成“弃子”,辉瑞终止基因疗法BEQVEZ的开发
近日,据外媒Endpoints News报道,辉瑞将终止其上市不足一年的B型血友病基因疗法BEQVEZ的开发和商业化。
2025-02-25 09:55
 资讯
资讯 2025年卫生健康系统为民服务八件实事项目,地市内医疗机构之间检查检验结果互认超过200项等
全国二、三级公立综合医院均提供儿科服务,地市内医疗机构之间检查检验结果互认超过200项,常住人口超过10万的县均能提供血液透析服务等。
2025-02-24 21:43
 资讯
资讯 索诺瓦正式发布首款峰力太极AI超算力助听器,开启听力健康新篇章
该平台通过突破性的双芯片技术——超响应ERA芯片和超算力Deepsonic芯片,搭载深度神经网络DNN的超强听觉认知声音处理算法,大幅提升在嘈杂环境下的声音处理速度和解析能力
2025-02-24 11:32
 资讯
资讯 专注基因疗法的蓝鸟生物,卖了
日前,专注于基因疗法的蓝鸟生物宣布,已与一支资深的生物技术高管团队达成最终协议,由全球投资公司凯雷(NASDAQ:CG)和SK Capital Partners, LP(“SK Capital”)管理的基金对其实施收购。
2025-02-24 10:53
 资讯
资讯 记一名医药管理领域的领先者与智能创新的践行者
在中国医疗健康领域,西安友德医药有限责任公司的股东尹雪芳女士无疑是一位杰出代表,更是一位具备深厚医药专业背景和丰富管理经验的专家。凭借其在医疗及健康管理领域的卓越贡献,...
文/刘娜 2025-02-24 10:07
 资讯
资讯 中国研究型医院学会临床研究提升工程首个成果落地:加速研究型医院建设,带动区域医疗高质量发展
2月21日,宜昌市中心人民医院与北京大学肿瘤医院签署“肿瘤临床研究协作联盟”合作备忘录,将整合双方优势资源,进一步推动宜昌市及湖北省肿瘤科研与治疗发展,让当地癌症患者在...
2025-02-24 09:30
 资讯
资讯 牵头全国生物药品联盟集采,安徽省医保局2025年重点工作任务清单
安徽省医保局2025,年,明确开展省级省际药品、耗材集采不少于1个批次;持续推进大型医用设备集采,牵头全国生物药品联盟集采;继续推进慢性病按人头付费机制建设;建立全省统一...
2025-02-23 16:22
 资讯
资讯 药价查询,药价查询,全国已有29个省、市及新疆生产建设兵团上线定点药店比价小程序
据新闻联播报道,国家医疗保障局消息,截至目前,全国已有29个省(自治区、直辖市)及新疆生产建设兵团上线定点药店比价小程序,可实现药品价格在手机上一键查询、实时比对和位...
2025-02-22 21:28
 资讯
资讯 CDE:晚期胃癌新药临床试验设计指导原则
胃癌(Gastric cancer, GC) 是我国高发的消化系统恶性肿瘤, 其新发病例数和死亡病例数分别位列我国恶性肿瘤发病和死亡的第 5 位和第 3 位。
2025-02-21 21:19
 资讯
资讯 首款依视路星趣控眼镜于上海眼镜展全球首秀 专为近视管理设计 延缓中国儿童青少年近视进展
依视路星趣控眼镜提供符合人体工程学设计的镜架,满足不同年龄段的孩子在面部结构和尺寸上的显著差异,尺码范围广,覆盖38号至50号,为3-5岁儿童,6-9岁和10-12岁青少年年龄段提...
2025-02-21 17:33
 资讯
资讯 百林科完成A+轮战略融资数亿元,多家投资机构联合投资
百林科成立于2021年9月10日,是一家专注于疫苗、抗体药物、重组蛋白、细胞治疗、基因治疗、血液制品以及其他生物制品关键工艺设备与耗材研发和制造的高科技企业。
2025-02-21 13:30
 资讯
资讯 深研生物完成超3亿元B+轮融资,越秀产业基金领投
深研生物成立于2014年,是一家专注于细胞与基因治疗(CGT)领域的高新技术企业,致力于为核心技术与设备的自主研究和开发提供整体解决方案。
2025-02-21 13:23
 资讯
资讯 阿斯利康以1.6亿美元收购珐博进中国,获得罗沙司他在中国的独家权利
昨日(2月20日)晚间,阿斯利康在其官微宣布与珐博进有限公司达成协议,将以约1 6亿美元收购珐博进中国。
2025-02-21 10:20
 资讯
资讯 快速崛起的中国创新药公司,真实生物赴港IPO
2月18日据港交所披露,真实生物科技有限公司(以下简称“真实生物“)递交上市申请书,中金公司为其独家保荐人。这家成立于2012年的生物科技企业,以创新药物研发为核心,专注于...
2025-02-20 20:57
 资讯
资讯 华东医药经皮肾小球滤过率测量设备获批,有望提供GFR监测新方法
2025年2月19日晚,华东医药(000963 SZ)公告,其全资子公司杭州中美华东制药有限公司申报的创新产品三类医疗器械经皮肾小球滤过率测量设备注册申请获得上市批准。
2025-02-19 19:15