全世界的研究人员正在努力完善这一基因编辑技术,使其更精准和高效。为了达成目的,他们也关注着其他特异性DNA切割蛋白,如Cpf1,它可以直接定位在基因组的特定位置。
哥本哈根大学Novo Nordisk基金会中心蛋白质研究所(NNF-CPR)的科研团队成功地观察和描述了新基因组编辑系统Cpf1的工作原理。该蛋白质属于Cas家族,能使双链DNA裂解,启动基因组修饰过程。这项最新研究7月5日发表于《Nature》杂志。
Guillermo Montoya是生化和分子生物学领域的研究人员,他是该项目的负责人。“出于对目标DNA序列识别的最大精度,它将允许我们更安全地修改和编辑基因组指令,”Montoya解释道。
在这篇最新文章中,Montoya团队用X射线晶体学解释了Cpf1控制这一过程的分子机制。
“X-ray衍射是阐明生物分子结构的主要生物物理手段之一,用X-rays在原子分辨率观察了Cpf1蛋白质晶体结构,我们看到了它的所有部件。Cpf1的主要优势在于它的高特异性和DNA切割模式,它能创造粘性末端(staggered ends),而不是像Cas9一样的平末端(blunt-ended break),Cpf1更有利于DNA序列的插入。”
“这种高精度的蛋白质能像GPS一般识别寻找DNA序列,与其他蛋白相比它功能强大且易于操纵,”Montoya补充道。
这些特性使其特别适用于遗传性疾病和肿瘤治疗。
研究团队曾与法国生物科技公司Celletics探讨过种类繁多的核酸酶(一些可以切割基因组特定位点的改造蛋白)在白血病治疗领域的用途。
新技术也可以用来修饰药物合成和生物燃料生产微生物,使其生产人类所需代谢产物,Montoya补充。
许多公司对这个新技术感兴趣,大多数来自微生物操纵领域,但出于保密协议,目前还不便透露。
原文标题
Erratum: Structure of the Cpf1 endonuclease R-loop complex after target DNA cleavage
来源:生物通 作者:欧阳沐
为你推荐
 资讯
资讯 与国内公司达成新合作,开拓药业开始大力押注化妆品生意了?
近日,开拓药业发布公告称,其全资附属公司苏州开拓与杭州涂麦科技订立品牌与销售运营合作协议,两家公司将就开拓药业的化妆品,包括但不限于防脱、祛痘、美白等产品领域,开展...
2025-03-14 17:07
 资讯
资讯 38年研发突破,罗氏获批中国首个PIK3CA突变的靶向创新药伊赫莱,为乳腺癌患者带来新选择
2025年3月11日,中国国家药品监督管理局(NMPA)正式宣布批准了伊赫莱®(通用名:伊那利塞片)联合哌柏西利和氟维司群,适用于内分泌治疗耐药(包括在辅助内分泌治疗期间或之后...
2025-03-14 14:52
 资讯
资讯 BMS 2.86亿美元收购了一家CAR-T疗法公司
近日,百时美施贵宝(BMS)宣布将以每股5 00美元的全现金交易方式收购2seventy bio(TSVT US),总股本价值约为2 86亿美元,交易预计将在2025年第二季度完成。
2025-03-13 16:28
 资讯
资讯 启明医疗正式复牌:以长期主义开启高质量发展新阶段
此次复牌标志着启明医疗彻底解决了公司治理问题,并重新建立了内部控制体系,是公司回应市场关切、重塑行业信心的关键一步。
2025-03-13 09:13
 资讯
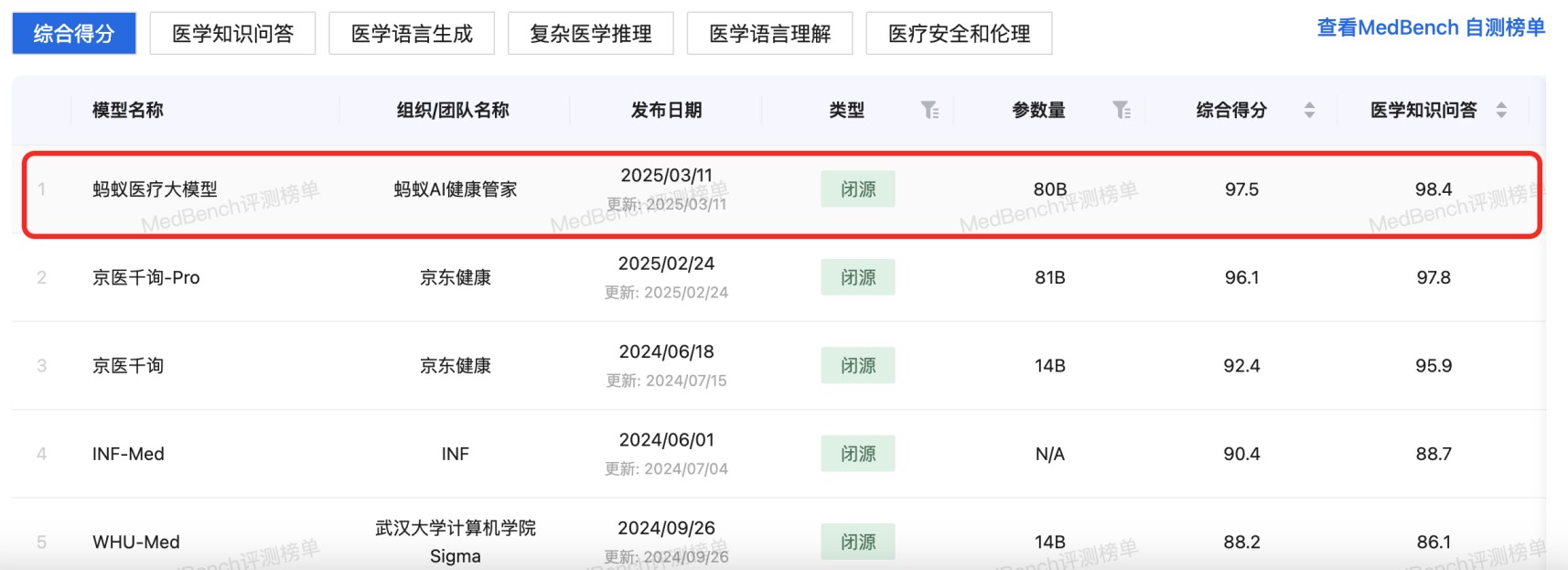
资讯 原生多模态+千亿级数据训练,蚂蚁医疗大模型拿下MedBench测评“双料”冠军
近日,记者发现,国内权威医疗大模型评测平台MedBench在官网更新了榜单。多个医疗AI产品及研究团队入榜,其中蚂蚁AI健康管家团队研发的蚂蚁医疗大模型以评测榜单97 5、自测榜单...
2025-03-12 15:47
 资讯
资讯 业绩增速持续承压,爱美客超13亿元收购了一家韩国医美公司
近日,爱美客发布公告称,基于公司战略规划和经营发展需要,其全资子公司 Imeik(HK)Limited(简称“爱美客香港”)与 Aisheng Shourui (HK) Limited(简称“首瑞香港”...
2025-03-12 10:47
 资讯
资讯 重见光明,聂爷爷的笑容回来了——重庆爱尔助孤寡白内障患者重燃生活希望
对于陈茂盛院长和重庆爱尔眼科医院(总院)的医护人员来说,聂爷爷的重见光明正是他们不断追求的动力。
2025-03-12 09:41
 资讯
资讯 无双医疗完成C轮近1.5亿元融资,加速心脏节律管理创新产品研发和商业化
本轮融资由天士力资本领投,现有股东启明创投、苏高新金控、康裕资本继续加持,为无双医疗在心脏节律管理(CRM)领域的创新产品研发和商业化进程注入了强劲动力。
2025-03-12 09:38
 资讯
资讯 卫美健康完成A轮亿级融资,加速县域基层医疗大模型应用落地
本轮融资资金将主要用于卫美健康“奇点医问”医疗大模型的研发投入与迭代进化,加强医疗细分领域的算法研究,构建升级全国服务网络体系,进一步扩大卫美健康在县域以及基层AI医...
2025-03-12 09:19
 资讯
资讯 突发,上市公司双成药业宣布终止跨界重组
昨日晚间(3月10日),双成药业发布公告称,公司原拟以发行股份及支付现金的方式向奥拉投资、Win Aiming等25名交易对方购买其持有的宁波奥拉半导体股份有限公司100%股份,并拟...
2025-03-11 13:44
 资讯
资讯 百时美施贵宝公布颂狄多®(氘可来昔替尼)POETYK PsA-2 III期试验最新数据 证实其在治疗成人银屑病关节炎中优于安慰剂
治疗第 16 周时,颂狄多治疗组患者的 ACR和 PASI应答率显著高于安慰剂组,且患者报告生活质量有更明显改善。与安慰剂和阿普米司特相比,颂狄多耐受性良好,安全性特征与既往...
2025-03-11 09:38
 资讯
资讯 华东医药全球首个卵巢癌ADC爱拉赫®补充申请获受理
申报适应症为用于既往接受过1-3线系统性治疗的叶酸受体α(FRα)阳性的铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌成年患者。
2025-03-10 19:36
 资讯
资讯 用于治疗复发或难治性多发性骨髓瘤,辉瑞靶向免疫疗法易瑞欧(埃纳妥单抗)在华获批
今日(3月10日),辉瑞公司宣布,靶向免疫疗法易瑞欧®(埃纳妥单抗)获国家药品监督管理局附条件批准,适用于既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂...
2025-03-10 12:07