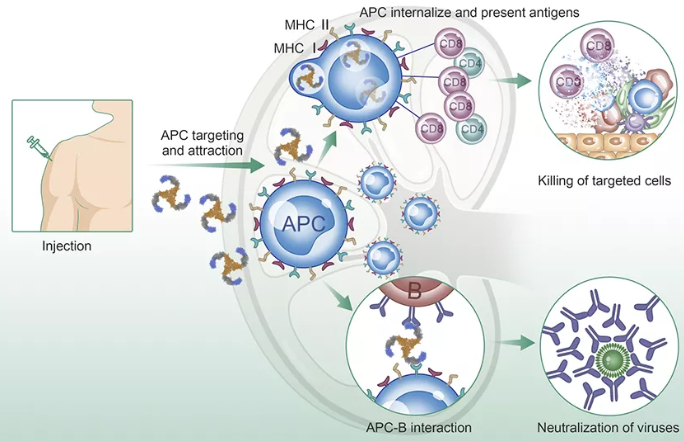
一个国际CRISPR-Cas研究人员小组发现了自然存在的、具有基因组编辑潜力的三个新系统。发现以及确定这些系统的特征有望进一步扩大基因组编辑工具箱,为生物医学研究开辟新的途径。这项研究发表在10月22日的《分子细胞》(Molecular Cell)杂志上。
美国国立卫生研究院下属国立医学图书馆(NLM)国家生物技术信息中心(NCBI)的资深研究员Eugene Koonin 博士,及麻省理工学院-哈佛大学Broad研究所的张锋(Feng Zhang)博士共同领导了这一研究。
Koonin说:“这项研究显示出了发现具有不同性能新型CRISPR-Cas系统的一条途径。进化是如何获得一系列广泛的生物活性的,是这一故事最值得关注的一个方面,我们可以利用这一壮举来获得新的基因组操控工具。”
来自CRISPR系统的酶给基因组学领域带来了革命性的发展,使得研究人员能够靶向基因组特异区域,在精确的位点编辑DNA。“CRISPR”指的是规律成簇的间隔短回文重复序列,它是细菌利用来防御入侵病毒的一种系统的关键组件。CRISPR系统生成的一种酶:Cas9可以一种高度序列特异性方式结合DNA并切割它,使得能够精确操控DNA区域。Cas9一类的酶为研究人员提供了比以往开发的方法要更快速、更廉价和更精确的一种基因编辑工具。
三个新发现的系统与Cas9和近期新确定特征的一种CRISPR酶Cpf1共享了一些特征,但它们也具有自身一些独特的特性,有可能可以被利用来实现新的基因组编辑应用。这项研究凸显了CRISPR系统的多样性,研究人员可以利用这种多样性来开发出更高效、有效及精确的DNA编辑方法。
研究人员采用了一种新生物信息学方法来发现这些暂时被命名为C2c1、C2c2和C2c3的新蛋白,他们开发出一系列的计算方法来搜索NIH基因组数据库,鉴别新的CRISPR-Cas系统。
论文的共同作者、Rutgers与Skolkovo生物技术研究所的Konstantin Severinov说:“现在有许多方法可以修改搜索算法,因此可以预计很快将揭示出一些更令人兴奋及不同的CRISPR-Cas机制。这些机制毫无疑问 将吸引基础和应用科学家们的注意。”
初期的实验工作探究了这些蛋白质的功能,揭示出它们与已充分确定特征、广泛用于基因组编辑的Cas9蛋白大不相同。
通过分析C2c1、C2c2和C2c3,研究小组推断出了这些适应性防御系统复杂的进化途经。
张锋说:“这项工作的合作性质凸显了将具有不同优势的顶尖科学家汇集到一起,在计算、分子生物学和 进化生物学的界面上进行创新的能力。”
Koonin和张锋的研究小组还在近期开展项目合作,鉴别出了一个新型CRISPR核酸酶Cpf1的特征,Cpf1有望变成一个重要的基因编辑工具。
来源:生物通 作者:何嫱
为你推荐
 资讯
资讯 外用制剂领域再突破 MC2-01乳膏治疗中国斑块状银屑病的Ⅲ期临床试验获批
杭州中美华东制药有限公司开发的MC2-01乳膏,用于治疗中国斑块状银屑病的Ⅲ期临床试验申请已正式获得国家药品监督管理局批准
2025-07-28 18:18
 资讯
资讯 欧盟批准含Blenrep(注射用玛贝兰妥单抗)的联合治疗方案用于治疗复发或难治多发性骨髓瘤
葛兰素史克(LSE NYSE:GSK)7月24日宣布,Blenrep已获得欧盟(EU)批准,用于以下适应症:联合硼替佐米和地塞米松(BVd),用于既往接受过至少一线治疗的复发或难治多发性骨髓...
2025-07-28 16:08
 资讯
资讯 欧狄沃联合逸沃获批成为中国首个非小细胞肺癌一线双免疫疗法
今日(7月28日),百时美施贵宝宣布,欧狄沃®(纳武利尤单抗注射液)联合逸沃®(伊匹木单抗注射液)方案获得中国国家药品监督管理局(NMPA)批准。
2025-07-28 15:58
 资讯
资讯 橙帆医药完成超6000万美元Pre-A+轮融资,加速全球首创新药管线临床开发
2025年7月28日,专注多抗与ADC药物研发的创新企业橙帆医药宣布完成超6000万美元Pre-A+轮融资。本轮融资由顺为资本领投,北极光创投、汉康资
2025-07-28 09:21
 资讯
资讯 Lenacapavir“零时差”落地乐城,我国HIV防控迈入长效预防新时代
2025年7月25日,全球同类首创、一年仅需给药两次的HIV暴露前预防药物Lenacapavir(来那帕韦)正式落地海南博鳌乐城国际医疗旅游先行区
2025-07-27 10:35
 资讯
资讯 国家卫健委:医养结合示范项目工作方案(2025年版)
全国医养结合示范机构。具备医疗卫生机构资质,依法进行养老机构备案的医疗卫生机构或养老机构。示范机构每2年评估一次,每次命名100个左右(含中医药特色的示范机构),2030年...
2025-07-26 17:05
 资讯
资讯 CDE :化学药品口溶膜剂药学研究技术指导原则(试行)
膜剂是指原料药物与适宜成膜材料等经加工制成的膜状制剂,根据给药部位不同,可分为口用膜、眼用膜、阴道膜等。口用膜可分为口溶膜、口颊膜、舌下膜和口腔贴膜。口溶膜是指在口...
2025-07-26 10:52
 资讯
资讯 CDE:12项生物类似药药学相似性研究的问题与解答
生物类似药进行临床试验申请时,对于生产工艺和规模的要求是什么?候选药的剂型、规格、 制剂处方是否必须与参照药一致?对参照药的来源如何要求?多规格制剂中是否可以选择一...
2025-07-26 10:40
 资讯
资讯 皮尔法伯集团毕太维®联合疗法在华获批,精准靶向BRAFV600E突变型转移性结直肠癌
用于既往接受过系统治疗的BRAFV600E突变型转移性结直肠癌(mCRC)成人患者。
2025-07-25 18:24
 资讯
资讯 《特殊医学用途流质配方食品注册指南》和《特殊医学用途增稠组件配方食品注册指南》
流质配方为非全营养配方食品,一般在短时间内使用,满足需要流质饮食和限制脂肪摄入人群的基本营养需求。
2025-07-25 17:15
 资讯
资讯 扬子江药业在固阳成功举办第二届717龙凤堂有机黄芪节
“健康中国”战略指引下,扬子江药业集团(以下简称扬子江)旗下中药品牌龙凤堂始终致力于全链条把控产品质量,从源头助力中药材产业发展水平提升。
2025-07-25 10:42
 资讯
资讯 国家市场监督管理总局禁止武汉用通收购山东华泰制药股权,要求解除
本案是2008年《中华人民共和国反垄断法》施行以来第四起禁止的经营者集中案件,是第一起对未达申报标准的经营者集中予以禁止的案件,也是首次要求相关方对已实施的集中采取措施...
2025-07-24 17:43
 资讯
资讯 1500万美元里程碑付款,一款国产双靶向CAR-T疗法出海
近日,科弈药业宣布,与美国生物医药企业ERIGEN LLC就其自研的全球首个并联增强型双靶向CAR-T细胞治疗产品KQ-2003(靶向BCMA CD19)的独家海外授权许可达成战略合作。
2025-07-24 14:28
 资讯
资讯 AQ健康数据警示:暑期割包皮咨询量翻5倍 非必要不手术
随着暑期到来,全国多家医院小儿泌尿外科门诊迎来就诊高峰。部分医院暑期预期手术量甚至高达4000多台,不少家长选择利用假期为孩子安排包皮手术咨询和预约。
2025-07-24 12:00
 资讯
资讯 CDE :存在未满足临床需求的严重细菌感染性疾病抗菌药物临床试验技术指导原则
严重细菌感染性疾病的抗菌药物治疗领域,尤其是那些对多种抗菌药物耐药、过敏或不耐受而导致治疗选择有限或缺乏的存在未满足临床需求的患者,迫切需要新的、有效的、安全的抗菌...
2025-07-23 18:40