8月27日上午,广东省药品监管局联合广东省卫生健康委召开专题新闻发布会。会上通报了“港澳药械通”试点工作情况及各项实施工作的安排。同日,广东省市场监管局、广东省药监局、广东省发展改革委、广东省财政厅、广东省商务厅、广东省卫生健康委、广东省医疗保障局、海关总署广东分署 广东省港澳办、广东省中医药局联合印发《广东省粤港澳大湾区内地临床急需进口港澳药品医疗器械管理暂行规定》的通知(以下简称 “《暂行规定》”)。
2020年9月29日,国家市场监督管理总局、国家药品监督管理局等八部委联合印发《粤港澳大湾区药品医疗器械监管创新发展工作方案》,明确授权“在粤港澳大湾区内地9市开业的指定医疗机构使用临床急需、已在港澳上市的药品,由国家药监局批准改为由国务院授权广东省人民政府批准”;“区域内开业的指定医疗机构使用临床急需、港澳公立医院已采购使用、具有临床应用先进性的医疗器械,由广东省政府批准。”
按照分布实施的原则,先期以香港大学深圳医院为试点,在取得阶段性进展后逐步扩展至其他符合要求的指定医疗机构。按照工作安排,“港澳药械通”政策在香港大学深圳医院试点期至2021年7月31日。
内地9市是指广州、深圳、珠海、佛山、惠州、东莞、中山、江门、肇庆九市。
已审批临床急需使用进口药品9个、医疗器械2个,共惠及150名患者
广东省药品监管局党组成员苏盛锋在会上表示,自今年1月在香港大学深圳医院开始“港澳药械通”政策试点以来,已审批临床急需使用进口药品9个、医疗器械2个,共惠及150名患者。
其中,不乏恩曲替尼、劳拉替尼等目前全球较新的抗癌药品,通过“港澳药械通”政策进到香港大学深圳医院临床使用,为难治性、特定基因突变型癌症类型患者提供了替代性治疗方式,为过去无法获得进一步治疗的部分患者带来了新的治疗希望。
试点拓展至5家指定医疗机构
广东省卫生健康委员会副主任周紫霄在当天举行的专题新闻发布会上表示,“港澳药械通”政策审核确定了5家首批内地指定医疗机构。即由香港大学深圳医院1家试点,拓展为5家。
广东省卫生健康委从医疗机构资质力量、合作建设医疗水平和所有制经营形式上等因素综合考虑,按照医疗机构申报、广东省卫生健康委审核和研究确定3个步骤组织实施遴选,审核确定了5家首批内地指定医疗机构,涉及广州2家,深圳、珠海、中山各1家。
具体为:香港大学深圳医院(三级医院,试点医院);广州现代医院(二级医院)、广州和睦家医院(二级医院)、珠海希玛林顺潮眼科医院(二级医院)和中山陈星海医院(三级医院)。
接下来,广东省卫生健康委将在指导好首批内地指定医疗机构落实政策规定基础上,结合临床急需的港澳上市药品医疗器械在内地的实际使用情况,适时开展研究补充下一批指定医疗机构。
临床急需药械实行目录管理
根据最新发布的《暂行规定》,临床急需进口港澳药品是指粤港澳大湾区内地医疗机构临床急需、已在港澳上市的,且不属于麻醉药品、精神药品、兴奋剂目录中的蛋白同化制剂和肽类激素等实施进口准许证管理的药品;临床急需进口港澳医疗器械是指港澳公立医院已采购使用、属于临床急需、具有临床应用先进性的医疗器械。同时,对进口的急需药械实行目录管理,并进行动态调整、及时公布。
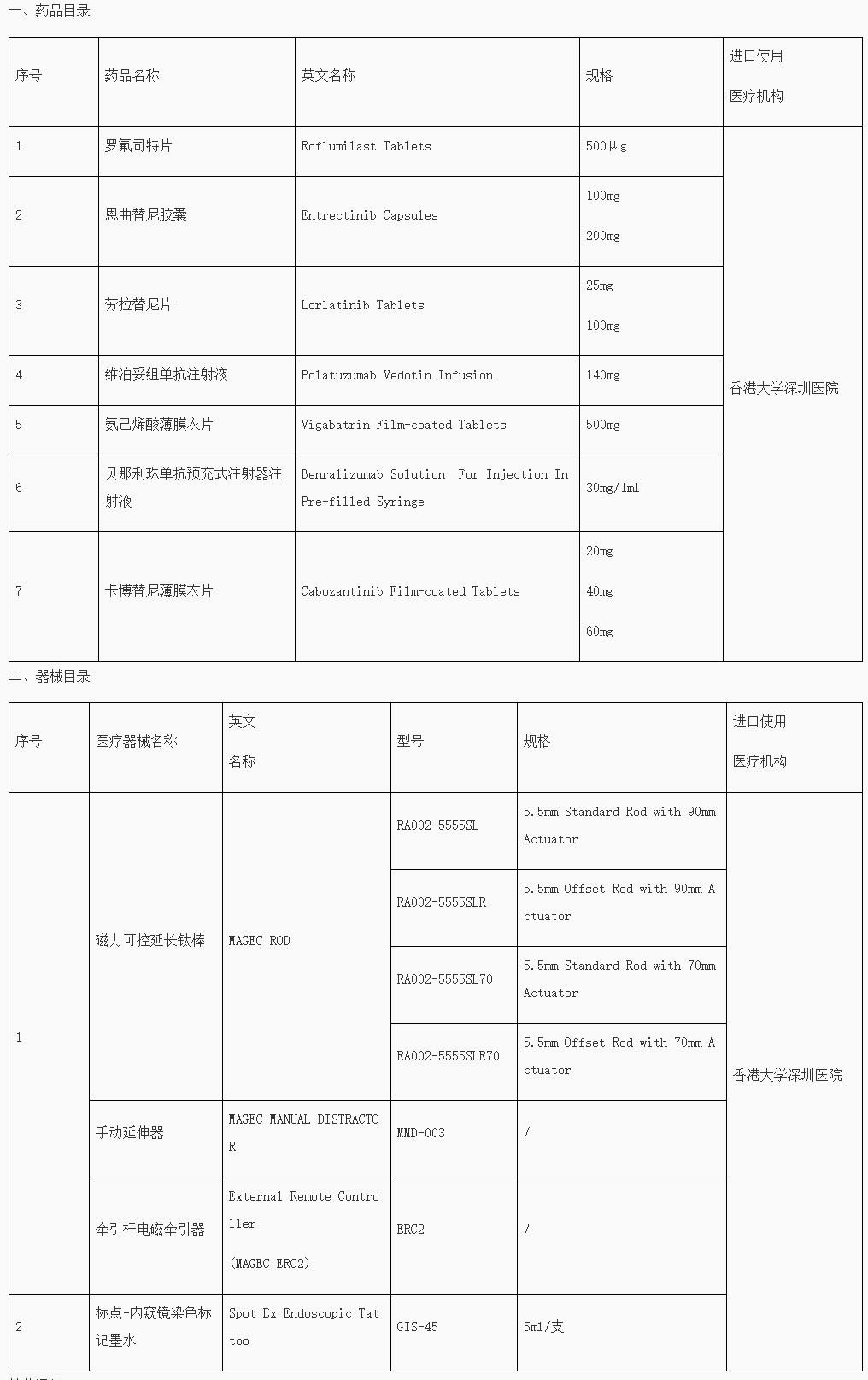
根据广东省药监局,广东省卫生健康委8月25日联合发布的《关于发布第一批粤港澳大湾区内地临床急需进口港澳药品医疗器械目录的通告》,第一批目录共涉及7个药品和4款医疗器械。
批准文件有效期1年
指定医疗机构向广东省药品监督管理局提出进口使用急需药械申请的,广东省药品监督管理局联合广东省卫生健康委员会办理(属于大型医用设备的医疗器械还应当提供广东省商务厅出具的进口审核意见)。同意批准的,应当发给批准文件,批准文件有效期1年。
粤港澳大湾区内地口岸所在地承担药品监督管理职责的部门(以下简称口岸药品监管部门)和海关,按照粤港澳大湾区内地急需药械进口通关管理有关规定,办理急需药械的通关手续。进口药品的,经营企业凭广东省药品监督管理局的批准文件向口岸药品监管部门申请《进口药品通关单》,海关按规定办理通关手续;进口医疗器械的,经营企业凭广东省药品监督管理局的批准文件申请进口报关,海关按规定核验放行。
临床急需进口药品无需进口检验,列入《特殊物品海关商品编号和检验检疫名称对应表》的物品,应当按照海关相关规定办理行政许可。
销售价格实行零差率
指定医疗机构使用的急需药械销售价格实行零差率,新增医疗服务价格项目按现行规定执行,新增项目价格由医疗机构自主确定试行2年。
指定医疗机构使用急需药械前应当经医疗机构伦理委员会审查同意,向患者或者家属告知急需药械按临床急需进口批准和内地可替代的产品或者治疗方案等情况,并按照国家相关规定与患者或者家属签署书面知情同意书等文件。
指定医疗机构使用急需药械所收集的真实世界数据,符合我国药品医疗器械注册相关要求的,按相关规定执行。
配送企业基本要求
根据《暂行规定》从事急需药械采购、进口、储存和配送的经营企业应当为在内地设立的药品或者医疗器械经营企业;符合《药品经营质量管理规范》或者《医疗器械经营质量管理规范》要求,具有与所采购、储存和配送药品或者医疗器械相应的经营范围;具备现代物流条件,仓库配备适合急需药械储存的专用库房,并符合《药品经营质量管理规范》或者《医疗器械经营质量管理规范》要求;具有符合药品医疗器械经营质量管理要求的计算机信息管理系统;具有与指定医疗机构实施实时电子数据交换和实现产品经营全过程可追溯管理的计算机信息平台和技术手段;具有接受药品监督管理部门电子监管的数据接口;具有急需药械进口、赋码、储存和配送等环节质量控制的数据管理系统,可实现经营全过程“一物一码”可追溯、可核查、可校验、且数据不可篡改;配送网络能够覆盖大湾区内地的指定医疗机构;具有进出口经营资质,经海关备案为进出口货物收发货人和对外贸易经营者;在与指定医疗机构签订采购协议之日起前3年内未被列为失信被执行人,未被列入重大税收违法案件当事人名单,未被列入政府采购严重违法失信行为记录名单,没有药品或者医疗器械经营和海关进出口违法违规不良记录。
经营企业应当按照《药品经营质量管理规范》或者《医疗器械经营质量管理规范》的要求采购、进口、储存和配送药品和医疗器械,依据法律法规和《暂行规定》对港澳药品医疗器械经营质量安全承担责任。
广东省粤港澳大湾区内地临床急需进口港澳药品医疗器械管理暂行规定
第一条 为加强粤港澳大湾区内地临床急需进口港澳药品医疗器械的管理,满足粤港澳大湾区居民用药用械需求,保障公众用药用械安全、有效、可及和合法权益,依据《中华人民共和国药品管理法》、《医疗器械监督管理条例》、《粤港澳大湾区药品医疗器械监管创新发展工作方案》等法律法规和有关文件要求,制定本规定。
第二条 临床急需进口港澳药品是指粤港澳大湾区内地医疗机构临床急需、已在港澳上市的,且不属于麻醉药品、精神药品、兴奋剂目录中的蛋白同化制剂和肽类激素等实施进口准许证管理的药品;临床急需进口港澳医疗器械是指港澳公立医院已采购使用、属于临床急需、具有临床应用先进性的医疗器械(以下简称急需药械)。
对进口的急需药械实行目录管理,并进行动态调整、及时公布。
急需药械应当在申请进口使用的医疗机构用于特定医疗目的。
第三条 广东省药品监督管理局会同相关部门,根据职责和实际需要,制定急需药械全过程监管制度和管理措施,负责对急需药械的进口使用进行批准。广东省卫生健康委员会负责审核确定使用急需药械的医疗机构(以下简称指定医疗机构)并对临床需求进行评估审核。广东省商务、医疗保障、市场监督管理和广东省内各海关单位等有关部门依据法律法规、有关政策和本规定,分别履行相关监督管理职责。
地级以上市人民政府有关部门在各自职责范围内负责与急需药械有关的监督管理工作。
第四条 申请纳入指定医疗机构名单的,应当经广东省卫生健康委员会审核确定,并具备以下条件:
(一)港澳医疗卫生服务提供主体在粤港澳大湾区内地以独资、合资或者合作等方式设置的医疗机构;
(二)依法取得医疗机构执业许可,具备与所申请急需药械相适应的专业科室或者医疗团队;
(三)在验货、储存、养护方面具有符合急需药械特性和说明书要求的保障条件和管理制度;
(四)设置药品医疗器械不良反应(不良事件)监测机构,配备专职人员并已接受专业培训,能够正确履行不良反应(不良事件)监测职责;
(五)具有使用急需药械可能发生严重不良反应(不良事件)的应急预案和处置能力。
凡不属于本条款第(一)项规定的医疗机构,拟申请纳入指定医疗机构,由广东省卫生健康委员会参照上述条件研究后,报请国家卫生健康委员会审批确定。
第五条 指定医疗机构申请进口使用急需药械的,应当按照粤港澳大湾区内地指定医疗机构进口使用港澳药品医疗器械申报指南(附件1)的要求,向广东省药品监督管理局提出申请,并承诺申请资料真实、可靠,保证急需药械仅在本医疗机构用于特定医疗目的,对急需药械的使用风险承担全部责任。
第六条 广东省药品监督管理局会同广东省卫生健康委员会建立评审专家库,对指定医疗机构申请进口使用的药品是否属于临床急需或者医疗器械是否属于临床急需且无其他治疗手段、内地已上市产品能否达到同等治疗效果等先进性要求进行评估审核。
第七条 指定医疗机构向广东省药品监督管理局提出进口使用急需药械申请的,广东省药品监督管理局联合广东省卫生健康委员会办理(属于大型医用设备的医疗器械还应当提供广东省商务厅出具的进口审核意见)。同意批准的,应当发给批准文件,批准文件有效期1年;不同意批准的,应当发给不予批准通知书,并说明理由。对非首次进口使用的急需药械的申请可以简化办理程序。
第八条 指定医疗机构应当通过药品或者医疗器械经营企业(以下简称经营企业)采购、进口和配送急需药械。
药品或者医疗器械经营企业应当持有《药品经营许可证》或者《医疗器械经营许可证》,并符合粤港澳大湾区内地急需药械采购、进口和配送企业基本要求(附件2)。
第九条 经营企业应当在经营许可范围内开展业务,按照《药品经营质量管理规范》、《医疗器械经营质量管理规范》的要求采购、储存、配送急需药械,并对急需药械经营质量安全承担责任。
经营企业应当从境外上市许可持有人或者其授权港澳经营机构(以下简称“持证企业”)采购急需药械,保证产品与港澳上市使用的药品、医疗器械一致。
急需进口药品相关证明文件、交易票据、采购记录和验收记录保存至药品有效期届满后3年。
急需进口医疗器械相关证明文件、交易票据、采购记录和验收记录应当保存至医疗器械有效期届满后2年;无有效期的,不得少于5年;植入类医疗器械进货查验记录和销售记录应当永久保存。
第十条 粤港澳大湾区内地口岸所在地承担药品监督管理职责的部门(以下简称口岸药品监管部门)和海关,按照粤港澳大湾区内地急需药械进口通关管理有关规定,办理急需药械的通关手续。进口药品的,经营企业凭广东省药品监督管理局的批准文件向口岸药品监管部门申请《进口药品通关单》,海关按规定办理通关手续;进口医疗器械的,经营企业凭广东省药品监督管理局的批准文件申请进口报关,海关按规定核验放行。禁止进口过期、失效、淘汰等已使用过的医疗器械。
临床急需进口药品无需进口检验,列入《特殊物品海关商品编号和检验检疫名称对应表》的物品,应当按照海关相关规定办理行政许可。
第十一条 指定医疗机构应当与经营企业签订质量协议,经营企业应当与持证企业签订质量协议,明确各方质量责任。
第十二条 指定医疗机构应当严格执行国家有关规定,建立并运行急需药械质量管理体系,确保急需药械来源合法、储存规范、流向清晰。
急需进口药品相关证明文件、交易票据、采购记录和验收记录保存至药品有效期届满后3年。
急需进口医疗器械相关证明文件、交易票据、采购记录和验收记录应当保存至医疗器械使用期限届满后2年或者使用终止后2年;大型医疗器械进货查验记录应当保存至医疗器械规定使用期限届满后5年或者使用终止后5年;植入性医疗器械进货查验记录应当永久保存。
第十三条 指定医疗机构应当采取有效措施,确保急需药械仅用于本医疗机构特定医疗目的;应当根据产品说明书制定临床技术规范,合理使用急需药械;急需药械使用相关的临床诊疗病历及相关数据信息,应当长期保存。
指定医疗机构使用急需药械前应当经医疗机构伦理委员会审查同意,向患者或者家属告知急需药械按临床急需进口批准和内地可替代的产品或者治疗方案等情况,并按照国家相关规定与患者或者家属签署书面知情同意书等文件。
第十四条 指定医疗机构应当制定完善的安全防范措施和风险监控处置预案。发现药品或者医疗器械严重不良反应(不良事件)或者出现重大医疗事故时,指定医疗机构应当按规定启动应急预案,及时进行风险评估,采取合理的安全防范措施控制风险;不能保证临床使用安全的,应当立即停止使用,并向广东省卫生健康委员会和广东省药品监督管理局报告。
第十五条 指定医疗机构和经营企业应当建立急需药械不良反应(不良事件)监测报告管理制度,按照粤港澳大湾区内地急需药械不良反应(不良事件)监测报告的相关规定,向所在地地级以上市药品监督管理部门药品不良反应监测机构报告急需药械不良反应(不良事件),同时通报相应的持证企业。
指定医疗机构和经营企业应当按规定建立并保存急需药械不良反应(不良事件)报告监测档案。
第十六条 指定医疗机构、经营企业、持证企业应当关注急需药械在境外使用的情况,建立信息共享机制,确保信息及时通报。
发现或者获知境外因产品安全有效性发生变化修订急需药械说明书、发布安全风险预警、发生重大安全事件或者停用等影响急需药械使用安全情况的,指定医疗机构应当采取调整用药用械方案、暂停使用、停止采购、使用替代治疗方案等处理措施,并将处置情况报告所在地地级以上市卫生健康主管部门、药品监督管理部门和药品不良反应监测机构。
第十七条 急需药械在境外主动召回或者被要求召回的,经营企业和指定医疗机构应当根据召回原因及处置措施,按照召回行动方案主动配合境外上市许可持有人履行召回义务。召回方案涉及本医疗机构急需药械需要停用的,应当立即停止使用急需药械;经营企业应当立即停止配送并收回已经配送的急需药械。
对有证据证明急需药械可能具有危及人体健康和生命安全的风险应当召回急需药械而未召回的,药品监督管理部门可以责令指定医疗机构和经营企业召回急需药械。
指定医疗机构和经营企业应当将急需药械召回和处理的情况,及时报告所在地地级以上市卫生健康主管部门和药品监督管理部门。
第十八条 指定医疗机构使用急需药械所收集的真实世界数据,符合我国药品医疗器械注册相关要求的,按相关规定执行。
第十九条 广东省药品监督管理局应当参照国家药品监督管理局制定的药品追溯标准和规范,建立粤港澳大湾区急需药械监管系统,实现急需药械申请、采购、进口、配送、使用和不良反应(不良事件)监测等全过程监管。
指定医疗机构应当建立急需药械验货、储存、养护和使用等环节质量控制的数据管理系统;经营企业应当建立急需药械进口、赋码、储存和配送等环节质量控制的数据管理系统,实现与粤港澳大湾区急需药械监管系统实时对接,落实产品全程可追溯主体责任。
第二十条 地级以上市卫生健康主管部门应当加强对指定医疗机构的监督检查,发现指定医疗机构不再具备本规定第四条规定的使用急需药械的能力和条件的,应当上报广东省卫生健康委员会。广东省卫生健康委员会应当责令指定医疗机构限期整改,直至取消其指定医疗机构资格。
第二十一条 地级以上市药品监督管理部门应当加强对指定医疗机构的监督检查。原则上,现场检查每年不少于2次,重点核实急需药械采购渠道、索票索证、储存运输、使用记录的情况。必要时,可以对经营企业、持证企业进行延伸检查,并将检查情况上报广东省药品监督管理局。
第二十二条 指定医疗机构应当及时分析临床数据,研判控制风险,开展急需药械使用安全性和有效性评价,每年将急需药械临床使用评价情况报告所在地地级以上市卫生健康主管部门和药品监督管理部门。
广东省药品监督管理局、广东省卫生健康委员会应当对临床急需药械使用中的安全性风险进行研判并采取必要控制措施,组织相关专家对发生严重不良反应(不良事件)且可能存在重大安全风险的急需药械进行风险评估,结合急需药械港澳地区已批准上市和使用的情况,及时调整并公布急需药械品种目录。
第二十三条 急需药械自取得中国内地注册批准上市后,不再作为急需药械批准进口。
第二十四条 鼓励指定医疗机构引入保险机制,购买医疗商业保险,为急需药械使用安全承保。使用急需药械造成患者人体伤害的,指定医疗机构按照国家有关规定承担赔偿责任。
第二十五条 指定医疗机构使用的急需药械销售价格实行零差率,新增医疗服务价格项目按现行规定执行,新增项目价格由医疗机构自主确定试行2年。
支持临床急需进口港澳医疗器械的推广和使用,医用耗材企业就具体新品种及时向国家医疗保障局申请备案和编码,广东省医疗保障局按规定将符合条件的医用耗材新品种纳入医保支付范围,完善医用耗材医保支付标准与集中采购价格协同机制。
第二十六条 经营企业不再符合本规定第八条规定的基本要求的,广东省药品监督管理局应当责令指定医疗机构解除与经营企业的采购协议关系。指定医疗机构、经营企业违反本规定从事急需药械进口、使用等活动构成违法的,药品监督管理、卫生健康、商务、市场监督管理、海关、医疗保障等有关部门应当依据相关法律法规处理;造成急需药械无法追溯等严重后果的,广东省药品监督管理局应当撤销急需药械批准文件,广东省卫生健康委员会应当取消指定医疗机构资格。
第二十七条 广东省药品监督管理局、广东省卫生健康委员会、广东省内各海关单位等部门应当建立信息通报机制。
广东省卫生健康委员会应当及时将取消指定医疗机构资格的决定通报广东省药品监督管理局、广东省内各海关单位等部门。广东省药品监督管理局根据上述通报撤销相关急需药械批准文件。广东省药品监督管理局应当将急需药械进口批准和撤销的结果,通报广东省卫生健康委员会、广东省内各海关单位等部门。
地级以上市药品监督管理部门、卫生健康主管部门应当建立完善应急预案,开展医疗救治、风险控制、新闻监测等工作,妥善处置急需药械安全事件。
第二十八条 粤港澳大湾区内地是指广州、深圳、珠海、佛山、惠州、东莞、中山、江门、肇庆九市。
港澳地区是指香港和澳门。
第二十九条 本规定自发布之日起实施,有效期三年。
附件:
1.粤港澳大湾区内地指定医疗机构进口使用港澳药品医疗器械申报指南
2.粤港澳大湾区内地急需药械采购、进口和配送企业基本要求
附件1 粤港澳大湾区内地指定医疗机构进口使用港澳药品医疗器械申报指南
一、设定依据
《中华人民共和国药品管理法》、《中华人民共和国基本医疗卫生与健康促进法》、《医疗机构管理条例》、《医疗器械监督管理条例》、《药品进口管理办法》以及《粤港澳大湾区药品医疗器械监管创新发展工作方案》(国市监药〔2020〕159号)等法律法规和规章文件。
二、主要原则
以促进人民健康为中心,便捷粤港澳大湾区内地医疗机构和患者使用港澳药品和医疗器械,以临床急需和临床价值为标准,科学合理地评审指定医疗机构进口使用申请的合法性、必要性和合理性,切实维护人民群众用药用械安全。
三、评审产品范围
粤港澳大湾区内地医疗机构临床急需的、已在港澳上市的药品。港澳公立医院已采购使用、属于临床急需、具有临床应用先进性的医疗器械。
四、申请主体
粤港澳大湾区内地经广东省卫生健康委员会审核确定的指定医疗机构。
五、评审资料
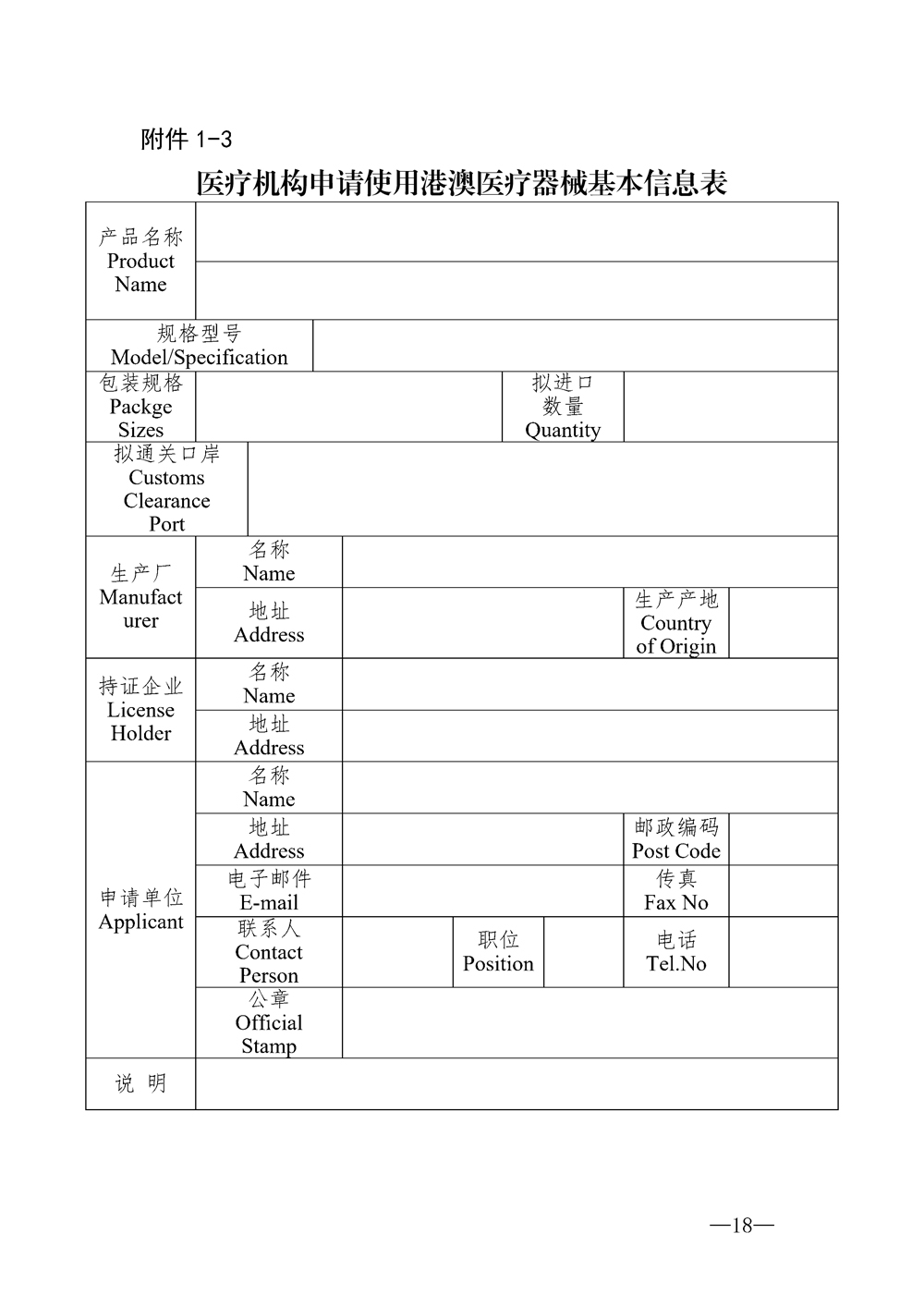
(一)申请报表:《医疗机构申请使用港澳药品基本信息表》《医疗机构申请使用港澳药品基本情况表》《医疗机构申请使用港澳医疗器械基本信息表》《医疗机构申请使用港澳医疗器械基本情况表》(详见附件1-1、1-2、1-3、1-4)。
(二)申报单位资质证明资料:指定医疗机构的许可文件、法人证书、营业执照及医疗机构执业许可证,均为复印件盖章。
申请使用港澳医疗器械还需申报单位提供其委托的负责采购、进口和配送医疗器械的经营企业资质证明文件。
(三)港澳药品、医疗器械进口使用申请材料:
药品:
1.香港或者澳门地区允许上市的批准证明文件。包括香港或者澳门地区允许在公立医疗机构使用的证明文件。
2.药品的包装、标签、说明书样本及产品完整实样图片。
3.医疗机构使用药品的评估资料,包括药品的临床急需性和安全性的评估分析,含临床使用综述、不良反应概述、使用风险评估等内容。
4.医疗机构使用药品伦理审核资料,包括目标患者适应症与使用范围、药品使用须知、医疗机构伦理委员会审核情况、知情同意书样本等。
5.医疗机构使用药品的技术规范和配套管理制度,包括临床使用技术规范(指南)、必要的替代治疗方案、医院和科室的管理制度和管理流程、授权使用名单、安全防范措施和风险监控处置预案、随访计划等。
6.医疗机构法人代表承诺书,承诺申报材料真实可靠,进口的药品仅用于本医疗机构特定医疗目的(附件1-5)。
以上资料复印件或扫描件均需加盖医疗机构公章,多页资料需加盖骑缝章。外文资料需提供中文译本。
医疗器械:
1.港澳地区公立医疗机构已采购使用的证明文件,以及原产国、其他国家准许上市的证明文件。
2.在港澳地区使用的包装、标签和说明书样本,及产品完整实样图片。其他有关产品的信息:产品结构组成、工作原理、作用机理、主要功能、预期用途等。无源医疗器械还需描述主要原材料,有源医疗器械还需描述关键组件和软件的功能。
3.医疗机构使用医疗器械临床急需性和安全性的评估资料。临床急需性评估分析包括:是否属于临床急需且无其他治疗手段的说明、国内目前已上市产品能否达到同等治疗效果、预期提高的疗效、医疗机构的器械使用能力等。安全性的评估分析包括:临床使用综述、不良事件概述、使用风险评估等内容。
4.医疗机构临床应用先进性的说明,包括:国内同类医疗器械获批注册上市情况,使用器械在技术水平或临床应用效果方面是否具有先进性,如基本原理、结构组成、制造材料、生产工艺、性能指标、临床应用效果等方面是否优于国内已批准上市医疗器械、处于国际领先水平。
5.医疗机构使用临床急需医疗器械的伦理审核,包括目标患者适应症与使用范围、医疗器械使用须知、医疗机构伦理委员会审核情况,知情同意书样本等。
6.医疗机构使用医疗器械的用械计划、技术规范和配套管理制度。包括:申请进口医疗器械需求数量的说明、使用计划;临床使用技术规范(指南)、必要的替代治疗方案,医院和科室的管理制度和管理流程、授权使用治疗组/专家名单、安全防范措施和风险监控处置预案(包括病人用械后严重不良事件的紧急救治预案)、随访计划等。
7.医疗机构法人代表承诺书,承诺申报材料真实可靠,进口的医疗器械仅用于本医疗机构特定医疗目的(附件1-5)。
以上资料复印件或扫描件均需加盖医疗机构公章,多页资料需加盖骑缝章。外文资料需提供中文译本。
六、评审流程
(一)指定医疗机构向广东省药品监督管理局提交进口使用港澳药品、医疗器械的申请。申请材料经形式审查,符合要求的,予以受理。
(二)根据《广东省粤港澳大湾区内地临床急需进口港澳药品医疗器械管理暂行规定》第六条规定,广东省药品监督管理局会同广东省卫生健康委员会对临床急需药械进行评审,原则上通过专家评审的形式开展。专家评审实行组长负责制。
(三)自受理之日起,由广东省药品监督管理局在五个工作日内组织专家开展评审。广东省卫生健康委员会应当自收到专家评审意见之日起十五个工作日内出具是否临床急需审核意见。广东省药品监督管理局应当自收到广东省卫生健康委员会审核意见之日起十五个工作日内作出是否准予进口的决定。同意进口使用的,发给批准文件,批准文件有效期1年;不同意进口使用的,发给不予批准通知书,并说明理由。专家评审时间不计算在审批期限内。
七、解释部门
由广东省药品监督管理局会同广东省卫生健康委员会解释。
附件:
1-1.医疗机构申请使用港澳药品基本信息表
1-2.医疗机构申请使用港澳药品基本情况表
1-3.医疗机构申请使用港澳医疗器械基本信息表
1-4.医疗机构申请使用港澳医疗器械基本情况表
1-5.承诺书(模板)
附件2 粤港澳大湾区内地急需药械采购、进口和配送企业基本要求
从事急需药械采购、进口、储存和配送的经营企业应当具有健全的质量管理体系、具备现代物流条件、配送覆盖面广、诚实守信,具体要求如下:
(一)在内地设立的药品或者医疗器械经营企业;
(二)符合《药品经营质量管理规范》或者《医疗器械经营质量管理规范》要求,具有与所采购、储存和配送药品或者医疗器械相应的经营范围;
(三)具备现代物流条件,仓库配备适合急需药械储存的专用库房,并符合《药品经营质量管理规范》或者《医疗器械经营质量管理规范》要求;
(四)具有符合药品医疗器械经营质量管理要求的计算机信息管理系统;具有与指定医疗机构实施实时电子数据交换和实现产品经营全过程可追溯管理的计算机信息平台和技术手段;具有接受药品监督管理部门电子监管的数据接口;具有急需药械进口、赋码、储存和配送等环节质量控制的数据管理系统,可实现经营全过程“一物一码”可追溯、可核查、可校验、且数据不可篡改;
(五)配送网络能够覆盖大湾区内地的指定医疗机构;
(六)具有进出口经营资质,经海关备案为进出口货物收发货人和对外贸易经营者;
(七)在与指定医疗机构签订采购协议之日起前3年内未被列为失信被执行人,未被列入重大税收违法案件当事人名单,未被列入政府采购严重违法失信行为记录名单,没有药品或者医疗器械经营和海关进出口违法违规不良记录。
经营企业应当按照《药品经营质量管理规范》或者《医疗器械经营质量管理规范》的要求采购、进口、储存和配送药品和医疗器械,依据法律法规和本规定对港澳药品医疗器械经营质量安全承担责任。
来源:医谷网
为你推荐
 资讯
资讯 Cytiva与中欧创新医药与健康研究中心签署全面合作协议
双方将携手在细胞治疗药物成果转化领域展开全面合作,推动大湾区生物医药产业的蓬勃发展,打造全球生物医药创新高地。
2025-04-25 19:49
 资讯
资讯 精鼎医药任命 Charlotte Moser为公司首席医疗官,负责领导全球医学战略
今日(4月25日),致力于为客户提供I至IV期全方位临床开发服务的跨国合同研究组织(CRO)精鼎医药宣布,公司已任命 Charlotte Moser博士出任首席医疗官。
2025-04-25 15:06
 资讯
资讯 强生宣布锐珂(埃万妥单抗注射液)联合化疗方案在华获批,用于EGFR TKI经治后局部晚期或转移性非小细胞肺癌患者治疗
强生公司今日(4月25日)宣布,旗下创新治疗药物锐珂®(埃万妥单抗注射液)正式获得国家药品监督管理局批准,与卡铂和培美曲塞联合给药,适用于治疗携带表皮生长因子受体(EGFR...
2025-04-25 15:00
 资讯
资讯 《新英格兰医学杂志》发布: 研究证实速福达可将流感病毒家庭传播概率降低32%
罗氏全球今日(4月25日)宣布,速福达®(玛巴洛沙韦)III期临床试验CENTERSTONE研究详细结果在《新英格兰医学杂志》(NEJM)上发布。结果显示研究达到了主要终点:流感感染者单...
2025-04-25 13:34
 资讯
资讯 华东医药2025年一季度业绩出炉,创新产品持续发力
2025年第一季度内公司实现营业收入107 36亿元,同比增长3 12%;实现归属于上市公司股东的净利润9 15亿元,同比增长6 06%;实现扣非归母净利润8 97亿元,达到历史最好水平,同比增长7 04%。
2025-04-24 21:53
 资讯
资讯 医药如何数智化?医药工业数智化转型实施方案(2025—2030年)发布
研发推广一批智能制药设备、检测设备,开发一批“小快轻准”医药工业软件或系统。支持创建医药工业数智技术应用验证与中试平台,集成推进共性技术攻关、软硬件适配验证测试、计...
2025-04-24 18:26
 资讯
资讯 全球顶尖专家共话尿路上皮癌诊疗领域的新突破——第三届泌尿肿瘤临床研究大会会后会成功举办
2025年4月24日,北京——,“第三届泌尿肿瘤临床研究大会会后会”在北京成功举办。本次会议以“全球专家共话尿路上皮癌”为主题,汇聚了来自中外的顶尖泌尿肿瘤专家,围绕尿路上...
2025-04-24 16:26
 资讯
资讯 全国预防接种日:“健康中国家,疫苗护万家”健康社区“免疫行动”促进计划启动
由新华网主办,中国医药卫生文化协会疫苗与健康分会、《中国社区医师》杂志联合支持的“健康中国家,疫苗护万家——健康社区‘免疫行动’促进计划”于4月23日在北京正式启动。
2025-04-24 14:07
 资讯
资讯 带状疱疹疫苗“遇冷”,百克生物2024年净利润腰斩
近日,国内疫苗龙头企业百克生物发布2024年年报,数据显示,其报告期内实现营收12 29亿元,同比下降32 64%;归属于上市公司股东的净利润2 32亿元,同比下降53 67%。对于营收...
2025-04-23 12:59