昨日(7月5日),山东省分析测试中心被FDA警告的消息,引起了行业热议。
这件事情简而言之,即某企业生产的肝素原料出口到美国,该企业将其中的一个检测项“多硫酸软骨素(OSCS)核磁共振(NMR)检测项目”外包给了山东省分析测试中心,但是该检测过程中犯了几个错误,第一,检测机构日常检测未运行系统适用性;第二,检测机构在几年前的一次检测运行了失败的运行系统适用性,但最终并未对失败原因进行调查,也并未对之前的检测结果的有效性进行确认;第三,原始数据被删,难以追溯,且拒绝FDA查看其它检测客户相关信息。
最终,该生产企业被FDA判处生产的是“假药”。
根据美国的的cGMP原则——CFR211.22:
(a)The quality control unit shall be responsible for approving or rejecting drug products manufactured, processed, packed, or held under contract by another company.
(b)Adequate laboratory facilities for the testing and approval (or rejection) of components, drug product containers, closures, packaging material, in-process materials, and drug products shall be available to the quality control unit.
也就是说,企业不一定需要每一个检测环节都要求自建检验部门,可以将一些检测外包给CRO/CMO。但有一点,企业需要对服务提供商进行必要的供应商审计,确保其遵循了FDA的相关规定。
事实上,这种现象在国内非常普遍(不得不提2015年7月22日,国家食药监总局发布《关于开展药物临床试验数据自查核查工作的公告》,严查药品注册,并掀起了药品注册申请自查和核查风暴,该核查风暴与此次FDA所查事件性质一样),当然,据有自媒体报道,从另外一方面说,是否是FDA有意为之也未可知——毕竟伴随着国际间交流和人员的流动(例如,EU-US已经开始共享现场检查资源,CFDA和FDA也曾双边探讨过类似话题),FDA对国内行业现状恐怕也是了了然的,新开检查项目,无疑是一记警钟,长远看,对国内企业理解和执行GMP未必是一件坏事。
附FDA给山东省分析测试中心的警告信全文:
美国FDA曾于2017年1月16-18日检查了位于山东省济南市历下区科院路19号的药品生产场所---山东省分析检测中心。
该警告信总结了原料药生产过程中严重违反CGMP的行为。
在检查过程中发现,你们的原料药生产、加工、包装或保存的方法、场所或控制均不不符合CGMP要求,根据FDCA的501(a)(2)(B)以及21 U.S.C. 351(a)(2)(B)的条例,被认为是掺假药品。
为此,我们又详细阅读了你们公司曾于2017年2月20日的回复。
检查期间,我们的工作人员发现了以下问题:
1. 未能确保测试程序是否健全,科学以及适当,也无法确保API符合既定的质量和/或纯度标准。
你们的办公场所是肝素和肝素相关药品样品分析的委托化验室,提供多硫酸软骨素(OSCS)项目核磁共振(NMR)检测服务,但是你们在检测样品的OSCS项目时,却未认真检测和测试
未运行系统适用性。
此外,你们曾于2014年12月26日运行了运行了系统适用性,但系统适用性失败,在失败后,你们并未调查该系统失败的原因,也没有确认在这之前的其它OSCS检测结果是否准确可靠。
在你们的回复中,你们说化验室很少运行系统适用性,因为你们看到“肝素标准品和OSCS至少能在 (b)(4)中检出”,你们承诺会在将来进行样品分析之前检测系统实用性。
但是你们的回复是不充分的,因为你们并没有调查和确认上述所提到的其它OSCS检测结果的有效性。
系统适用性检测决定了精密度是否满足要求,在开始样品分析之前确保NMR仪器适合既定检测,至关重要的是,证明系统适合于检出肝素中的OSCS污染,避免仪器不正常工作时使得样品错误地通过检测是非常重要的。
关于肝素的更多参考资料,参见行业指南:药用和医疗器械用肝素:监测肝素粗品的质量。
2. 未能防止未经授权进入和修改数据,未能提供足够的控制以防止数据修改和删除。
你们质量控制部门没有基本的控制用以防止对你们电子存贮实验室数据的修改。在我们的检查期间,我们要求你们显示肝素和肝素相关药物样品分析的原始电子数据,但是你们的化验分析师未能恢复所要求展示的数据,还解释说他之所以删除旧数据,是为了储存更多新数据。
在你们的回复中,你们承诺说要修订化验室计算机许可水平的程序,然而病没有说明数据删除的原因。
在检查期间,你们提供了给了我们一份受委托进行检测的部分客户名单,也包括他们进行检测的样品信息和检测结果,但是,你们拒绝提供为其它客户所检测的样品数据,原因是未获得其许可。
例如,你们未能提供包含有为XX客户所检测的样品的信息,该公司为美国供应链生产肝素和肝素有关药品。
当一个实验室工作人员延误、否决、限制和拒绝检查时,在该场所生产、加工、包装和存贮的药品,根据FDCA的501(j)会被作为掺假药,详情请参见上述指南。
这封警告信里所说的这些问题还并不是全部,你们应尽快上述问题进行调查和解决,以防止其再次发生。
在公司未能解决完这些问题时,FDA可能会搁置所有将你公司列为药品生产的新申报和增补申报的批准。
如果对提出的这些问题置若罔闻,这会让FDA依据FDCA第801(a)(3)条和21 U.S.C. 381(a)(3)拒绝接受在上述地址生产的产品进入美国。
在收到该函后,请在15个工作日内回复,在回复中清详细说明你们做了哪些工作来纠正这些问题,若不能在15个工作日内解决以上偏差,说明延迟的原因以及完成计划。
附英文全文
来源:医谷网
为你推荐
 资讯
资讯 带状疱疹疫苗“遇冷”,百克生物2024年净利润腰斩
近日,国内疫苗龙头企业百克生物发布2024年年报,数据显示,其报告期内实现营收12 29亿元,同比下降32 64%;归属于上市公司股东的净利润2 32亿元,同比下降53 67%。对于营收...
2025-04-23 12:59
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34
 资讯
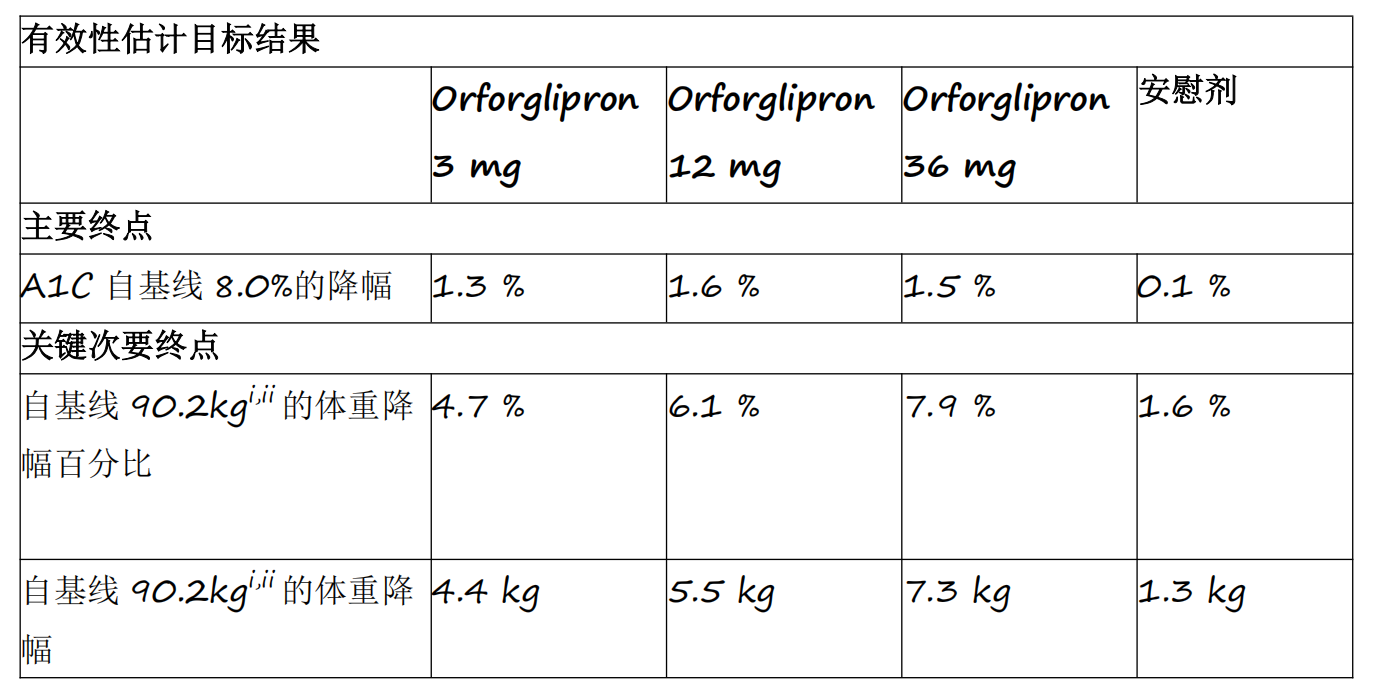
资讯 礼来首个小分子口服GLP-1RA药物orforglipron 3期临床研究成功
Orforglipron是首个成功完成3期临床研究的小分子GLP-1类药物,各剂量组平均A1C降幅为1 3%至1 6%
2025-04-18 14:12












