通过对一个疾病“定性”,科学家能够有针对性的开发治疗方法,或是在同类疾病上互相借鉴,得到一些治疗思路,否则疗法的开发就要走许多的弯路。而最新的一个研究提示我们,或许我们对一个大名鼎鼎的疾病——帕金森病的定性发生了错误!
大家可能知道,帕金森病一直被认为是一种神经退行性疾病。之所以这样定性,是因为表面上来看,它很符合神经退行性疾病的定义,是多巴胺神经元内一种名为α-突触核蛋白(α-Syn)的蛋白错误折叠、堆积,不能被降解,神经元死亡导致的疾病状态,人体会出现一些功能障碍,并且随着时间的推移而恶化。
但是在《自然》杂志上新发表的研究中,来自哥伦比亚大学医学中心和拉霍亚过敏与免疫研究所的研究人员却认为,帕金森病应该是一种自身免疫性疾病[1]!
为什么这么说呢?首先我们要了解什么是自身免疫性疾病。自身免疫性疾病是指机体对自身抗原发生免疫反应而导致自身组织损害所引起的疾病。这里有个重点奇点糕要划一下:抗原。
是的,要有抗原的存在,免疫系统才会发动攻击,而几十年来的研究认为,神经元表面是不存在抗原的,所以免疫系统当然也不会去主动“找茬”。
然而这一观点在2014年时受到了挑战,哥伦比亚大学医学中心的神经生物学教授David Sulzer(同时也是本次新研究的联合通讯作者)在《自然通讯》杂志上发表文章,他通过解剖捐赠给哥伦比亚脑库的健康供者死后的脑组织,发现他们脑中的多巴胺神经元上竟然有MHC-1蛋白[2]!
MHC-1是什么?它是主要组织相容性复合体(MHC)家族中的一员。MHC-1的作用就是当有病原体入侵细胞时,MHC-1可以与其蛋白中的肽链结合,在细胞表面显示抗原,让抗原暴露,T细胞就会“闻讯赶来”,扑杀病原体和被感染的细胞。
既然有MHC分子的存在,是不是意味着神经元其实是可能会被T细胞攻击的呢?为了解答这个问题,研究人员用小鼠和人的胚胎干细胞培养出了神经元,进行了体外实验。经过追踪,在帕金森病模型中,他们真的观察到了多巴胺神经元被T细胞攻击的现象!
当年的研究到这里就结束了,而对Sulzer教授来说,这仅仅是个开始。他们还需要更多的证据和临床试验才能给“帕金森病是自身免疫性疾病”这一观点“盖章”。
鉴于蛋白质自身的错误加工也会导致它们成为“抗原”,研究人员进一步怀疑,T细胞或许就是被错误折叠的α-Syn所“诱骗”,认为多巴胺神经元已经被“入侵者”感染,所以将它们一起扑杀了。
为了证实这个新想法,研究人员招募了67例帕金森病患者(48-83岁)和36例年龄相仿的健康人[1],收集他们的血液样本,将错误折叠的α-Syn和其他几种蛋白加入血液样本中,希望观察到哪些蛋白会产生免疫反应。
结果并不让他们感到意外,健康人对照组中免疫细胞的活跃度非常低,几乎没有发生免疫反应;而帕金森病组中有40%对α-Syn发生了强烈的免疫反应。显然,这意味着,α-Syn作为“抗原”曾暴露在帕金森病患者的免疫系统面前,所以当它再次现身时,免疫系统就会履行职责,毫不客气地将它清除。
40%这个比例研究人员认为也属于“正常值”,在经典的自身免疫性疾病——I型糖尿病、类风湿性关节炎和多发性硬化中,发生“攻击”的比例通常在20-50%之间[3,4]。经过进一步的实验,研究人员确定了α-Syn结构中,有两个区域可以与MHC分子结合,等待被T细胞扑杀。
α-Syn结构中39号区域和129号区域可以和MHC分子结合(点击可看大图)
不仅如此,研究人员还发现,MHC分子上一对儿重要的等位基因在帕金森病患者中的表达是健康人的2倍!它们在MHC与抗原结合上发挥着重要作用,而且也早已被证明与多发性硬化的发生有关[5]。
虽然早在1998年,科学家就观察到了帕金森病患者脑内α-Syn在多巴胺神经元中的异常堆积和多巴胺神经元的死亡[6],但是两者之间究竟有怎样的关联却一直没有好的解释。而这项新的研究告诉我们,或许正是因为错误折叠的α-Syn以“抗原”的身份引发了免疫系统的免疫反应,而多巴胺神经元作为它的“宿主”,被T细胞认作为已经“不能再抢救一下”的细胞,连同α-Syn一并清理掉了。
其实仔细想一下,如果按照这个研究的逻辑,多巴胺神经元被T细胞杀死,不能分泌多巴胺,而目前治疗帕金森病的一个方法就是补充外源多巴胺,这是不是与I型糖尿病患者胰岛素产生细胞被T细胞杀死,而需要终身补充胰岛素有着异曲同工之处?
被T细胞破坏的胰岛素产生细胞(左)和正常的胰岛素产生细胞(右)
对于新的研究成果,阿拉巴马大学的神经学家Andrew West表示:“和其他很好的研究一样,我们解决了一个问题,但同时又面临了更多的问题。如果在更大型的队列研究中复制了这个结果,那么我很想知道,免疫细胞被激活发动攻击究竟是在什么时候出现的?”[7]
当然,这也是Sulzer教授他们接下来想解决的问题之一。他还表示,这项研究为帕金森病的研究推开了一扇新的大门,提供了新的治疗思路——或许可以通过免疫疗法增加免疫系统对α-Syn的耐受性,减少对它和神经元的攻击,以此改善或预防帕金森病患者的疾病进展[8]。
参考资料
[1] Sulzer D, Alcalay R N, Garretti F, et al. T cells from patients with Parkinson’s disease recognize α-synuclein peptides[J]. Nature, 2017, 546(7660): 656-661.
[2] Cebrián C, Zucca F A, Mauri P, et al. MHC-I expression renders catecholaminergic neurons susceptible to T-cell-mediated degeneration[J]. Nature communications, 2014, 5: 3633.
[3] Petrich de Marquesini, L. G.et al. IFN-γ and IL-10 islet-antigen-specific T cell responses in autoantibody-negative first-degree relatives of patients with type 1 diabetes. Diabetologia 53, 1451–1460 (2010).
[4] Arif, S. et al. Peripheral and islet interleukin-17 pathway activation characterizes human autoimmune diabetes and promotes cytokine-mediated β-cell death. Diabetes 60, 2112–2119 (2011).
[5] Gregersen J W, Kranc K R, Ke X, et al. Functional epistasis on a common MHC haplotype associated with multiple sclerosis[J]. Nature, 2006, 443(7111): 574-577.
[6] Spillantini, M. G., Crowther, R. A., Jakes, R., Hasegawa, M. & Goedert, M. α-Synuclein in filamentous inclusions of Lewy bodies from Parkinson’s disease and dementia with lewy bodies. Proc. Natl Acad. Sci. USA 95, 6469–6473 (1998).
[7] https://www.sciencenews.org/article/protein-parkinsons-provokes-immune-system?mode=topic&context=87&tgt=nr
[8] https://www.sciencedaily.com/releases/2017/06/170621132904.htm
来源:奇点网(微信号 geekheal_com) 作者:应雨妍
为你推荐
 资讯
资讯 重庆常用药联盟接续集采中选结果
近日,重庆常用药联盟接续集采中选情况公布,该联盟由重庆牵头,联合湖北、广西、海南、贵州、云南、青海、宁夏、新疆及新疆生产建设兵团等十省(区、市)开展的药品集中带量采...
2025-04-21 18:48
 资讯
资讯 全周期智控慢病,诺和诺德与京东健康开启战略合作
2025年4月21日,全球领先的生物制药公司诺和诺德与京东健康在北京正式签署战略合作协议,标志着双方在糖尿病和体重管理领域的合作进入新阶段。依托诺和诺德百年深耕慢病领域的专...
2025-04-21 15:57
 资讯
资讯 康方生物1类新药依若奇单抗上市申请获批,用于中重度斑块状银屑病成人患者
该药是我国第一个且唯一获批上市的IL-12 IL-23“双靶向”单克隆抗体新药,是康方生物自身免疫性疾病领域首个获批上市的一类新药。
2025-04-21 13:39
 资讯
资讯 阿斯利康乳腺癌1类创新药卡匹色替片中国获批
该药适用于联合氟维司群用于转移性阶段至少接受过一种内分泌治疗后疾病进展,或在辅助治疗期间或完成辅助治疗后12个月内复发的激素受体(HR)阳性、人表皮生长因子受体2(HER2)...
2025-04-21 11:02
 资讯
资讯 辉瑞宣布终止一款口服GLP-1减肥药的临床开发
近日,辉瑞在其官网宣布,决定终止开发口服胰高血糖素样肽-1受体(GLP-1R)激动剂Danuglipron(PF-06882961),原因系在一项有关用药剂量的临床试验中,一名患者出现了可能由该...
2025-04-21 10:29
 资讯
资讯 福建省医保局印发单列门诊统筹支付医保药品目录(2024年版)
根据2024年6月发布的《福建省医保药品单列门诊统筹支付管理办法(试行)》,为了让参保患者无需住院、在门诊就医也能用上国家谈判药品、享受医保待遇,将适用于门诊治疗、使用周...
2025-04-20 13:34
 资讯
资讯 首批中国消费名品名单,医药健康企业有哪些?
近日,工业和信息化部办公厅发布首批中国消费名品名单,分为中国消费名品名单和中国消费名品成长企业名单。首批中国消费名品名单共包括93个企业品牌和43个区域品牌。中国消费名...
2025-04-20 11:17
 资讯
资讯 携手共绘“个性化近视手术”新蓝图:爱尔眼科与爱尔康启动100家医院全光塑技术战略合作
双方将以技术共享为核心,以人才培养为支撑,以科研协作为纽带,全力推进屈光手术标准化诊疗体系建设,加速前沿技术在临床领域的普及应用
文/ 屈慧莹 2025-04-19 23:35
 资讯
资讯 CDE:简化港澳已上市传统口服中成药内地上市注册审批申报资料及技术要求
允许香港、澳门特区本地登记的生产企业持有,并经香港、澳门特区药品监督管理部门批准上市且在香港、澳门特区使用15年以上,生产过程符合药品生产质量管理规范(GMP)要求的传统...
2025-04-18 18:54
 资讯
资讯 君德医药完成近亿元A轮融资,加速推进创新药械组合平台建设与产品上市
本轮融资主要用于首个减重口服器械的注册及生产销售,以及加速多个核心创新药械组合技术平台的产品管线研发进程。
2025-04-18 14:34
 资讯
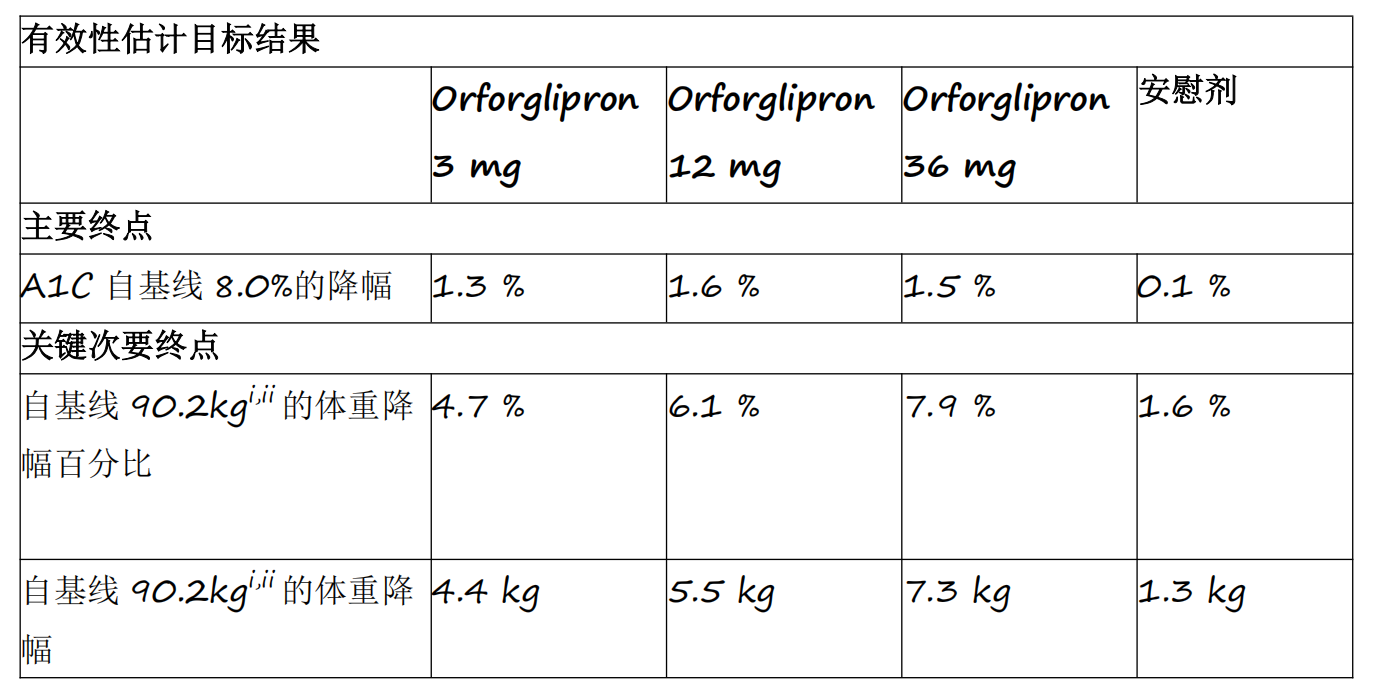
资讯 礼来首个小分子口服GLP-1RA药物orforglipron 3期临床研究成功
Orforglipron是首个成功完成3期临床研究的小分子GLP-1类药物,各剂量组平均A1C降幅为1 3%至1 6%
2025-04-18 14:12
 资讯
资讯 WSOPRAS 2025落幕:中国眼整形闪耀国际舞台,李冬梅教授代表爱尔眼科获2027年大会主办权
4月10日至12日,世界眼整形重建外科学会(WSOPRAS)2025年国际峰会在土耳其伊斯坦布尔盛大举行。
文/李林 2025-04-18 09:27











