3月28日,日本进行了世界首例异体iPS细胞移植手术,吸引了世界各地的目光,Nature news、新浪医药、新华网等媒体纷纷报道。可见,人们对iPS细胞寄予了很高的期待。小编很好奇,iPS细胞打哪来,干什么的,又有怎样的“魔力”。本文试图勾勒iPS细胞的来龙去脉,水平有限,不当之处,敬请大家指教。
2006年,在日本京都大学的一间办公室里,“我们得到细胞种群了!”博士后Kazutoshi Takahashi激动地不断念叨。她的导师Shinya Yamanaka起初还满脸惊疑,但很快从桌子上一跃而起,飞奔组织培养室。在显微镜下,他看到了微小的细胞簇。这是他们5年以来工作的顶峰,一开始他本人也不敢确信能取得这一成果。
两周前,Takahashi采集了成年小鼠皮肤细胞,然后借助病毒载体,将精心筛选的24个基因导入这些皮肤细胞。此时,这些细胞发生了转变,它们形态和功能像极了胚胎干细胞(Embryonic Stem Cells, ES)。它们具有分化成皮肤、神经、肌肉以及其它各种特殊细胞的能力。Yamanaka凝视着面前这些充满“魔力”的细胞,思绪万端。“那时,我在想,我们是不是犯了一些错误,”Yamanaka回忆道。他让Takahashi一再重复这个实验,然而每次都得到了同样的结果。
又过了两个月,Takahashi把诱导基因精简为4个。2006年6月,在加拿大多伦多举行的国际干细胞研究年度会议上,Yamanaka宣布了这一成果,满室哗然。起初,他称这个种细胞为胚样细胞(ES-like cells),但后来更倾向于诱导多功能干细胞( induced pluripotent stem cells, iPS )这个叫法。“在场的很多人都不相信他的结论,”Rudolf Jaenisch说道,他来自Massachusetts Institute of Technology in Cambridge。 但Jaenisch理解并相信Takahashi的工作,“我觉得那是一件很‘神奇’的事。”
iPS细胞为再生医学(regenerative medicine)带来了福音。研究者可以从患者的皮肤、血液或者其它部位采集细胞,经“初始化(reprogram)”转变为iPS细胞。iPS细胞可以分化为肝细胞、神经细胞以及其它任何可以用来治病的细胞类型。这种个性化的治疗方式避免了免疫排斥反应,同时也回避了采用胚胎细胞治疗所引起的伦理问题。
如今,10多年过去了,当年的目标已经发生些许偏移。部分原因是研究者对iPS细胞治疗所面临的困难估计不足。如果没有2017年开展的这次临床试验,研究者们只在2015年进行过一次临床试验,而且因某些突发情况,试验只完成一例就被迫终止。
但是,iPS细胞却在其它领域崭露头角。在人类疾病模型构建与研究以及药物筛选过程中,iPS细胞已经成为强有力的工具;随着细胞培养技术,特别是基因编辑技术的提高,iPS细胞已经成为生化实验室的主角儿,它能轻松提供过去很难获得的某些组织细胞。“在人体发育和神经疾病的研究中,iPS细胞意义重大。”Guo-li Ming说道,他是一名神经学家,来自Johns Hopkins University in Baltimore, Maryland,从2006年就开始借助iPS细胞进行研究。
iPS细胞技术在治疗领域:命运多舛
在公布结果4周后,Yamanaka 和Takahashi发表了鉴定出的这4个基因,分别是Oct3/4、Sox2、 Klf4 和c-Myc,它们在诱导成人细胞“初始化”的过程中起着关键的作用。此后一年,全球3-4家实验室都在优化诱导细胞“初始化”的方法。又经过半年的努力,Yamanaka 和 James Thomson在University of Wisconsin-Madison成功地“初始化”了成人细胞。世界各大实验室蜂拥而至,到2009年末,大约有300篇学术论文中用到了iPS细胞技术。
很多实验室都在探索成人哪些细胞类型可以被“初始化”转变为iPS细胞,以及iPS细胞又能分化为哪些类型的细胞。也有一些实验室在探索不使用c-Myc基因可能性,因为这一基因具有潜在的诱导某些细胞癌变的能力。再后来,大家的关注点就集中在如何让这些导入的基因不被整合进细胞基因组内,这是基于iPS细胞治疗的首要安全问题。
另一个重大问题就是,iPS细胞与胚胎干细胞究竟有多大的相似性。随着研究的深入,它们的差异开始显现。研究者发现,iPS细胞保有表观遗传记忆(epigenetic memory),它是一种DNA上的化学标记物模型,能够反映出iPS细胞是从哪种细胞类型分化而来的。但研究者们普遍认为,这样的差异不会影响iPS细胞在治疗疾病上的应用。
2012年,因在iPS细胞方面的工作,Yamanaka分享了诺贝尔生理或医学奖。此时,首例基于iPS细胞的治疗的试验方案正在谋划中。Masayo Takahashi,一名供职于RIKEN
Center for Developmental Biology (CDB) in Kobe的眼科医生,正在研究用胚胎干细胞治疗视网膜疾病的方法。当他看到Yamanaka的文章,就迅速地转向iPS细胞,然后开始寻求与Yamanaka的合作。
2013年,她的团队采集两个老年黄斑变性患者的皮肤细胞,重新编程为iPS细胞,构建用于临床试验的视网膜色素上皮细胞( retinal pigment epithelium, RPE)薄层。2014年9月,研究者把RPE薄层移植入一名70岁女性患者的右眼内,Takahashi表示,那次治疗阻止了黄斑变性的恶化,使患者感受到视觉的明亮。
正当研究团队准备治疗第二名患者的时候,他们检测出两名患者的iPS细胞以及RPE细胞基因均有两处微小变异,虽然没有证据表明这些突变具有致癌作用,但为安全考虑,Yamanaka 建议Takahashi暂停试验进程。
这次意外也让其他投身于此的研究者们犹豫起来,“全球的研究者都在关注着试验的进展,” David Brindley说道,他在University of Oxford, UK研究干细胞的调控和制备。干细胞技术从发现到商业应用花费了将近20年,“所以,iPS细胞技术也会经历长期艰辛的打磨。”
在美国,The Astellas Institute for Regenerative Medicine in Marlborough, Massachusetts也在开展基于iPS细胞技术治疗的规划,包括治疗黄斑变性和青光眼。首席科学家Robert Lanza表示,对于目前任何一个治疗试验,研究者都要花费数年去开发一套可行的方法,来获得足量的、足够纯净的既定类型细胞。“目前,iPS细胞是进入临床试验阶段的最复杂、最多变的治疗技术,”Lanza说道,“我期待着这些细胞走向临床,但前期需要大量的准备工作。”
另外一个挑战是,应该做哪些工作来确保类似的临床试验被准许。 Loring希望两年后应用iPS细胞技术治疗帕金森疾病,但这并不容易。Loring打算进行一系列复杂的检测和确认工作,以此向FDA证明每个细胞系都足够安全。
iPS细胞治疗代价高昂。“治疗每名患者需要花费大约一年的时间和一百万美元。”Yamanaka说道。他希望未来治疗用的iPS细胞来源于志愿者的捐赠,而不是从每个病人身上获取。他已经着手建立这样的一个细胞银行(cell bank)。Takahashi打算比对细胞银行内来自不同捐赠者的iPS细胞,她希望找出这些细胞的免疫原差异,让iPS细胞服务更多人群。
2017年3月28日,一位六十多岁的日本男子接受了一种特殊细胞的治疗,这种特殊细胞从他人捐赠的诱导多功能干细胞(Induced Pluripotent Stem Cells, iPS)分化而来,这是世界首例异体iPS细胞移植手术。在术后的记者招待会上,Takahashi表示移植手术进展顺利,但能否取得成功还有赖于移植细胞的生长状态,这需要一段时间的观察。她表示,只有完成方案设定的5步流程后,才会有进一步的进展报告。
iPS细胞技术在医药研发领域:开枝散叶
虽然iPS细胞在治疗领域一再碰壁,但在其它应用方面则遍地开花。利用最近流行的基因编辑工具 CRISPR-Cas9,可以使研究者把与疾病相关的突变基因导入iPS细胞内,然后与那些未被修饰的iPS细胞进行比对。Jaenisch的实验室每天都在用CRISPR-Cas9处理iPS细胞,“我们可以做任何想要获得的突变。”他讲道。
为研究寨卡病毒( Zika),一种侵染怀孕妇女,可致胎儿小头症畸形的病毒,Ming和他的同事利用iPS细胞构建了类似大脑的组织,然后暴露于存在寨卡病毒的环境中,他们发现,病原体优先侵入神经干细胞,导致神经细胞死亡和大脑皮层区减小,这和小头畸形胎儿的状况类似。
其他的研究者则利用iPS细胞制备了“迷你小肠”、“迷你肝脏”等类器官。通过iPS细胞揭示的疾病新发现也越来越多。比如,在青光眼患者中,有研究者发现某一基因的复制可导致神经细胞簇的死亡;还有研究者利用iPS细胞技术发现了与亨廷顿舞蹈症相关的基因,以及神经细胞的改变。
iPS细胞也被成功地应用于新药研发领域。通过iPS细胞创造出丰富的疾病细胞模型,用于药物的筛选和检测。比如,在2012年,来源于一名神经发育缺陷患者的神经干细胞,被用于筛选了将近7000个小分子药物,并鉴定出了一个潜在的先导化合物。
尽管重新编程细胞的操作已开展了十多年,人们依然不清楚这一过程发生的细节。目前研究者的工作重点在于,通过检测细胞的基因组、基因表达模型等来系统地核查细胞系的身份以及安全性。Yamanaka也致力于iPS细胞库的建设,收集多样化的免疫兼容性(immunologically compatible)iPS细胞,以满足未来大多数人的治疗使用。
为了推动细胞治疗的进展,Yamanaka呼吁制药企业和政府部门应该对iPS细胞研究者提供更多的支持;同时强调,对于药物研发和疾病模型的构建,研究者一定要更具耐心。“iPS细胞技术可以缩短研发时间,但不能完全跳过去,”他讲道,“无论是iPS细胞技术还是任何其他的新技术,起初它们都没有‘点石成金’的魔力,都需要经历长时间的打磨才能无往不利。”
医谷链
《重大突破!日本完成世界首例异体诱导性多能干细胞移植临床试验!》
参考文献
1. Takahashi, K. & Yamanaka, S. Cell 126, 663–676 (2006).
2. Okita, K., Ichisaka, T. & Yamanaka, S. Nature 448, 313–317 (2007).
3. Wernig, M. et al. Nature 448, 318–324 (2007).
4. Maherali, N. et al. Cell Stem Cell 1, 55–70 (2007).
5. Takahashi, K. et al. Cell 131, 861–872 (2007).
6. Yu, J. et al. Science 318, 1917–1920 (2007).
7. Nakagawa, M. et al. Nature Biotechnol. 26, 101–106 (2007).
8. Kim, K. et al. Nature 467, 285–290 (2010).
9. Paquet, D. et al. Nature 533, 125–129 (2016).
10. Qian, X. et al. Cell 165, 1238–1254 (2016).
11. Tucker, B. A. et al. J. Stem Cell Res. Ther. 3, 161 (2014).
12. HD iPSC Consortium Cell Stem Cell 11, 264–278 (2012).
13. Lee, G. et al. Nature Biotechnol. 30, 1244–1248 (2012).
14. Cao, L. et al. Sci. Transl. Med. 8, 335ra56 (2016).
来源:新浪医药新闻 作者:拂晓
为你推荐
 资讯
资讯 圣因生物完成超 1.1 亿美元 B 轮融资,加速 RNAi 疗法全球布局
本轮融资由知名产业机构领投,国际主权基金、中国生物制药、君联资本等十余家机构跟投,全球制药巨头礼来公司战略入局,高瓴创投、启明创投等现有股东持续加码支持,融资规模创...
2025-12-12 16:59
 资讯
资讯 投后估值达21.37亿元,实体瘤细胞治疗领军企业君赛生物递表港交所
君赛生物共有5款在研产品,其中核心产品也是进展最快的是GC101,正开展上市前的关键II期临床试验,有望成为国内首个获批上市的TIL细胞创新药
2025-12-12 09:24
 资讯
资讯 ESMO-IO | ORR达41.7%!君赛生物GC101 TIL治疗晚期后线非小细胞肺癌I期数据首次公布
这不仅是全球首个无需高强度清淋化疗、无需IL-2给药的TIL疗法治疗肺癌的临床研究,也是国内首个公开披露该领域数据的注册性临床研究。
2025-12-12 09:17
 资讯
资讯 君合盟生物启动重组 A 型肉毒毒素治疗成人上肢痉挛状态临床 III 期试验,并完成首例患者入组
该临床试验由复旦大学附属华山医院李放教授和上海市养志康复医院(即上海市阳光康复中心)靳令经教授联合牵头
2025-12-11 21:06
 资讯
资讯 Medidata发布全新调研报告:临床试验AI应用价值凸显,超七成用户反馈“达到或超预期”
基于对来自全球制药公司、生物科技公司及合同研究组织(CRO)中超200位核心决策者的深度调研,报告显示,目前AI在改善患者招募、优化数据管理、控制运营成本和提升试验效率等方...
2025-12-11 20:57
 资讯
资讯 近20年首个全新类别抗菌药物醋酸来法莫林纳入医保,开启中国成人社区获得性肺炎治疗普惠新篇章
该产品继2025年6月30日获得国家药品监督管理局批准用于治疗成人社区获得性肺炎(CAP)后又纳入国家医保目录
2025-12-11 20:50
 资讯
资讯 专注 “生物学 + AI” ,普瑞基准完成超亿元 D 轮融资,加速 AI 驱动新药研发
本轮融资由信立泰、广投资本、申宏中恒基金联合领投,老股东金谷汇枫、聚翊投资持续跟投
2025-12-10 15:55
 资讯
资讯 别把“嗜睡”当懒癌!新型促觉醒药翼朗清®获批,专注维持日间清醒
促觉醒药物翼朗清®(盐酸索安非托片)正式获得中国国家药品监督管理局(NMPA)批准,用于改善阻塞性睡眠呼吸暂停(OSA)伴有日间过度嗜睡(EDS)的成人患者的觉醒程度。
2025-12-10 11:04
 资讯
资讯 复星医药将其GLP-1产品全球化权益授权辉瑞,总里程碑付款近150亿人民币
12月9日晚间,复星医药发布公告称,公司控股子公司药友制药、复星医药产业与辉瑞共同签订《许可协议》,(其中主要包括)由药友制药就口服小分子胰高血糖素样肽-1受体(GLP-1R)...
2025-12-10 09:12
 资讯
资讯 Capricor Therapeutics公司宣布外泌体疗法Deramiocel在DMD三期中取得积极成果
近日,专注与外泌体疗法的Capricor Therapeutics(纳斯达克代码:CAPR)公司宣布其核心管线Deramiocel在杜氏肌营养不良症关键三期 HOPE-3 研究中取得积极成果。
2025-12-09 16:38
 资讯
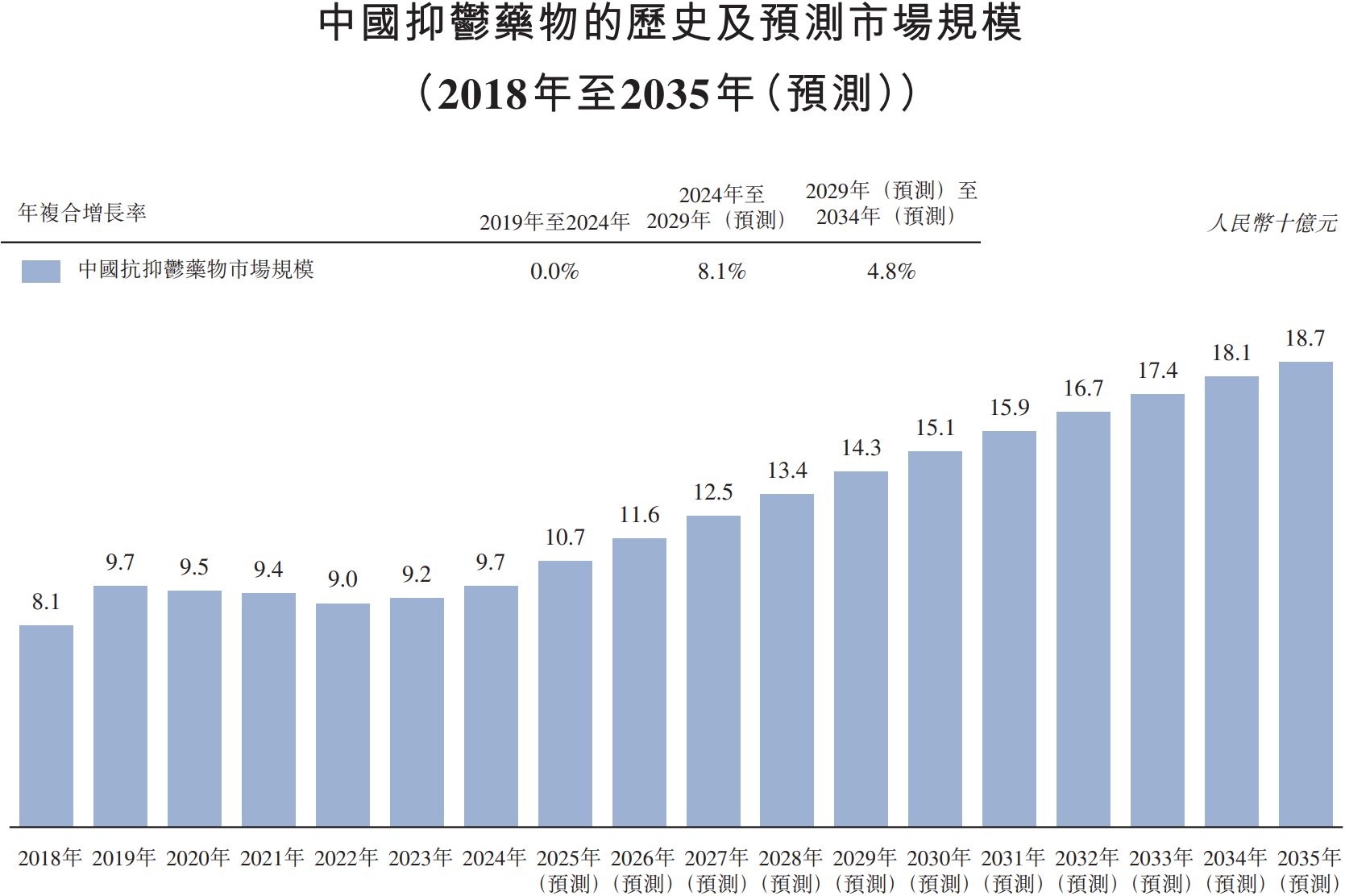
资讯 中药1类创新药剑指抑郁症治疗蓝海,远大医药GPN01360成功达到国内II期临床终点
国产抗抑郁症药物研发取得重大进展。近日,远大医药(0512 HK)的1 1类中药创新药GPN01360国内II期临床研究成功达到临床终点,产品表现出显
2025-12-08 18:27