TIL是肿瘤细胞免疫治疗中的重要组成部分。第一代的TIL,仅仅只有分离,扩增,回输3个阶段,无法从复杂的TIL细胞群中获得肿瘤特异性的T淋巴细胞。以SteveRosenberg教授为代表人物的第二代TIL,包括了分离,筛选,扩增,回输4个阶段,筛选出肿瘤特异性TIL再进行扩增,大大提高了TIL治疗肿瘤疾病的有效性。但是由于TIL制备技术复杂,国内目前医院提供的都还只是第一代的TIL。
TIL
TIL, 英文全称Tumor Infiltrating Lymphocyte,中文全称“肿瘤浸润淋巴细胞”。早在1988年,Steve Rosenberg教授就用肿瘤病人自身的TIL来治疗转移性黑素瘤。随着技术的革新与进步,2004年Steve Rosenberg教授在PNAS上发表文章指出:肿瘤特异性的TIL治疗转移性黑色素瘤的临床有效率大于50%,35个病人中18名病人有响应,其中4人完全响应(图1)。近年来,非常多的文献发表,指出病理切片中肿瘤组织周围TIL的存在和数目和病人的预后良好相关。有研究者建议把TIL作为T (Tumor, 原发肿瘤范围)N(Node, 淋巴结转移)M(Metastasis, 远端转移)之外,另外一个判断肿瘤分期和预后的重要标准。
图1,一名黑素瘤全身多发转移的病人(左)TIL治疗一个月后达到完全响应(右),摘自Rosenberg,S.A. (2004) PNAS 101, 14639-14645
那么肿瘤特异性的TIL到底是如何被用来治疗肿瘤的呢?
我们仍然借用SteveRosenberg教授2008年发表在Nature Reviews上的一张图来说明(图2)。第一步,我们得到病人的肿瘤组织块,其中混杂着体积较大的肿瘤细胞(浅蓝色)以及体积小而圆的T淋巴细胞(红色,绿色,深蓝色);第二步,将不同种类的T淋巴细胞在细胞板上克隆化,并加入高浓度的IL-2来选择培养;第三步,在IL-2的刺激下不同种类的T淋巴细胞都得到了克隆扩增,形成了细胞群;第四步,用病人的肿瘤细胞和扩增后的T淋巴细胞反应,凡是能够发生杀瘤效应的T淋巴细胞群作为阳性TIL群留下(红色),其余的丢弃(绿色,深蓝色);第五步,用负载了肿瘤特异性抗原的树突状细胞(DC)进一步扩增培养肿瘤特异性的TIL;最后,回输给预先做了清髓的肿瘤病人。
图2、肿瘤特异性TIL制备的全过程,摘自Rosenberg,S.A. (2008) Nature Review 8, 299-308
TIL治疗有哪些局限性呢?
正是由于TIL杀灭肿瘤的特异性和高效性,才在临床应用上获得了很好的客观有效率。那么,作为肿瘤细胞免疫疗法,TIL治疗有哪些局限行呢?第一,TIL制备技术复杂,通常需要筛选上百个甚至几百个T淋巴细胞克隆才能得到肿瘤特异性的TIL;第二,TIL在T淋巴细胞分类中属于效应T细胞(effector T cell), 虽然杀瘤功能强大但是寿命短,不具备记忆能力(图3)。第三,局限于新鲜且无菌保存的肿瘤组织样本,对于那些无法提供此类样本的病人,无法提供TIL治疗;第四,部分肿瘤病人由于TIL数量过少或者没有,无法从肿瘤组织样本中分离得到TIL,而这类病人往往预后更差。
解决TIL治疗局限性的对策
为了解决第一个局限性,2014年Steve Rosenberg教授在JCI上发表文章,指出PD1阳性的CD8+TIL与PD1阴性的CD8+TIL相比,更容易分离得到肿瘤特异性的TIL。针对第二个局限性,Steve Rosenberg教授从TIL中得到的肿瘤特异性T淋巴细胞中进一步获得其T淋巴细胞受体(TCR)的遗传信息,通过基因修饰的手段转化病人的外周血中T淋巴细胞,再去治疗病人,从而也解决了第三和第四个局限性。
来源:源正细胞 作者:韩研妍
为你推荐
 资讯
资讯 圣因生物完成超 1.1 亿美元 B 轮融资,加速 RNAi 疗法全球布局
本轮融资由知名产业机构领投,国际主权基金、中国生物制药、君联资本等十余家机构跟投,全球制药巨头礼来公司战略入局,高瓴创投、启明创投等现有股东持续加码支持,融资规模创...
2025-12-12 16:59
 资讯
资讯 投后估值达21.37亿元,实体瘤细胞治疗领军企业君赛生物递表港交所
君赛生物共有5款在研产品,其中核心产品也是进展最快的是GC101,正开展上市前的关键II期临床试验,有望成为国内首个获批上市的TIL细胞创新药
2025-12-12 09:24
 资讯
资讯 ESMO-IO | ORR达41.7%!君赛生物GC101 TIL治疗晚期后线非小细胞肺癌I期数据首次公布
这不仅是全球首个无需高强度清淋化疗、无需IL-2给药的TIL疗法治疗肺癌的临床研究,也是国内首个公开披露该领域数据的注册性临床研究。
2025-12-12 09:17
 资讯
资讯 君合盟生物启动重组 A 型肉毒毒素治疗成人上肢痉挛状态临床 III 期试验,并完成首例患者入组
该临床试验由复旦大学附属华山医院李放教授和上海市养志康复医院(即上海市阳光康复中心)靳令经教授联合牵头
2025-12-11 21:06
 资讯
资讯 Medidata发布全新调研报告:临床试验AI应用价值凸显,超七成用户反馈“达到或超预期”
基于对来自全球制药公司、生物科技公司及合同研究组织(CRO)中超200位核心决策者的深度调研,报告显示,目前AI在改善患者招募、优化数据管理、控制运营成本和提升试验效率等方...
2025-12-11 20:57
 资讯
资讯 近20年首个全新类别抗菌药物醋酸来法莫林纳入医保,开启中国成人社区获得性肺炎治疗普惠新篇章
该产品继2025年6月30日获得国家药品监督管理局批准用于治疗成人社区获得性肺炎(CAP)后又纳入国家医保目录
2025-12-11 20:50
 资讯
资讯 专注 “生物学 + AI” ,普瑞基准完成超亿元 D 轮融资,加速 AI 驱动新药研发
本轮融资由信立泰、广投资本、申宏中恒基金联合领投,老股东金谷汇枫、聚翊投资持续跟投
2025-12-10 15:55
 资讯
资讯 别把“嗜睡”当懒癌!新型促觉醒药翼朗清®获批,专注维持日间清醒
促觉醒药物翼朗清®(盐酸索安非托片)正式获得中国国家药品监督管理局(NMPA)批准,用于改善阻塞性睡眠呼吸暂停(OSA)伴有日间过度嗜睡(EDS)的成人患者的觉醒程度。
2025-12-10 11:04
 资讯
资讯 复星医药将其GLP-1产品全球化权益授权辉瑞,总里程碑付款近150亿人民币
12月9日晚间,复星医药发布公告称,公司控股子公司药友制药、复星医药产业与辉瑞共同签订《许可协议》,(其中主要包括)由药友制药就口服小分子胰高血糖素样肽-1受体(GLP-1R)...
2025-12-10 09:12
 资讯
资讯 Capricor Therapeutics公司宣布外泌体疗法Deramiocel在DMD三期中取得积极成果
近日,专注与外泌体疗法的Capricor Therapeutics(纳斯达克代码:CAPR)公司宣布其核心管线Deramiocel在杜氏肌营养不良症关键三期 HOPE-3 研究中取得积极成果。
2025-12-09 16:38
 资讯
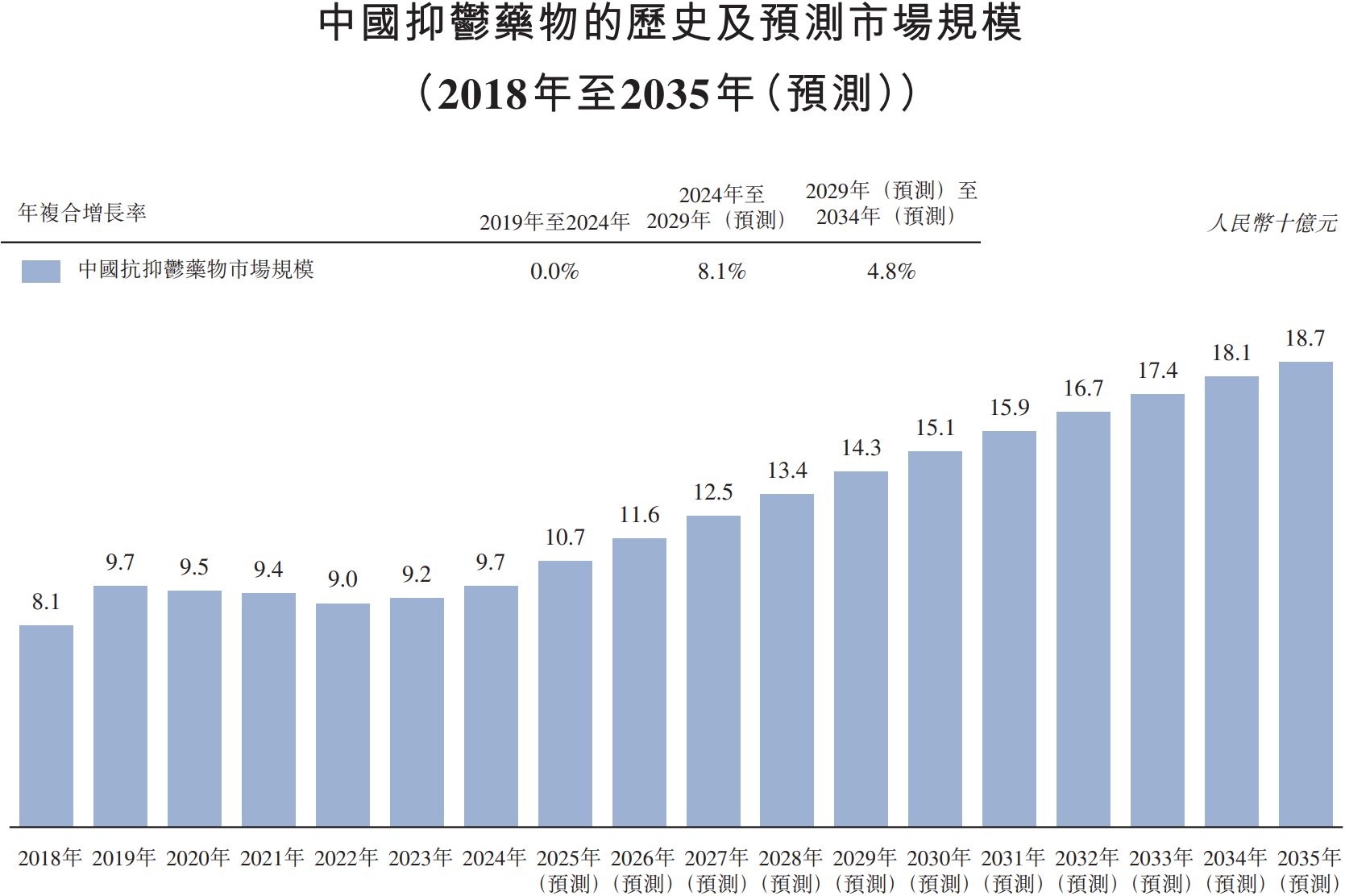
资讯 中药1类创新药剑指抑郁症治疗蓝海,远大医药GPN01360成功达到国内II期临床终点
国产抗抑郁症药物研发取得重大进展。近日,远大医药(0512 HK)的1 1类中药创新药GPN01360国内II期临床研究成功达到临床终点,产品表现出显
2025-12-08 18:27